
еОЯеРНпЉЪSingle-cell analysis of human B cell maturation predicts how antibody class switching shapes ¬†selection dynamics
иѓСеРНпЉЪдЇЇз±їBзїЖиГЮжИРзЖЯзЪДеНХзїЖиГЮеИЖжЮРйҐДжµЛжКЧдљУз±їеИЗжНҐе¶ВдљХељ±еУНйАЙжЛ©еК®еКЫе≠¶
еПСи°®жЬЯеИКпЉЪScience immunology
еПСи°®жЧ•жЬЯпЉЪ2021еєі2жЬИ12
ељ±еУНеЫ†е≠РпЉЪ24.8
иГМжЩѓ
¬† ¬†¬† дЄЇдЇЖжПРйЂШжИСдїђеѓєдЇЇBзїЖиГЮеЬ®дљУеЖЕжИРзЖЯињЗз®ЛдЄ≠зїЖиГЮгАБиљђељХеТМжКЧдљУеЇУеК®жАБзЪДзРЖиІ£пЉМдљЬиАЕеѓєдЄАзІН襀府ж≥Ыз†Фз©ґзЪДSLOж®°еЮЛвАФвАФдЇЇжЙБж°ГдљУињЫи°МдЇЖжЧ†еБПзЪДеНХзїЖиГЮиљђељХзїДе≠¶еТМеЇУеИЖжЮРгАВињЩдЇЫжХіеРИзЪДе§ІеЃєйЗПеТМеНХзїЖиГЮжКЧдљУеЇУдЄОеНХзїЖиГЮиљђељХзїДе≠¶йЕНеѓєпЉМиГље§ЯеЃЪдєЙиљђељХBзїЖиГЮзКґжАБпЉМеМЕжЛђиѓ¶зїЖжΥ糥MBCеЉВиі®жАІпЉМйЗНеїЇжЧґйЧіеЯЇеЫ†и°®иЊЊеК®жАБпЉМеєґиІ£еЖ≥дЄОжКЧдљУз±їеИЂеИЗжНҐзЫЄеЕ≥зЪДGCеТМMBCsзЪДеКЯиГљгАВдЇЇз±їBзїЖиГЮжИРзЖЯзЪДиЈѓзЇњеЫЊжПРдЊЫдЇЖеЙНжЙАжЬ™жЬЙзЪДBзїЖиГЮдїЛеѓЉеЕНзր嚥жИРзЪДеИЖиЊ®зОЗпЉМжШѓз†Фз©ґж≠£еЄЄеТМзЧЕзРЖBзїЖиГЮеПНеЇФзЪДеЃЭиіµиµДжЇРгАВ
еЃЮй™МиЃЊиЃ°
¬† ¬† ¬†йАЪињЗеѓєеЈ≤еИЖз±їзЪДBзїЖиГЮзЊ§дљУињЫи°Ме§ІйЗПжКЧдљУеЇУжµЛеЇПпЉИBulk BCR-seqпЉЙпЉМзїУеРИдљњзФ®еНХзїЖиГЮиљђељХзїДе≠¶еТМVDJ-seqеѓєеЯЇеЫ†и°®иЊЊеТМеЇУињЫи°МжЧ†еБПжАІи°®еЊБпЉМжЭ•и°®еЊБдЇЇз±їжЙБж°ГдљУBзїЖиГЮзКґжАБзЪДжКЧдљУеЇУгАВ
1.дљњзФ®дЇЖжО•еПЧеЄЄиІДжЙБж°ГдљУеИЗйЩ§жЬѓзЪДеДњзЂ•жВ£иАЕ(>3е≤Б)зЪДжЙБж°ГдљУж†ЈжЬђпЉМ
2.е∞Же§ІйЗПжКЧдљУеЇУеТМеНХзїЖиГЮжКЧдљУеЇУдЄАиµЈеИЖжЮРпЉМдї•ж£АжЯ•жКЧдљУеЇУзЪДдЇЪзЊ§зЙєеЉВжАІзЙєеЊБпЉМеєґеЬ®scVDJ-seqиѓХй™МдЄ≠еҐЮеК†йЙіеЃЪеЕЛйЪЖзЫЄеЕ≥BзїЖиГЮзЪДиГљеКЫгАВ
3.еЕНзЦЂзїЖиГЮзЊ§жШѓйАЪињЗscRNA-seqжХ∞жНЃйЫЖзЪДжЧ†еБПиБЪз±їдї•еПКеЈ≤зЯ•еТМдї•еЙНжЬ™жК•йБУзЪДеЯЇеЫ†и°®иЊЊж†ЗиЃ∞еТМBзїЖиГЮдЇЪзЊ§жКЧдљУеЇУзЙєеЊБзЪДж≥®йЗКжЭ•йЙіеЃЪзЪДгАВ
4.зФ®жµБеЉПзїЖиГЮжЬѓињЫдЄАж≠•ж£АжµЛжЦ∞йЙіеЃЪзЪДзІНзЊ§гАВжЛЯжЧґеЇПеИЖжЮРжШѓдЄЇдЇЖж£Ай™МдЄНеРМBзїЖиГЮжИРзЖЯйШґжЃµдєЛйЧізЪДеЕ≥з≥їгАВ
5.дЄЇдЇЖй™МиѓБжКЧдљУз±їеИЂдЄОBзїЖиГЮеСљињРеТМеКЯиГљзЫЄеЕ≥зЪДеБЗиЃЊпЉМе∞ЖжКЧдљУз±їеИЂзЙєеЉВжАІBзїЖиГЮзЪДеНХзїЖиГЮиљђељХзїДдЄОеМєйЕНзЪДSHMйҐСзОЗињЫи°МдЇЖжѓФиЊГпЉМеєґињЫи°МдЇЖеЈЃеЉВеЯЇеЫ†и°®иЊЊеТМйАФеЊДеѓМйЫЖеИЖжЮРгАВ
зїУжЮЬ
01еЃЪдєЙдЇЇжЙБж°ГдљУBзїЖиГЮзЪДжКЧдљУCSRеЫЊи∞±
¬† ¬† ¬†е§Іе§ЪжХ∞дЇЇз±їйЂШйАЪйЗПжКЧдљУеЇУжµЛеЇПз†Фз©ґйГљж£АжµЛдЇЖе§ЦеС®и°АBзїЖиГЮдЇЪзЊ§пЉМињЩдЄОжіїжАІSLOsзЪДеК®жАБеЇУдЇЪеЯЇжЬђдЄНеРМгАВдЄЇдЇЖжПРдЊЫдЇЇз±їжЙБж°ГдљУжКЧдљУеЇУжЩѓиІВзЪДдЇЪз±їзЙєеЉВжАІеТМеЃЪйЗПеИЖжЮРпЉМдљЬиАЕдљњзФ®зЛђзЙєзЪДеИЖе≠Рж†ЗиѓЖзђ¶пЉИUMIпЉЙеѓєеЫЫдЄ™еєњдєЙжЙБж°ГдљУBзїЖиГЮдЇЪзЊ§зЪДжКЧдљУеЇУињЫи°МдЇЖna√ѓve, GC, memoryеТМPBsжµЛеЇПпЉИеЫЊ1AпЉЙгАВ
¬† ¬† ¬† дљЬиАЕеИЖжЮРдЇЖе§НеПСжАІжЙБж°ГдљУзВОжВ£иАЕеТМйШїе°ЮжАІзЭ°зЬ†еСЉеРЄжЪВеБЬжВ£иАЕзЪДжЙБж°ГдљУBзїЖиГЮпЉМеПСзО∞е§ІйЗПиНІеЕЙжіїеМЦзїЖиГЮеИЖйАЙ(FACS)еИЖйАЙзЪДBзїЖиГЮеЇУдЄОдЊЫдљУеМєйЕНзЪДжЬ™еИЖйАЙеНХзїЖиГЮжКЧдљУеЇУдєЛйЧіе≠ШеЬ®иЙѓе•љзЪДдЄАиЗіжАІ(еЫЊ2)гАВж≠£е¶ВйҐДжЬЯзЪДйВ£ж†ЈпЉМna√ѓve BзїЖиГЮеЇУдЄїи¶БжЬ™еИЗжНҐеТМжЬ™з™БеПШгАВGCеТМMBCsзФ±еЉАеЕ≥еТМжЬ™еЉАеЕ≥зЪДIgHеЇПеИЧзїДжИРпЉМSHMеНЗйЂШпЉМPBsеЗ†дєОеЕ®йГ®еЉАеЕ≥еТМйЂШеЇ¶з™БеПШ(еЫЊ1BеТМC)гАВ
¬† ¬† ¬† GCеЖЕиЊГйЂШзЪДIgH-SHMйҐСзОЗйАЪеЄЄеПНжШ†еЗЇиЊГйЂШзЪДдЇ≤еТМжАІBCRsпЉМ庴襀聧䪯䚜GC BзїЖиГЮеАЊеРСдЇОPBиАМдЄНжШѓMBCеСљињРгАВдЄОж≠§дЄАиЗізЪДжШѓпЉМжЙБж°ГдљУдЄ≠PBи°НзФЯзЪДеЯЇеЫ†еЇУйАЪеЄЄжѓФMBCsеРЂжЬЙжЫійЂШзЪДSHMйҐСзОЗ(еЫЊ1C)гАВзДґиАМпЉМйАЪињЗиІ£жЮРжКЧдљУдЇЪз±їпЉМдљЬиАЕеПСзО∞SHMж∞іеє≥еЬ®дЄНеРМзЪДжИРзЖЯBзїЖиГЮдЇЪзЊ§дєЛйЧіе§ІиЗізЫЄдЉЉпЉМйЩ§дЇЖIgDпЉМеєґдЄФж≤њзЭАеЕНзЦЂзРГиЫЛзЩљдљНзВєзЪДйҐСзОЗеҐЮеК†(еЫЊ1D)гАВ
¬† ¬† ¬† жѓФиЊГдЇЪз±їзЙєеЉВжАІMBCsеТМPBsзЪДеЕЛйЪЖе§Ъж†ЈжАІеПСзО∞пЉМдЄОзЫЄеРМеРМеЮЛзЪДPBsзЫЄжѓФпЉМжЬ™еИЗжНҐзЪДеТМIgA+MBCsзЪДеЕЛйЪЖжЙ©еҐЮиЊГе∞С(зФ±жЫійЂШзЪДе§Ъж†ЈжАІиѓБжШО)пЉМиАМIgG+ MBCsеТМPBsзЪДеЕЛйЪЖжЙ©еҐЮз®ЛеЇ¶зЫЄдЉЉ(еЫЊ1E)гАВињЩеПѓиГљдЄНиГљзФ®SHMйҐСзОЗзЪДеЈЃеЉВжЭ•иІ£йЗК(еЫЊ1D)пЉМдљЖеПѓиГљеПНжШ†дЇЖдЄОCSRзїУжЮЬзЫЄеЕ≥зЪДеЃГдїђзЪДйАЙжЛ©жИЦзїЖиГЮеСљињРиІДж†ЉзЪДеЈЃеЉВгАВељУдљЬиАЕж£АжЯ•ињЩдЇЫеєњж≥ЫеЃЪдєЙзЪДBзїЖиГЮзЊ§дЄ≠зЪДжКЧдљУдЇЪз±їйҐСзОЗжЧґпЉМдљЬиАЕеПСзО∞пЉМйЩ§дЇЖдњЭзХЩIgMи°®иЊЊзЪДеАЊеРСеҐЮеК†е§ЦпЉМMBCsи°®иЊЊIgA1жИЦIgA2зЪДеПѓиГљжАІеИЖеИЂжШѓPBsзЪД3.3еАНжИЦ7.3еАНпЉМиАМPBsжЫіеПѓиГљи°®иЊЊIgG1(еЫЊ1F)гАВињЩдЇЫеѓМйЫЖдЄОзЙєеЃЪзЪДBзїЖиГЮеСљињРжЬЙеЕ≥пЉМзФЪиЗ≥еѓєдЇОиЈ®иґКдЄНеРМдЇЪзЊ§зЪДжЙ©е±ХеЕЛйЪЖдєЯжШѓе¶Вж≠§(еЫЊ1G)гАВ
¬† ¬†¬† дЄЇдЇЖжΥ糥ињЩдЇЫдЇЪзЊ§зЙєеЉВжАІз±їеИЗжНҐж®°еЉПжШѓе¶ВдљХдЇІзФЯзЪДпЉМдљЬиАЕйЗНеїЇдЇЖ28,845дЄ™жЙ©еҐЮеЕЛйЪЖзЪДз≥їзїЯеПСиВ≤пЉМеєґиЃ°зЃЧдЇЖеЬ®еѓЖеИЗзЫЄеЕ≥зЪДBзїЖиГЮдєЛйЧіеПСзФЯзЙєеЃЪCSRдЇЛдїґзЪДеПѓиГљжАІпЉМиАМдЄНжШѓеБґзДґеПСзФЯзЪДеПѓиГљжАІ(еЫЊ1H)пЉМз±їдЉЉдЇОеЬ®е§ЦеС®и°АBзїЖиГЮдЄ≠ињЫи°МзЪДеИЖжЮРгАВMBCеЕЛйЪЖи∞±з≥їжШЊз§ЇеЗЇжЫіе§ІзЪДеПѓиГљжАІпЉМеЬ®ж≤њзЭАIgHдљНзВєзЪДзЇњжАІз©ЇйЧідЄ≠пЉМеѓЖеИЗзЫЄеЕ≥зЪДеРМеЮЛеѓєеПСзФЯеИЗжНҐгАВдЄОPBеЕЛйЪЖзЫЄжѓФпЉМPBеЕЛйЪЖи°®зО∞еЗЇжЫіеєњж≥ЫзЪДеРМеЮЛеИЗжНҐж®°еЉП(еЫЊ1H)гАВжЧ†иЃЇжШѓжКЧдљУдЇЪз±їйҐСзОЗињШжШѓйЗНзїДзЪДз±їеИЗжНҐе±Вжђ°йГљдЄОGCзїЖиГЮйЭЮеЄЄзЫЄдЉЉпЉМињЩдЄОжПРеЗЇзЪДGCзїЖиГЮйЪПжЬЇйААеЗЇзЪДж®°еЮЛдЄАиЗіпЉМиАМдЄНжШѓжµЖзїЖиГЮеСљињРзЪДдЄїеК®йАЙжЛ©гАВ
жАїдєЛпЉМињЩдЇЫеИЖжЮРжПРдЊЫдЇЖиѓБжНЃпЉМиѓБжШОеЯЇдЇОжКЧдљУзЪДйАЙжЛ©жЬЇеИґеѓєдЇОдЄ§зІНдЄїи¶БзЪДBзїЖиГЮеСљињРдЄНеРМпЉМињЩдЉЉдєОдЄОжИРзЖЯжЧ©жЬЯCSRзЪДзїУжЮЬжЬЙеЕ≥гАВ
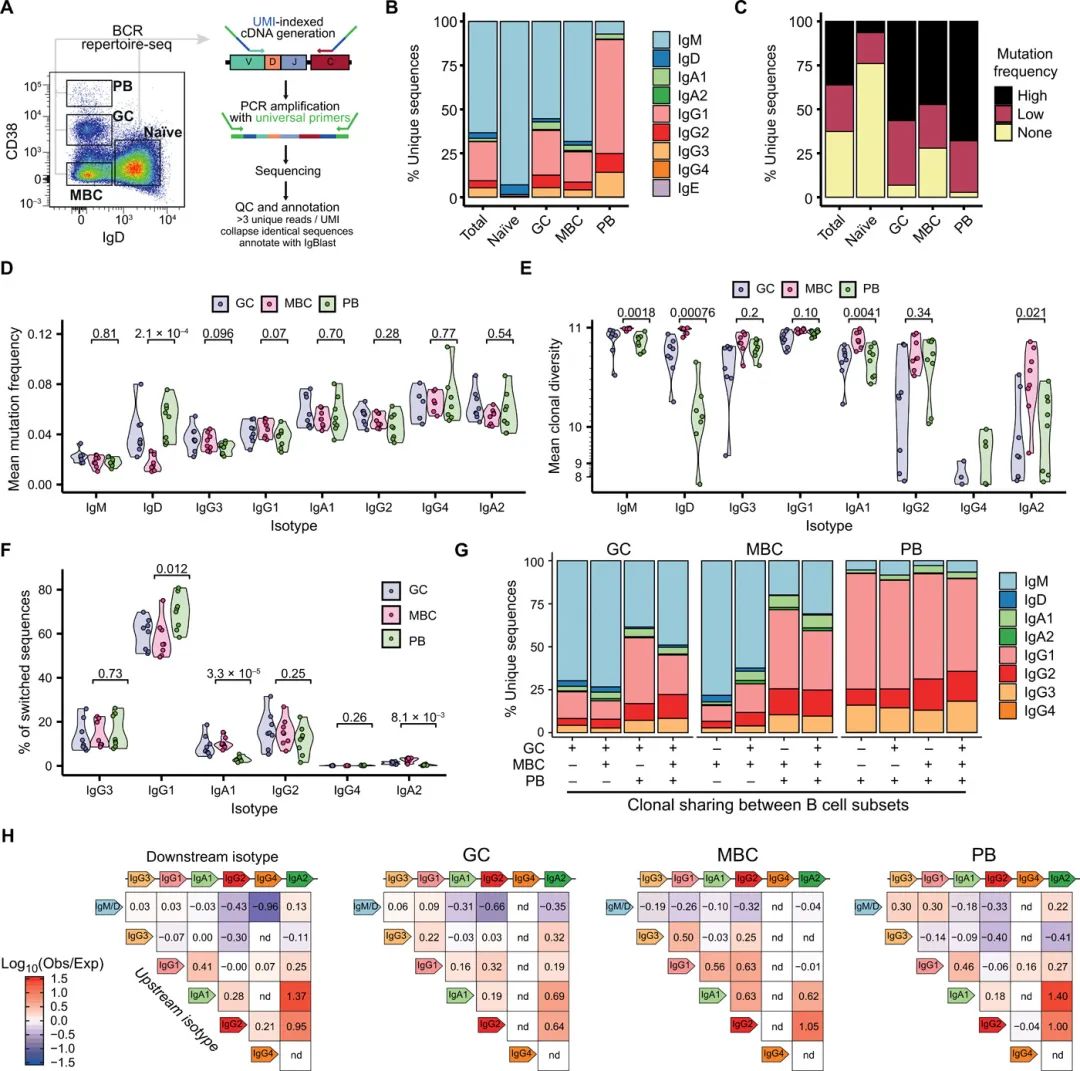
еЫЊ1 дЇЇз±їжЙБж°ГдљУBзїЖиГЮзЪДдЇЪз±їеТМдЇЪзЊ§зЙєеЉВжАІзЙєеЊБгАВ
02жЙБж°ГдљУеЕНзЦЂзїЖиГЮзЪДеНХзїЖиГЮеЫЊи∞±еЃЪдєЙдЇЖжИРзЖЯињЗз®ЛдЄ≠дЄНеРМзЪДBзїЖиГЮзКґжАБ
¬† ¬†¬† еЯЇдЇОFACSзЪДз≠ЦзХ•жЭ•з†Фз©ґдЇЇдљУзїДзїЗдЄ≠зЪДеК®жАБзїЖиГЮињЗз®ЛеПѓиГљдЉЪйФЩињЗзљХиІБжИЦжЬ™зЯ•зЪДзїЖиГЮзЊ§гАВеЫ†ж≠§пЉМдЄОе§ІйЗПжКЧдљУеЇУ(еЫЊ1)еє≥и°МпЉМдљЬиАЕеѓєжЭ•иЗ™зЫЄеРМж†ЈеУБзЪДжЬ™еИЖз±їжЙБж°ГдљУеЕНзЦЂзїЖиГЮињЫи°МдЇЖеНХзїЖиГЮRNAжµЛеЇП(scRNA-seq)еТМеНХзїЖиГЮеЕНзЦЂзРГиЫЛзЩљVDJжµЛеЇП(scVDJ-seq)йЕНеѓє(еЫЊ2AеТМB)гАВзїПињЗдЄ•ж†ЉзЪДиі®йЗПжОІеИґпЉМдљЬиАЕдњЭзХЩдЇЖ32,607дЄ™зїЖиГЮзЪДиљђељХзїД(n = 7;дЄ≠дљНжХ∞дЄЇ3142пЉМеє≥еЭЗжѓПдЄ™дЊЫиАЕ4658дЄ™зїЖиГЮ)пЉМдїОдЄ≠дљЬиАЕз°ЃеЃЪдЇЖ30дЄ™дЄНеРМзЪДзїЖиГЮзЊ§(еЫЊ2CеТМD)гАВиЩљзДґдљЬиАЕзЪДдЄїи¶БйЗНзВєжШѓдЇЖиІ£BзїЖиГЮзЪДжИРзЖЯпЉМдљЖдљЬиАЕж≥®йЗКдЇЖ11дЄ™TзїЖиГЮеТМ7дЄ™йЭЮжЈЛеЈізїЖиГЮзЊ§дљУ(еЫЊ2C)дљЬдЄЇз†Фз©ґињЩдЇЫзїЖиГЮзЪДеЃЭиіµиµДжЇРгАВ
¬† ¬† ¬†жЙБж°ГдљУжШѓдЄАзІНжЧҐиГљиѓ±еѓЉеЕ®иЇЂеЕНзЦЂеПИиГљиѓ±еѓЉз≤ШиЖЬеЕНзЦЂзЪДеЕЄеЮЛSLOгАВдљЬиАЕеПСзО∞дЄїи¶БзЪДжЙБж°ГдљУеЕНзЦЂзїЖиГЮзКґжАБеЬ®еЕґдїЦSLOs дЄ≠еєњж≥ЫдњЭеЃИпЉМе¶ВжЈЛеЈізїУеТМиДЊиДПпЉМдЄОеЕґдїЦеИЖжЮРз±їдЉЉпЉМе∞љзЃ°иІВеѓЯеИ∞еДњзЂ•жЙБж°ГдљУдЄ≠GCзЫЄеЕ≥зїЖиГЮзКґжАБзЪДеѓМйЫЖеПѓиГљеПНжШ†дЇЖдЊЫдљУеєійЊДзЪДеЈЃеЉВ(еЫЊ2BиЗ≥D)гАВдљЬиАЕињШиІВеѓЯеИ∞жКЧдљУзЙєеЊБзЪДеЈЃеЉВ(еЫЊ2EеТМF)пЉМињЩеПѓиГљеПНжШ†дЇЖе±АйГ®зїЖиГЮеЫ†е≠РзОѓеҐГзЪДзїДзїЗзЙєеЉВжАІеЈЃеЉВгАВдЄНеРМSLOs зїЖиГЮзКґжАБзЪДеєњж≥ЫдњЭеЃИжАІжФѓжМБе∞ЖжЙБж°ГдљУдљЬдЄЇз†Фз©ґеЕ®иЇЂеЕНзЦЂзЪДж®°еЮЛз≥їзїЯпЉМеєґеЉЇи∞ГдЇЖеИЖжЮРеЕНзЦЂжіїжАІзїДзїЗдї•зРЖиІ£GCдЊЭиµЦжАІBзїЖиГЮжИРзЖЯзЪДйЗНи¶БжАІгАВ
¬† ¬† ¬†жО•дЄЛжЭ•пЉМдљЬиАЕеЬ®еНХзїЖиГЮиљђељХзїДеЫЊи∞±дЄ≠ж£АжЯ•дЇЖBзїЖиГЮзКґжАБгАВдЄЇдЇЖжПРйЂШеНХзїЖиГЮжКЧдљУеЇУеИЖжЮРзЪДиГљеКЫеТМеЗЖз°ЃжАІпЉМжХіеРИдЇЖжѓПдЄ™дЊЫдљУзЪДеНХзїЖиГЮеТМжЙєйЗПжКЧдљУеЇУ(еЫЊ2E)гАВеЯЇдЇОеЯЇеЫ†и°®иЊЊзЪДжЧ†еБПиБЪз±ї(еЫЊF)пЉМдљЬиАЕйЙіеЃЪдЇЖ12дЄ™дЄНеРМзЪДBзїЖиГЮзЊ§пЉМеєґйЗПеМЦдЇЖеЃГдїђзЪДжКЧдљУеРМеЮЛйҐСзОЗ(еЫЊG)гАБSHMж∞іеє≥(еЫЊH)гАБеЕЛйЪЖе§Ъж†ЈжАІ(еЫЊ2IеТМJ)пЉМдї•еПКдЄОеЕґдїЦBзїЖиГЮдЇЪзЊ§зЪДеЕ≥з≥ї(еЫЊKеТМеЫЊL)гАВжЙАжЬЙдЇЇзЊ§еЬ®жВ£иАЕдЄ≠еЭЗеПѓйЗНе§НиІВеѓЯпЉМиАМдЄНиАГиЩСжЙБж°ГдљУзВОзЧЕеП≤(еЫЊM)гАВдљЬиАЕз°ЃеЃЪдЇЖдЇЇз±їжЙБж°ГдљУдЄ≠BзїЖиГЮжИРзЖЯзЪДжЙАжЬЙдЄїи¶БйШґжЃµпЉМеМЕжЛђna√ѓveгАБжіїеМЦгАБGC(еМЕжЛђLZеТМйЭЮеҐЮжЃЦDZзїЖиГЮ)гАБMBCsгАБзїДзїЗеЖЕFcеПЧдљУ4 (FCRL4+) MBCsгАБPBsеТМдЄїи¶БзФ±DZ GCзїЖиГЮзїДжИРзЪДеЊ™зОѓзЊ§дљУ(еЫЊ2H)гАВдљЬиАЕињШж≥®йЗКдЇЖдЄАдЄ™з±їеИЂеИЗжНҐгАБиґЕз™БеПШеТМеЕЛйЪЖжЙ©еҐЮзЪДGC BзїЖиГЮдЇЪзЊ§пЉМи°®иЊЊPBзЙєеЉВжАІиљђељХеЫ†е≠Р(PRDM1еТМXBP1)(еЫЊ2FиЗ≥J)гАВдљЬиАЕеПСзО∞pre-PB GCзїЖиГЮйАЙжЛ©жАІеЬ∞и°®иЊЊдЇЖеЗ†дЄ™жЬЙиґ£зЪДеЯЇеЫ†ж†ЗиЃ∞пЉМеМЕжЛђдњ°еПЈеИЖе≠РпЉМжП≠з§ЇдЇЖ嚥жИРдЇЇз±їBзїЖиГЮдїЛеѓЉеЕНзЦЂзЪДеК®жАБзїЖиГЮзКґжАБпЉМе¶ВFRZBеТМBTNL9(еЫЊ2F)гАВ
¬† ¬† дљЬиАЕеЬ®GCдЄ≠еПСзО∞дЇЖиљђељХдЄНеРМдЄФеЕЛйЪЖжЙ©еҐЮзЪДIgM+ BзїЖиГЮзЊ§пЉМеЕґдЄОжКСеИґжАІBCRдњ°еПЈзЫЄеЕ≥зЪДеЯЇеЫ†и°®иЊЊеНЗйЂШпЉМе¶ВFCRL3пЉМ FCRL2пЉМ SAMSN1еТМSIGLEC10(еЫЊDеТМFиЗ≥J)пЉМ襀зІ∞дєЛдЄЇFCRL3highGC BзїЖиГЮгАВ
¬† ¬† ¬†еЫ†дЄЇињЩзЊ§жЬ™иљђжНҐзїЖиГЮжШѓзФ±йЭЮеЄЄйЂШFCRL2еТМFCRL3и°®иЊЊеЉП(еЫЊ2F),дљЬиАЕж£АжЯ•дЇЖињЩдЇЫж†ЗиЃ∞жµБеЉПзїЖиГЮжЬѓзЪДжЙБж°ГдљУBзїЖиГЮеТМи°®йЭҐи°®иЊЊдЄОFCRL3еПСзО∞дЄАдЄ™жЬЙеЊИеЉЇеЕ≥иБФпЉМдљЖдЄНжШѓFCRL2еТМIgMи°®иЊЊGCеТМMBCдЇЇеП£(еЫЊS8, F)гАВиЩљзДґињЩдЇЫзїЖиГЮзЪДз≤Њз°ЃжЬђдљУе∞ЪдЄНжЄЕж•Ъ,еЯЇдЇОscVDJеИЖжЮРеПСзО∞пЉМFCRL3highGC BзїЖиГЮжШѓйЂШеЇ¶жЙ©еҐЮзЪДGCи°НзФЯеЕЛйЪЖзЪДдЄАйГ®еИЖпЉМиѓ•еЕЛйЪЖеРЂжЬЙMBCsеТМPBs(еЫЊ2KеТМL)гАВи°®жШОеЃГдїђжШѓйАЪињЗдЇІж∞ФзЫЄиЙ≤и∞±еПНеЇФдЇІзФЯзЪДпЉМдЄН姙еПѓиГљжЭ•иЗ™еНХзЛђзЪДжИЦеЫЇеЃЪзЪДи∞±з≥їгАВ
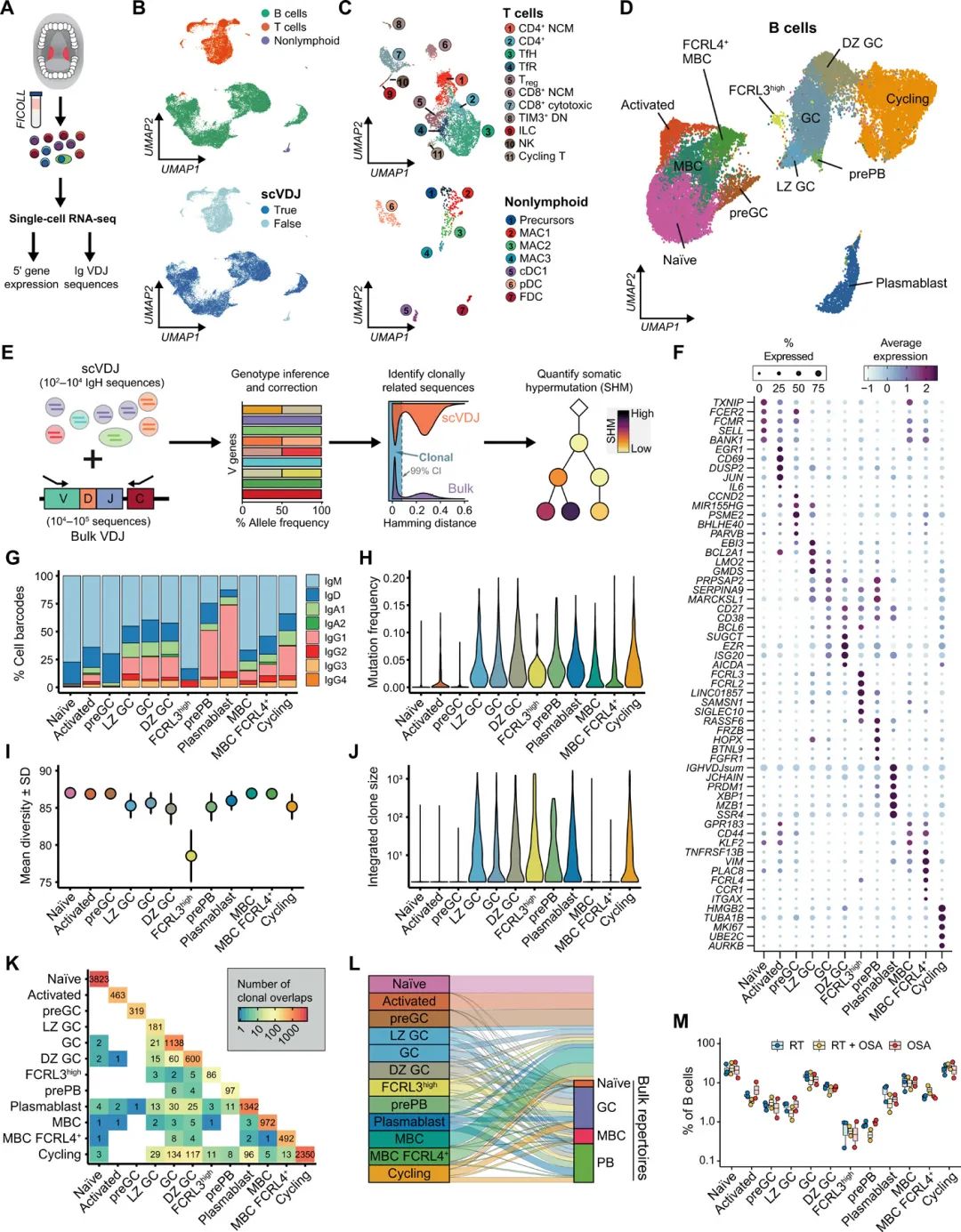
еЫЊ2 дЇЇз±їжЙБж°ГдљУеЕНзЦЂзїЖиГЮеНХзїЖиГЮеЫЊи∞±дї•дЇЖиІ£BзїЖиГЮжИРзЖЯгАВ
03дЇЇBзїЖиГЮжіїеМЦеТМGC嚥жИРзЪДжЛЯжЧґйЗНеїЇ
¬† ¬† ¬† еЬ®жіїеМЦињЗз®ЛдЄ≠пЉМBзїЖиГЮиОЈеЊЧжКЧеОЯпЉМи¶БдєИдї•еПѓжЇґжАІељҐеЉПе≠ШеЬ®пЉМи¶БдєИжШЊз§ЇеЬ®жї§ж≥°жКЧеОЯеСИйАТзїЖиГЮ(APCs)и°®йЭҐпЉМеЕБиЃЄеЃГдїђињБзІїеИ∞TзїЖиГЮеМЇпЉМеЬ®йВ£йЗМеЃГдїђеПѓдї•еПВдЄОGCеПНеЇФгАВдљЬиАЕжО®жЦ≠пЉМBзїЖиГЮжИРзЖЯеНХзїЖиГЮеЫЊи∞±е∞ЖеМЕеРЂеЃМжХізЪДжњАжіїзКґжАБпЉМеєґеЕБиЃЄйЗНеїЇBзїЖиГЮжњАжіїеТМGCеПНеЇФ嚥жИРињЗз®ЛдЄ≠зЪДжЧґйЧіеЯЇеЫ†и°®иЊЊеТМжКЧдљУеЇУеК®жАБгАВscRNA-seqеИЖжЮРз°ЃеЃЪдЇЖдЄАдЄ™BзїЖиГЮз∞ЗпЉМзФ±жЧ†жКЧеОЯna√ѓve BзїЖиГЮеТМжКЧеОЯзїПеОЖзЪДMBCs(еЫЊS10)зїДжИРпЉМеЃГдїђеЕЈжЬЙжњАжіїж†ЗиЃ∞еЯЇеЫ†зЪДи°®иЊЊеНЗйЂШ(еЫЊ3A)еТМйҐДжµЛзЪДдЄОAPCsзЪДзїЖиГЮ-зїЖиГЮзЫЄдЇТдљЬзФ®зЪДйЂШйҐСзОЗ(еЫЊ3B)гАВ
¬† ињЩзІНжіїеМЦзЪДBзїЖиГЮзКґжАБдЉЉдєОиГље§ЯеИЖеИЂйАЪињЗзїЖиГЮйЧіз≤ШйЩДеИЖе≠Р-1-ITGAL(жХіеРИзі†дЇЪеНХдљНќ± L) (LFA-1)еТМ/жИЦзЩљзїЖиГЮдїЛзі†-6 (IL6)дЄОAPCsеТМTзїЖиГЮињЫи°МйАЪдњ°(еЫЊ3C)гАВиЃЄе§ЪињЩдЇЫйҐДжµЛзЪДзїЖиГЮ-зїЖиГЮзЫЄдЇТдљЬзФ®дєЯеЬ®GCеЙНеТМLZ GC BзїЖиГЮзКґжАБдЄ≠襀ж£АжµЛеИ∞(еЫЊ3C)пЉМзДґеРОеЬ®еЕґдїЦGC BзїЖиГЮзЊ§дЄ≠䪥姱пЉМињЩи°®жШОGCеЙНBзїЖиГЮеПѓиГљдљЬдЄЇеИЭеІЛBзїЖиГЮжњАжіїеТМGC嚥жИРдєЛйЧізЪДињЗжЄ°зКґжАБе≠ШеЬ®гАВ
¬† ¬†¬† дЄЇдЇЖжЫіе•љеЬ∞дЇЖиІ£дЄНеРМBзїЖиГЮзЊ§зЪДиљђељХеК®еКЫе≠¶пЉМзЙєеИЂжШѓpre-GC BзїЖиГЮзКґжАБпЉМдљЬиАЕињЫи°МдЇЖRNA йАЯзОЗеИЖжЮРжЭ•ж®°жЛЯеНХдЄ™BзїЖиГЮзЪДиљђељХеК®еКЫе≠¶пЉМеєґжО®жЦ≠еЃГдїђзЪДжЦєеРСжАІдї•еПКдЄОеЕґдїЦBзїЖиГЮзЊ§зЪДеЕ≥з≥їгАВињЩиѓБеЃЮдЇЖGCеЙНзїЖиГЮеѓєLZ GCзКґжАБи°®зО∞еЗЇеЊИеЉЇзЪДжЦєеРСжАІ(еЫЊ3D)гАВеЯЇдЇОйАЯеЇ¶зЪДna√ѓveгАБжіїеМЦгАБpre-GCеТМLZ GC BзїЖиГЮзЪДжЛЯжЧґжОТеЇПе∞ЖйҐДGCзїЖиГЮзљЃдЇОжіїеМЦеТМLZ GC BзїЖиГЮдєЛйЧіпЉМеєґжП≠з§ЇдЇЖдїОжЧ©жЬЯжіїеМЦдЇЛдїґеИ∞зЬЯж≠£зЪДGC BзїЖиГЮзЪДеЯЇеЫ†и°®иЊЊзЪДеЃМжХіињЮзї≠дљУ(еЫЊ3EеТМF)гАВињЩеМЕжЛђеЕ≥йФЃдњ°еПЈеИЖе≠РеТМиљђељХеЫ†е≠Ре¶ВCD40гАБEBI3гАБMIFгАБBATFгАБBHLHE40еТМMYCзЪДеК®жАБи°®иЊЊ(еЫЊ3EеТМF)гАВиЗ≥еЕ≥йЗНи¶БзЪДжШѓпЉМдљЬиАЕеПСзО∞жњАжіїзЪДBзїЖиГЮз∞З(еМЕжЛђжњАжіїзЪДna√ѓveеТМMBCдЇЪзЊ§)(еЫЊS10)дљНдЇОиљ®ињєзЪДжЧ©жЬЯпЉМеєґдЄФеѓМйЫЖдЇЖдЄОжА•жАІ(1е∞ПжЧґ)BзїЖиГЮеИЇжњАзЫЄеЕ≥зЪДеЃЮй™Ми°НзФЯеЯЇеЫ†зЙєеЊБпЉМиАМpre-GC BзїЖиГЮжЫіжО•ињСдЇОдЄ≠зЇІж∞іеє≥зЪДBзїЖиГЮеИЇжњА(3иЗ≥6е∞ПжЧґ)(еЫЊ3G)гАВињЩиѓБеЃЮдЇЖињЩдЇЫBзїЖиГЮеЬ®йБЗеИ∞жКЧеОЯеРОеТМGCs嚥жИРдєЛеЙНи°®зО∞еЗЇдЇМзЇІжњАжіїзКґжАБгАВеЫ†ж≠§пЉМеѓєBзїЖиГЮжіїеМЦзЪДйЗНеїЇдЄЇз†Фз©ґињЩдЇЫеК®жАБBзїЖиГЮеЬ®дљУеЖЕзЪДзКґжАБжПРдЊЫдЇЖдЄАдЄ™жЬЙдїЈеАЉзЪДж°ЖжЮґгАВ
¬† ¬† ¬†дљЬиАЕеѓєдЇЇдљУеЖЕBзїЖиГЮжњАжіїзЪДйЗНеїЇжШЊз§ЇпЉМеЬ®pre-GC BзїЖиГЮдЄ≠пЉМдЄОCSRзЫЄеЕ≥зЪДеЯЇеЫ†жДПе§ЦеѓМйЫЖ(еЫЊ3HиЗ≥J)пЉМдЄОеЄЄиІДCSRдљНзВєзЪДLZ GC BзїЖиГЮзЫЄжѓФпЉМеЕґеѓМйЫЖз®ЛеЇ¶зЫЄдЉЉжИЦжЫійЂШгАВиЩљзДґAICDAзЪДи°®иЊЊж∞іеє≥еЊИдљО(еЫЊ2H)пЉМдљЖдљЬиАЕеѓєpre-GCеТМLZ GCињЗжЄ°зЪДеИЖжЮРжШЊз§ЇпЉМеЕґдїЦеЯЇеЫ†дЄОCSRжЬЙжЬЇеИґиБФз≥їпЉМеМЕжЛђйВ£дЇЫиГље§ЯзїУеРИIgHдљНзВєеЖЕзЪДеЉАеЕ≥еМЇеЇПеИЧгАБдЄОCSRжЬЇеИґзЫЄдЇТдљЬзФ®жИЦи∞ГиКВAICDA/AICDAз®≥еЃЪжАІзЪДеЯЇеЫ†(еЫЊ3K)гАВиЩљзДґдљЬиАЕиІВеѓЯеИ∞еЊИе∞СжЬЙеИЗжНҐзЪДpre-GC BзїЖиГЮ(еЫЊ2)гАВеЯЇдЇОеѓєйЂШзљЃдњ°еЇ¶scVDJеЇПеИЧзЪДеИЖжЮРпЉМдљЬиАЕеПСзО∞pre-GCзїЖиГЮдЄ≠IgHзІНз≥їиљђељХжЬђ(GLTs)зЪДи°®иЊЊеЬ®IgHдљНзВєиЊЊеИ∞е≥∞еАЉ(еЫЊM)гАВ
¬† ¬† ¬† е∞љзЃ°ињЩеЬ®еНХзїЖиГЮдЄ≠дЉЉдєОж∞іеє≥ињЗдљОпЉМжЧ†ж≥ХйЗНеїЇйЂШиі®йЗПзЪДscVDJ йЗНеП†зЊ§гАВињЩдЇЫеЬ®дЇЇз±їжЙБж°ГдљУдЄ≠зЪДиІВеѓЯзїУжЮЬдЄОе∞ПйЉ†ж®°еЮЛдЄ≠GLTиљђељХе≥∞еАЉеТМCSRеПСзФЯеЬ®GC嚥жИРдєЛеЙНдЄАиЗігАВињЩи°®жШОпЉМеЬ®GCеПНеЇФ嚥жИРдєЛеЙНпЉМpre-GCзЪДBзїЖиГЮзКґжАБеПѓиГљеЈ≤зїПеЗЖе§Зе•љињЫи°МCSRпЉМе∞љзЃ°иІВеѓЯзїУжЮЬеєґдЄНжОТйЩ§GCеЖЕдєЯдЉЪеПСзФЯCSRгАВ
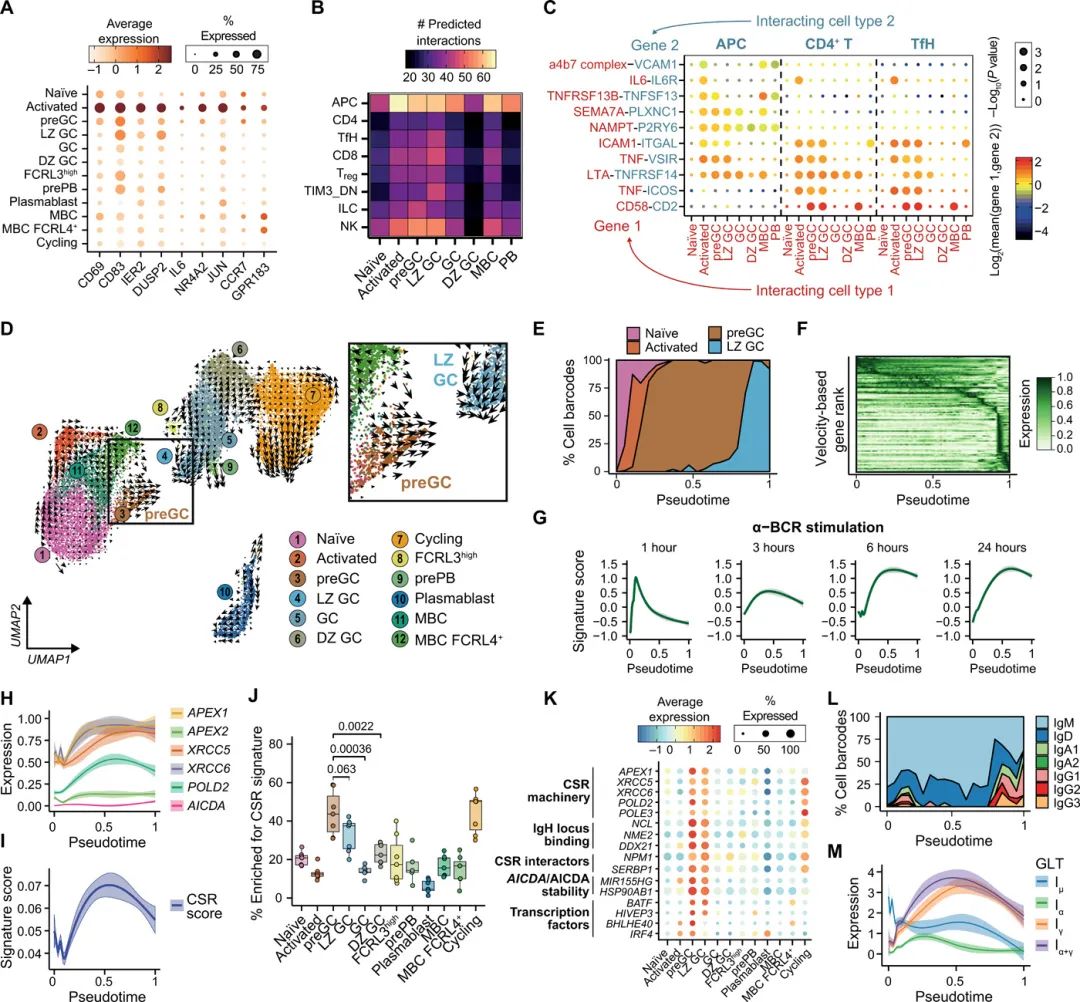
еЫЊ3.дЇЇBзїЖиГЮжіїеМЦеТМGCињЫеЕ•зЪДеИґеЫЊеК®еКЫе≠¶гАВ
04жЙБж°ГдљУеЕНзЦЂзїЖиГЮзЪДеНХзїЖиГЮеЫЊи∞±еЃЪдєЙдЇЖжИРзЖЯињЗз®ЛдЄ≠дЄНеРМзЪДBзїЖиГЮзКґжАБ
¬† ¬† ¬† дљЬиАЕдљњзФ®йЕНеѓєзЪДеНХзїЖиГЮиљђељХзїДеТМжКЧдљУеЇУжЭ•еЙЦжЮРGCеПНеЇФдЄ≠дЄОеЯЇдЇОжКЧдљУзЪДйАЙжЛ©зЫЄеЕ≥зЪДеЯЇеЫ†и°®иЊЊгАВ
¬† ¬† ¬† е∞љзЃ°GC BзїЖиГЮеЬ®зЙ©зРЖдЄКдЄНеРМзЪДLZsеТМDZsдєЛйЧіеЊ™зОѓпЉМдљЖдљЬиАЕеПСзО∞иЃЄе§ЪGC BзїЖиГЮеЬ®ињЩдЄ§зІНзКґжАБдєЛйЧіињЮзї≠е≠ШеЬ®(еЫЊ4AеТМB)пЉМињЩдЄОеЕИеЙНзЪДз†Фз©ґзЫЄдЉЉпЉМйЩ§дЇЖFCRL3highеТМpre-PBзїЖиГЮеЬ®иљђељХдЄКдЄНеРМ(еЫЊ2FеТМ4C)гАВињЩдЇЫGC BзїЖиГЮдЇЪзЊ§дєЯи°®зО∞еЗЇдЄНеРМзЪДз±їеИЗжНҐж®°еЉПпЉМpre-PBзїЖиГЮжЫійҐСзєБеЬ∞и°®иЊЊз±їеИЗжНҐеРМзІНеЮЛпЉМFCRL3highGCзїЖиГЮдњЭзХЩIgM/IgDзЪДи°®иЊЊ(еЫЊ2GгАБ4D)гАВеРЂжЬЙFCRL3highGCзїЖиГЮзЪДжЙ©еҐЮBзїЖиГЮеЕЛйЪЖеЗ†дєОеЃМеЕ®жШѓIgM+(еЫЊ4E)пЉМињЩи°®жШОжКЧдљУз±їеИЂеПѓиГљдЄОзЙєеЃЪзЪДеЯЇеЫ†и°®иЊЊз®ЛеЇПеТМзїЖиГЮеСљињРжЬЙеЕ≥пЉМеПНдєЛдЇ¶зДґгАВ
¬† ¬† ¬† жО•дЄЛжЭ•пЉМдљЬиАЕеИ©зФ®йЕНеѓєзЪДеНХзїЖиГЮVDJеТМиљђељХзїДе≠¶жХ∞жНЃйЫЖпЉМж†єжНЃжКЧдљУSHMйҐСзОЗдљЬдЄЇдЇ≤еТМеКЫзЪДдї£зРЖпЉМеѓєжЙАжЬЙйЭЮеЊ™зОѓGC BзїЖиГЮ(дЄНеМЕжЛђpre-PBеТМFCRL3highзЊ§дљУ)ињЫи°МеИЖе±В(еЫЊ4F)гАВйЂШSHMзЪДGC BзїЖиГЮжШЊиСЧеѓМйЫЖдЇЖйЂШдЇ≤еТМеКЫжКЧеОЯзїУеРИBзїЖиГЮзЪДеЯЇеЫ†зЙєеЊБпЉМBзїЖиГЮжИРзЖЯж†ЗењЧзЙ©CD27зЪДи°®иЊЊжЫійЂШпЉМеЕЛйЪЖе§Іе∞ПжЫіе§І(еЫЊ4F)пЉМеПНжШ†дЇЖеЯЇдЇОBCRдЇ≤еТМеКЫзЪДжЙ©еҐЮеТМжИРзЖЯгАВж£АжµЛеИ∞еЊИе∞СзЪДBзїЖиГЮи°®иЊЊжЧ†еКЯиГљзЪДIgHеЇПеИЧ(еЫЊ4F)пЉМеЗЛдЇ°зїЖиГЮжЧ†ж≥ХдЇІзФЯиґ≥е§ЯйЂШиі®йЗПзЪДиљђељХзїДжХ∞жНЃпЉМжИЦиАЕзФ±дЇОзЇњз≤ТдљУеРЂйЗПеНЗйЂШиАМ襀粿йЩ§гАВйЂШжИЦдљОSHMзЪДGC BзїЖиГЮеЬ®еЯЇеЫ†и°®иЊЊдЄКе≠ШеЬ®иЃЄе§ЪеЈЃеЉВ(еЫЊ4G)пЉМињЩдЄОйЂШдЇ≤еТМеКЫеТМдљОдЇ≤еТМеКЫзїУеРИдЇЛдїґеѓєGC BзїЖиГЮзЪДеЈЃеЉВи∞ГиКВжШѓдЄАиЗізЪДгАВзДґиАМпЉМињЩдЇЫSHMеЯЇеЫ†зЙєеЊБдЄОиљђжНҐжИЦжЬ™иљђжНҐзЪДGC BзїЖиГЮзЪДеЯЇеЫ†зЙєеЊБйЭЮеЄЄзЫЄдЉЉ(еЫЊ4G)пЉМж≠£е¶ВеЬ®IgM+ GC BзїЖиГЮзЪДеє≥еЭЗSHMйҐСзОЗиЊГдљОжЧґжЙАйҐДжµЛзЪДйВ£ж†ЈпЉИеЫЊ1D)гАВ
¬† ¬† ¬† дЄЇдЇЖеЕЛжЬНжИРзЖЯзКґжАБеѓєж£АжµЛеРМеЮЛзЙєеЉВжАІеЯЇеЫ†и°®иЊЊзЪДжЈЈжЭВељ±еУНпЉМдљЬиАЕе∞ЖGC BзїЖиГЮдЄОи°®иЊЊдЄНеРМжКЧдљУз±їеИЂзЪДеМєйЕНSHMж∞іеє≥ињЫи°МдЇЖжѓФиЊГгАВињЩи°®жШОпЉМеИЗжНҐеРОзЪДGC BзїЖиГЮеѓМеРЂзїЖиГЮе≠ШжіїгАБBCRдњ°еПЈдЉ†еѓЉгАБжКЧеОЯеСИйАТгАБеЕНзЦЂеЇФз≠ФеТМдї£и∞Ґдї•еПКеЕґдїЦйЗНи¶Бдњ°еПЈйАЪиЈѓжЙАйЬАзЪДеЯЇеЫ†(еЫЊ4HеТМI)гАВеИЗжНҐзЪДGC BзїЖиГЮдєЯжЬЙиѓБжНЃи°®жШОпЉМеѓєTзїЖиГЮи°НзФЯзЪДзїЖиГЮеЫ†е≠Р(е¶ВIL4гАБиљђеМЦзФЯйХњеЫ†е≠Р-ќ≤гАБеє≤жЙ∞зі†-ќ≥(IFN-ќ≥)еТМCD40LG)жИЦйАЪињЗдЄНеРМзЪДTOLLж†ЈеПЧдљУ(еЫЊ4H)еПСеЗЇзЪДеПНеЇФдњ°еПЈеҐЮеК†пЉМињЩдЄОеЃГдїђжО•еПЧжЫіе§ЪзЪДTзїЖиГЮеЄЃеК©жШѓдЄАиЗізЪДгАВ
¬† ¬† ¬† еЬ®IgG+еТМIgA+ GC BзїЖиГЮдЄ≠пЉМеПВдЄОGCзЇ¶жЭЯжИЦBзїЖиГЮзФЯжАБдљНељТеЈҐзЪДеЗ†дЄ™еЯЇеۆ襀дЄКи∞ГпЉМдЊЛе¶ВCXCL12дїЛеѓЉзЪДеРСGCињБзІїжЙАйЬАзЪДеЯЇеЫ†(LCP1еТМMYO1E)еТМGCзЇ¶жЭЯеПЧдљУP2RY8пЉМињЩи°®жШО襀蚐жНҐзЪДBзїЖиГЮеПѓиГљжЫіжЬЙеПѓиГљеЬ®GCдЄ≠еБЬзХЩжЫійХњжЧґйЧігАВињЩеПѓдї•иІ£йЗКдїЦдїђжЫійЂШзЪДSHMзОЗгАВе§Іе§ЪжХ∞еЯЇеЫ†и°®иЊЊеЈЃеЉВеЬ®IgG+еТМIgA+ BзїЖиГЮдєЛйЧіеЕЈжЬЙеПѓжѓФжАІ(еЫЊ4I)жЬАеРОпЉМдљЬиАЕиІВеѓЯеИ∞з±їзЙєеЉВжАІGC BзїЖиГЮдєЛйЧіиљђељХеЫ†е≠РзЪДи°®иЊЊе≠ШеЬ®иЃЄе§ЪеЈЃеЉВ(еЫЊ4I)гАВIgG+ BзїЖиГЮи°®иЊЊжЫійЂШж∞іеє≥зЪДBCL6гАБXBP1еТМID3пЉМињЩеПѓиГљеҐЮеК†дЇЖеЃГдїђй©їзХЩеЬ®GCжИЦеРСжµЖзїЖиГЮеИЖеМЦзЪДиГљеКЫпЉМиАМIgM+зїЖиГЮи°®иЊЊжЫійЂШж∞іеє≥зЪДBACH2пЉМжКСеИґжµЖзїЖиГЮеИЖеМЦгАВињШеПСзО∞дЇЖеЕґдїЦеЫ†е≠Р(LMO2гАБTOXгАБBCL11AеТМCUX1)зЪДеЈЃеЉВи°®иЊЊпЉМжПРеЗЇдЇЖеЃГдїђеЬ®GCеЖЕеЉАеЕ≥еТМжЬ™еЉАеЕ≥BзїЖиГЮзЪДиљђељХињЮжО•дЄ≠зЪДдљЬзФ®зЪДйЧЃйҐШгАВ
¬† ¬† ¬† еѓєGCеПНеЇФзЪДеНХзїЖиГЮеИЖиЊ®зОЗдљњдљЬиАЕиГље§ЯиІ£еБґиБФжКЧдљУдЇ≤еТМеКЫеТМз±їеИЂпЉМеєґиІ£еЙЦBзїЖиГЮеЇУдЄ≠ињЩдЄ§дЄ™еЕ≥йФЃиЗВеЬ®е°СйА†BзїЖиГЮеСљињРеТМеКЯиГљжЦєйЭҐзЪДеЈЃеЉВиі°зМЃгАВињЩдЇЫеИЖжЮРи°®жШОпЉМеИЗжНҐеТМжЬ™еИЗжНҐзЪДBзїЖиГЮеЬ®GCдЄ≠зФЯе≠ШеТМй©їзХЩзЪДиГљеКЫдЄНеРМпЉМеєґз°ЃеЃЪйЩ§дЇЖBCRдЇ≤еТМеКЫе§ЦпЉМGCдЄ≠еЯЇдЇОжКЧдљУзЪДйАЙжЛ©еПѓдї•зФ±BзїЖиГЮжШѓеР¶зїПеОЖињЗCSRжЭ•еЖ≥еЃЪгАВ

еЫЊ4 еЬ®еНХзїЖиГЮеИЖиЊ®зОЗдЄЛиІ£еЖ≥GC BзїЖиГЮдЄ≠жКЧдљУз±їдЊЭиµЦеЯЇеЫ†и°®иЊЊгАВ
05дЇЇз±їжЙБж°ГдљУдЄ≠е§Ъж†ЈзЪДMBCзКґжАБ
¬† ¬† ¬†жИРзЖЯзКґжАБеТМжКЧдљУз±їеИЂдЄОGC BзїЖиГЮзЪДзЙєеЃЪеЯЇеЫ†и°®иЊЊжЬЙеЕ≥пЉМеПѓиГљжШѓйАЪињЗдљЬдЄЇBCRдЄАйГ®еИЖзЪДеЕНзЦЂзРГиЫЛзЩљзЪДиЖЬзЙєеЉВжАІеРМзІНеЉВжЮДдљУгАВдЄОPBsзЫЄеПНпЉМMBCдњЭзХЩBCRи°®иЊЊпЉМеЕґеРМеЮЛеПѓиГљељ±еУНдЄНеРМMBCдЇЪзЊ§зЪДи°®еЮЛзЙєжАІпЉМеЕґеЃМеЕ®е§Ъж†ЈжАІе∞ЪдЄНжЄЕж•ЪгАВеЫ†ж≠§пЉМдљЬиАЕиѓХеЫЊжЫіе•љеЬ∞еЃЪдєЙдЇЇз±їжЙБж°ГдљУдЄ≠MBCеЇУзЪДеЉВиі®жАІпЉМеєґз°ЃеЃЪMBCsзЪДжКЧдљУз±їи°®иЊЊжШѓеР¶еПѓиГљдЄОдЄНеРМзЪДеКЯиГљжИЦдЇЪзЊ§жЬЙеЕ≥гАВ
¬† ¬† ¬†еДњзЂ•жЙБж°ГдљУдЄ≠зЫЄељУе§ІжѓФдЊЛзЪДMBCsжܙ襀蚐жНҐ(еЫЊ1BеТМ2G)гАВдЄЇдЇЖз†Фз©ґиЈ®з±їеИЂеИЗжНҐMBCдЇЪзЊ§зЪДжљЬеЬ®еЈЃеЉВеЯЇеЫ†и°®иЊЊпЉМдЄЇжЙАжЬЙ(n = 2)жИЦIgM犯姱(n = 4) MBCзФЯжИРдЇЖжИРеѓєзЪДеНХзїЖиГЮиљђељХзїДе≠¶еТМVDJи∞±(и°®S1)гАВжХ∞жНЃйЫЖжХіеРИеТМиі®йЗПжОІеИґжПРдЊЫдЇЖ21,595дЄ™йЂШиі®йЗПзЪДMBCеНХзїЖиГЮиљђељХзїДпЉМдљЬиАЕзФ®еПНжШ†дЄНеРМMBCдЇЪзЊ§еТМзКґжАБзЪД11дЄ™з∞ЗињЫи°МдЇЖж≥®йЗК(еЫЊ5AиЗ≥C)гАВйЩ§дЇЖеЕИеЙНйЙіеЃЪзЪДзїДзїЗеЖЕFCRL4+ MBC(еЫЊ2)пЉМдљЬиАЕињШж≥®йЗКдЇЖдЄ§дЄ™зљХиІБзЪДCR2/CD21low MBCдЇЪзЊ§пЉМеЃГдїђдЉЉдєОз±їдЉЉдЇОдЄНеРМзїДзїЗеТМзЦЊзЧЕзКґжАБдЄЛжППињ∞зЪДйЭЮеЕЄеЮЛMBCзЊ§дљУ(еЫЊ5AиЗ≥C)гАВеЕґдЄ≠дЄАдЄ™з∞З(CD21low 2)дЄОйЭЮеЕЄеЮЛFCRL5highзЪДMBCsеЕ±жЬЙеЗ†дЄ™зЙєеЊБпЉМе¶ВжКСеИґеПЧдљУ(CD22)еТМеПВдЄОжКЧеОЯеСИйАТзЪДеЯЇеЫ†(CIITA)зЪДйЂШи°®иЊЊ(еЫЊ5C)гАВеР¶еИЩпЉМдЇЇз±їжЙБж°ГдљУдЄ≠зЪДе§Іе§ЪжХ∞MBCе§Ъж†ЈжАІеПНжШ†зЪДжШѓзїЖиГЮзКґжАБжИЦжіїжАІзЪДеЈЃеЉВпЉМиАМдЄНжШѓдЄНеРМзЪДзїЖиГЮз±їеЮЛпЉМе¶ВзГ≠дЉСеЕЛиЫЛзЩљзЫЄеЕ≥еТМIFNзЫЄеЕ≥зЪДеЯЇеЫ†жіїжАІ(еЫЊ5AиЗ≥C)гАВињШеПСзО∞дЇЖе§ЪзІНжњАжіїзКґжАБ(Activated1/2)пЉМеМЕжЛђдЄОna√ѓve pre-GCзїЖиГЮзЫЄдЉЉзЪДеЯЇеЫ†и°®иЊЊеТМCSRеЯЇеЫ†еѓМйЫЖзЪДMBCs(еЫЊ5C)пЉМдљЬиАЕе∞ЖеЕґж†ЗиЃ∞дЄЇpre-GC MBCsгАВдљЬиАЕињШеПСзО∞пЉМдЄОFCRL3highGCзЊ§дљУзЫЄдЉЉзЪДFCRL3highMBCзКґжАБ(еЫЊ5C)еТМз±їдЉЉзЪДMBCзЊ§дљУдєЯеПѓдї•еЬ®жЈЛеЈізїУеТМиДЊиДПдЄ≠ж£АжµЛеИ∞пЉМе∞љзЃ°йҐСзОЗдЄНеРМ(еЫЊS15F)гАВињЩи°®жШОињЩдЇЫж≥®йЗКзЪДMBCзЊ§дљУеПѓиГљеєњж≥ЫеЕ±дЇЂиЈ®иґКе§ЪзІНBзїЖиГЮеСљињРеТМеЩ®еЃШз≥їзїЯзЪДеКЯиГљзКґжАБгАВ
¬† ¬†¬† жО•дЄЛжЭ•пЉМдљЬиАЕз†Фз©ґдЇЖеИЗжНҐз±їеИЂеТМжЬ™еИЗжНҐз±їеИЂзЪДMBCsжШѓеР¶и°®зО∞еЗЇдЄНеРМзЪДеЯЇеЫ†и°®иЊЊзљСзїЬпЉМињЩеПѓиГљеПНжШ†дЇЖзЙєжЃКзЪДеКЯиГљиГљеКЫгАВдљЬиАЕеПСзО∞еЊИе∞СжЬЙиѓБжНЃи°®жШОжКЧдљУз±їеИЂеѓєMBCеЬ®зїЩеЃЪзКґжАБдЄЛе≠ШеЬ®зЪДеПѓиГљжАІжЬЙиі°зМЃпЉМйЩ§дЇЖFCRL3highзЪДMBCпЉМдЄОFCRL3highзЪДGCзїЖиГЮзЫЄдЉЉпЉМscVDJеТМжµБеЉПзїЖиГЮжЬѓеИЖжЮРжШЊз§ЇеЕґдЄїи¶БжШѓIgM+(еЫЊ5AеТМB)гАВ
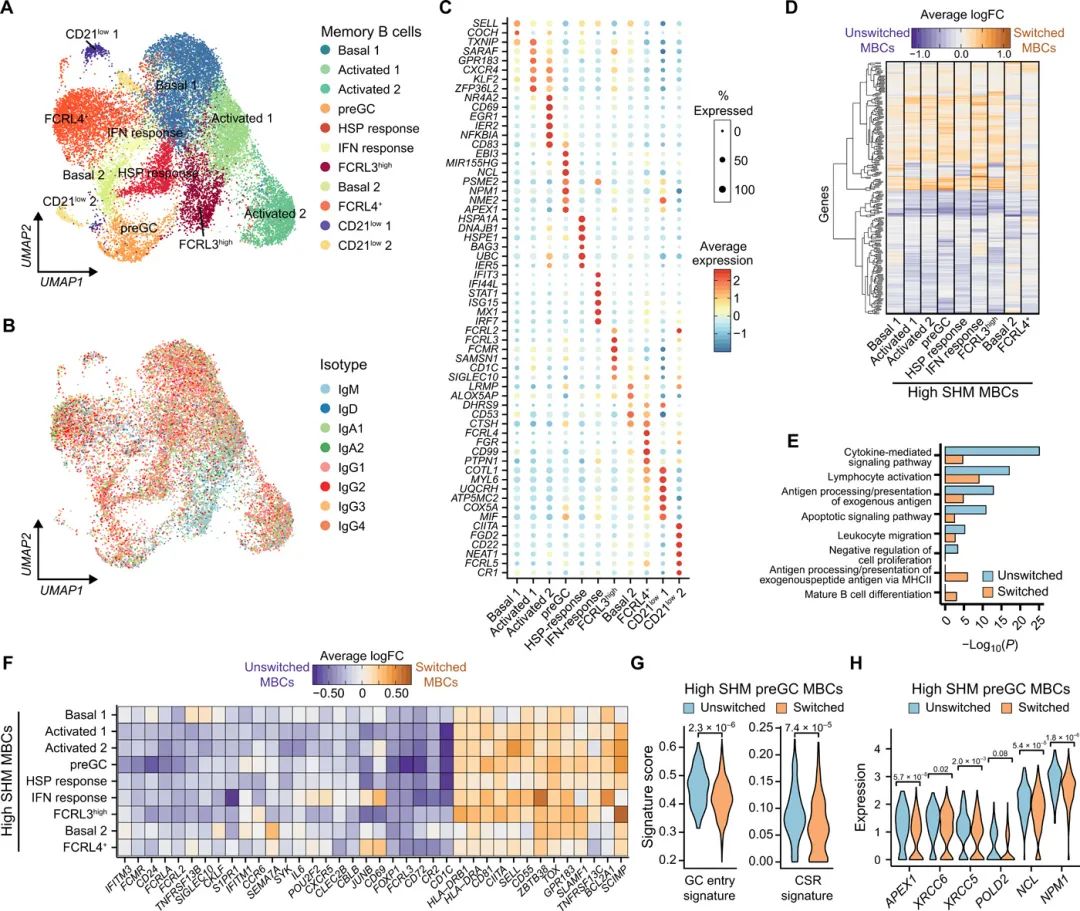
еЫЊ5.дЄНеРМзЪДMBCзКґжАБеТМжКЧдљУз±їдЊЭиµЦеЯЇеЫ†и°®иЊЊгАВ
06жЬ™еИЗжНҐзЪДMBCsзЪДиљђељХињЮжО•ж؃嚥жИРзїІеПСжАІGCsзЪДеЯЇз°А
¬† ¬† ¬†зФ±дЇОи°®иЊЊеЉАеЕ≥еРМеЮЛзЪДMBCsеЊАеЊАеЕЈжЬЙжЫійЂШзЪДSHMйҐСзОЗ(еЫЊ1D)пЉМеЫ†ж≠§еѓєеЕЈжЬЙзЫЄеРМSHMж∞іеє≥зЪДеЉАеЕ≥MBCsињЫи°МжѓФиЊГпЉМиѓБеЃЮдЇЖеєњж≥Ые≠ШеЬ®зЪДеЯЇеЫ†и°®иЊЊеЈЃеЉВдЄОMBCе≠РйЫЖжИЦзКґжАБжЧ†еЕ≥(еЫЊ5DеТМF)гАВињЩи°®жШОMBCsзЪДзЙєеЃЪиљђељХињЮжО•дЊЭиµЦдЇОеЕґжКЧдљУз±їеИЂгАВжЬ™еЉАеЕ≥зЪДMBCsеєњж≥ЫеѓМйЫЖеПВдЄОзїЖиГЮеЫ†е≠РдїЛеѓЉзЪДдњ°еПЈдЉ†еѓЉгАБжњАжіїгАБжКЧеОЯеСИйАТеТМињБзІїзЪДеЯЇеЫ†(еЫЊ5EеТМF)пЉМињЩеПѓиГљеПНжШ†дЇЖIgM+ MBCsдљЬдЄЇеЫЮењЖиЃ∞ењЖеПНеЇФзЪДдЄАйГ®еИЖйЗНжЦ∞еРѓеК®GCеПНеЇФзЪДиГљеКЫеҐЮеК†пЉМињЩжШѓBзїЖиГЮдїЛеѓЉзЪДйХњжЬЯеЕНзЦЂзЪДйЗНи¶БзїДжИРйГ®еИЖгАВдЄОзЫіиІЙзЫЄеПНпЉМIgM+ MBCsдєЯеѓМеРЂжКЧеҐЮжЃЦеТМеЗЛдЇ°еЯЇеЫ†йАЪиЈѓ(еЫЊ5E)пЉМдї•еПКиЃЄе§Ъ襀聧䪯и∞ГиКВжИЦжКСеИґBзїЖиГЮжіїеМЦзЪДеЯЇеЫ†пЉМе¶ВFCRLAгАБFCRL2гАБFCRL3гАБCBLBгАБCD72еТМSIGLEC10гАВињЩи°®жШОпЉМиљђељХж∞іеє≥дЄКзЪДиЙѓе•љи∞ГиКВеє≥и°°еПѓиГљжОІеИґжЬ™еЉАеЕ≥MBCsзЪДжњАжіїйШИеАЉгАВ
¬† ¬† ¬†жЬ™еИЗжНҐзЪДMBCsжѓФз±їеИЂеИЗжНҐзЪДMBCsи°®иЊЊжЫійЂШж∞іеє≥зЪДPOU2F2(дєЯзІ∞дЄЇOCT2)еТМFOXP1(еЫЊ5F)пЉМеЃГдїђеИЖеИЂеНПи∞ГBзїЖиГЮеѓєжКЧеОЯеПЧдљУдњ°еПЈзЪДж≠£еЄЄеПНеЇФиГљеКЫпЉМеєґзЫіжО•жКСеИґжµЖзїЖиГЮеИЖеМЦзЪДеЕ≥йФЃи∞ГиКВеЫ†е≠РгАВињЩдЄОеИЗжНҐеРОзЪДIgG+ MBCsжЫіжЬЙеПѓиГљеИЖеМЦдЄЇжµЖзїЖиГЮзЫЄдЄАиЗіпЉМиАМжЬ™еИЗжНҐзЪДIgM+ MBCsжЫіжЬЙеПѓиГљйЗНжЦ∞ињЫеЕ•жИЦ嚥жИРдЇМжђ°GCеПНеЇФдї•иОЈеЊЧжЫійЂШзЪДдЇ≤еТМеКЫгАВдЄОеРМдЄАз∞ЗдЄ≠еИЗжНҐзЪДMBCsзЫЄжѓФпЉМpre-GCз∞ЗдЄ≠жЬ™еИЗжНҐзЪДMBCsдЄОGCињЫеЕ•еТМCSRзЫЄеЕ≥зЪДеЯЇеЫ†з≠ЊеРНжШЊиСЧеѓМйЫЖ(еЫЊ5GгАБH)гАВињЩжФѓжМБињЩж†ЈдЄАзІНж®°еЮЛпЉМеН≥жЬ™еИЗжНҐзЪДMBCsжѓФеЈ≤еИЗжНҐзЪДMBCsжЫіжЬЙеПѓиÚ嚥жИРдЇМзЇІGCеУНеЇФпЉМеєґдЄФињЩдЇЫжЬ™еИЗжНҐзЪДMBCsеЬ®ж≠§ињЗз®ЛдЄ≠еЗЖе§ЗињЫи°Мз±їеИЗжНҐгАВ
зїУиЃЇ
¬† ¬† ¬†жПРдЊЫдЇЖдЄАдЄ™еЕ®йЭҐзЪДдЇЇз±їBзїЖиГЮжИРзЖЯиЈѓзЇњеЫЊпЉМеНХзїЖиГЮиљђељХзїДе≠¶дЄОе§ІеЃєйЗПеТМеНХзїЖиГЮжКЧдљУеЇУзЫЄеМєйЕНпЉМдї•еЃЪдєЙеЯЇеЫ†и°®иЊЊпЉМжКЧдљУеЇУпЉМдї•еПКеНХзїЖиГЮеИЖиЊ®зОЗдЄЛBзїЖиГЮзКґжАБзЪДеЕЛйЪЖеЕ±дЇЂпЉМеМЕжЛђеПНжШ†дЄНеРМеКЯиГљеТМдњ°еПЈзКґжАБзЪДиЃ∞ењЖBзїЖиГЮеЉВиі®жАІгАВ
¬† ¬† ¬†йЗНеїЇдЇЖBзїЖиГЮжњАжіїињЗз®ЛдЄ≠зЪДеЯЇеЫ†и°®иЊЊеК®жАБпЉМжП≠з§ЇдЇЖзФЯеПСеЙНдЄ≠ењГзКґжАБеРѓеК®ињЫи°Мз±їеЉАеЕ≥йЗНзїДпЉМеєґиІ£еЙЦдЇЖзФЯеПСдЄ≠ењГеТМиЃ∞ењЖBзїЖиГЮдЄ≠жКЧдљУз±їдЊЭиµЦзЪДеЯЇеЫ†и°®иЊЊе¶ВдљХдЄОзЛђзЙєзЪДиљђељХзЇњиЈѓиБФз≥їеЬ®дЄАиµЈпЉМињЩдЇЫиљђељХзЇњиЈѓеПѓиГљељ±еУНеЃГдїђзЪДеСљињРеТМеКЯиГљгАВ
¬† ¬† ¬†жП≠з§ЇдЇЖ嚥жИРдЇЇз±їBзїЖиГЮдїЛеѓЉеЕНзЦЂзЪДеК®жАБзїЖиГЮзКґжАБпЉМеєґеЉЇи∞ГдЇЖжКЧдљУеРМеЮЛе¶ВдљХеЬ®еЯЇдЇОжКЧдљУзЪДйАЙжЛ©дЄ≠еПСжМ•дљЬзФ®гАВ
еПВиАГжЦЗзМЃ
Hamish W. King et al.Single-cell analysis of human B cell maturation predicts how antibody class switching shapes selection dynamics.Sci.
Immunol.6,eabe6291(2021).DOI:10.1126/sciimmunol.abe6291

жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљеЖЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂеЯЇеЫ†зїДе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДйЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РпЉИзЇ≥жЦѓиЊЊеЕЛдї£з†БпЉЪGTHпЉЙдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†|TзїЖиГЮеЕНзЦЂжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃзЦЊзЧЕжЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБTCR-TиНѓзЙ©еЉАеПСз≠Йеє≥еП∞зЃ°зЇњгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВ
иЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ

