

жИРдЇЇжА•жАІжЈЛеЈізїЖиГЮзЩљи°АзЧЕдљОж∞іеє≥MRDзЪДйҐДеРОдїЈеАЉ

дљњзФ®дЄЛдЄАдї£жµЛеЇПпЉИNGSпЉЙеѓєMolNEж†ЈжЬђињЫи°МеЫЮй°ЊжАІйЗНжЦ∞еИЖжЮРпЉМзїУжЮЬеПСзО∞NGS-MRDйШіжАІзЪДжВ£иАЕзЪДйҐДеРОжШОжШЊдЉШдЇОNGS-MRDйШ≥жАІзЪДжВ£иАЕпЉМиѓіжШОNGSиГље§ЯеѓєдљОж∞іеє≥дЄНеПѓеЃЪйЗПзЪДRQ-PCR MRDйШ≥жАІзЪДжВ£иАЕињЫи°МжЫіеЗЖз°ЃзЪДй£ОйЩ©йҐДжµЛгАВ


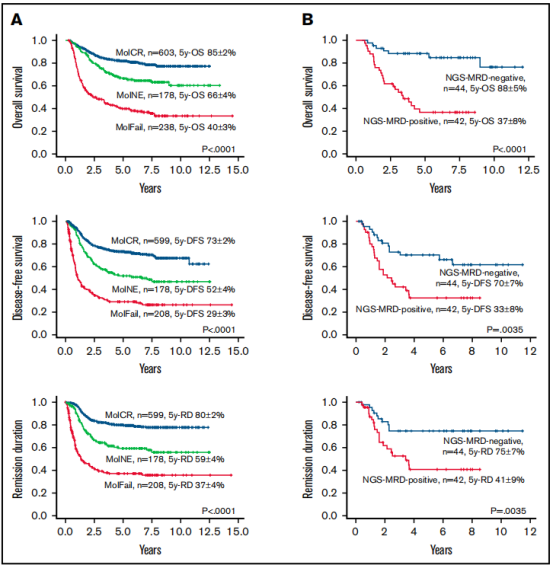
MolNEзїДжВ£иАЕзЪД5еєіOSгАБ5еєіDFSгАБ5еєіRDеЭЗдљНдЇОMolCRзїДеТМMolFailзїДдєЛйЧіпЉМжШЊз§ЇдЄ≠йЧійҐДеРОпЉИеЫЊAпЉЙгАВMolNE嚥жИРдЇЖдЄАдЄ™дЄ≠еЇ¶й£ОйЩ©зїДгАВ
еѓєMolNEзїДињЫи°МNGS-MRDж£АжµЛгАВNGS-MRDйШіжАІжВ£иАЕзЪД5еєіOSгАБ5еєіDFSгАБ5еєіRDеЭЗжШЊиСЧйЂШдЇОNGS-MRDйШ≥жАІзЪДжВ£иАЕпЉИеЫЊBпЉЙгАВиѓіжШОNGSињЫдЄАж≠•жФєеЦДдЇЖMolNEзїДзЪДй£ОйЩ©еЇ¶еИЖе±ВгАВ




жѓПзІНB/TжЈЛеЈізїЖиГЮи°®йЭҐеЭЗе≠ШеЬ®дЄАзІНзЙєеЉВжАІBзїЖиГЮеПЧдљУ B cell receptor,BCR/la)TзїЖиГЮеПЧдљУ (T cell receptor,TCR)пЉМзФ±дЇОBCR/TCRеЫ†дЄ≠VгАБDгАБJеЯЇеЫ†зЙЗжЃµйЗНзїДдЄО祱еЯЇзЪДйЪПжЬЇжПТеЕ•гАБеИ†еЗПпЉМеѓЉиЗіBCR/TCRеЕЈжЬЙйЂШеЇ¶е§Ъж†ЈжАІзЪДзЙєзВєпЉМдїОиАМBCR/TCRеПѓдљЬдЄЇжѓПдЄ™BTжЈЛеЈізїЖиГЮеФѓдЄАзЪДеИЖе≠Рж†Зз≠ЊгАВ
жЈЛз≥їи°Ажґ≤зЩМзЧЗжВ£иАЕеЫ†BTжЈЛеЈізїЖиГЮеПСзФЯзЩМеПШпЉМзЩМзїЖиГЮзїІиАМиЗ™жИСе§Неȴ嚥жИРеЕЛйЪЖжАІеҐЮжЃЦпЉМеЫ†ж≠§пЉМйАЪињЗж£АжµЛB/TжЈЛеЈізїЖиГЮи°®йЭҐеПЧдљУBCR/TCRеПѓдї•йЙіеЃЪзЩМзїЖиГЮеєґињљиЄ™ж£АжµЛзЩМзїЖиГЮзЪДеК®жАБеПШеМЦгАВ

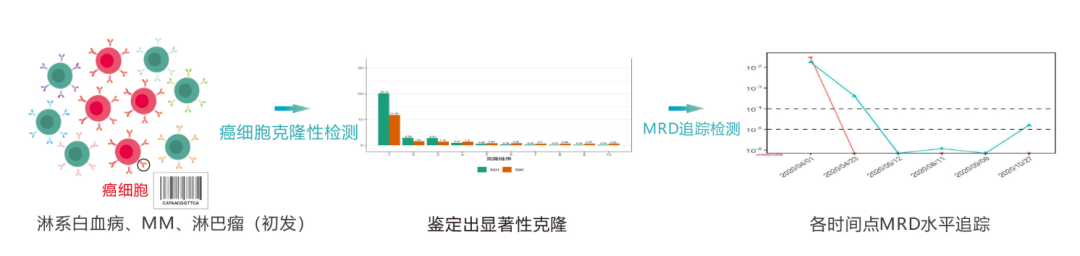
1.зЩМзїЖиГЮеЕЛйЪЖжАІж£АжµЛ
йАЪињЗжВ£иАЕеИЭиѓКжИЦзЩМзїЖиГЮйЂШиіЯиНЈжЧґзЪДй™®йЂУж†ЈжЬђпЉМжЙЊеИ∞зЩМзїЖиГЮзЙєжЬЙзЪДDNAвАЬж†Зз≠ЊвАЭеЇПеИЧгАВ
2.MRDињљиЄ™ж£АжµЛ
еИ©зФ®з≠ЫжЯ•еЗЇзЪДDNAвАЬж†Зз≠ЊвАЭеЇПеИЧпЉМеЬ®ж≤їзЦЧжЬЯйЧіжИЦж≤їзЦЧеРОиѓДдЉ∞MRDж∞іеє≥пЉМзЫСжµЛзЩМзїЖиГЮеРЂйЗПпЉМеРМжЧґж£АжµЛиѓЖеИЂжЦ∞еЗЇзО∞зЪДзЩМзїЖиГЮеЇПеИЧгАВ

1. Bз≥їи°Ажґ≤з≥їзїЯзЩМзЧЗ
жА•жАІ/жЕҐжАІBжЈЛеЈізїЖиГЮзЩљи°АзЧЕгАБе§ЪеПСжАІй™®йЂУзШ§гАБBеЮЛжЈЛеЈізШ§гАВ
2. Tз≥їи°Ажґ≤з≥їзїЯзЩМзЧЗ
жА•жАІ/жЕҐжАІTжЈЛеЈізїЖиГЮзЩљи°АзЧЕгАБTеЮЛжЈЛеЈізШ§гАВ

Seq-MRD¬ЃиГљжПРдЊЫйЂШз≤ЊеЇ¶гАБйЂШзБµжХПеЇ¶зЪДMRDж£АжµЛиІ£еЖ≥жЦєж°ИпЉМеПѓеЄЃеК©еМїзФЯжЫіеЗЖз°ЃеЬ∞иѓДдЉ∞зЩМзЧЗжВ£иАЕзЪДж≤їзЦЧеПНеЇФеТМйҐДеРОгАВињЩдЇЫжКАжЬѓеЬ®зО∞дї£иВњзШ§ж≤їзЦЧдЄ≠жЙЃжЉФзЭАиґКжЭ•иґКйЗНи¶БзЪДиІТиЙ≤пЉМеЫ†дЄЇеЃГдїђиГље§ЯеЄЃеК©еМїзФЯиѓЖеИЂйВ£дЇЫжВ£зЧЕе§НеПСй£ОйЩ©йЂШзЪДжВ£иАЕпЉМеєґдЄЇдїЦдїђжПРдЊЫжЫідЄ™жАІеМЦгАБжЫіжЬЙйТИеѓєжАІзЪДж≤їзЦЧжЦєж°ИгАВ



Seq-MRD¬ЃиОЈеЊЧжђІзЫЯCEиµДиі®пЉИж≥®еЖМеПЈпЉЪDE/CA20/01-IVD-Luxuslebenswelt-190/22пЉЙпЉМиОЈжЙєзЪДжШѓдЇЇжЈЛеЈіBзїЖиГЮеЊЃе∞ПжЃЛзХЩзЧЕеЯЇеЫ†ж£АжµЛиѓХеЙВзЫТпЉИеПѓйАЖжЬЂзЂѓзїИж≠ҐжµЛеЇПж≥ХпЉЙгАВ


иЙЊж≤РиТљжО®еЗЇзЪДSeq-MRD¬Ѓи°Ажґ≤зЩМзЧЗMRDж£АжµЛжШѓжЬАжЧ©жЙєеЃЮзО∞еХЖдЄЪеМЦзЪДдЇІеУБпЉМиЗ™2016еєіз†ФеПСдЄУеИ©жКАжЬѓиЗ≥дїКпЉМиЙЊж≤РиТљSeq-MRD¬ЃеЈ≤зїПиОЈеЊЧ3й°єеЫљеЃґеПСжШОдЄУеИ©пЉЪ
[1]вАЬдЄАзІНеЇФзФ®дЇОйЂШйАЪйЗПжµЛеЇПж£АжµЛTзїЖиГЮзЩљи°АзЧЕеЊЃе∞ПжЃЛзХЩзЧЕзЪДеЉХзЙ©зїДеРИеПКиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2016 11204857.0пЉМжОИжЭГеЕђеСКеПЈ:CN 106957906 BпЉЙ
[2]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1550133.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109652518 BпЉЙ
[3]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДжЦєж≥ХвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1549203.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109680062 BпЉЙ


Seq-MRD¬ЃеПСи°®зЫЄеЕ≥жЦЗзМЃ
Huang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H.¬†Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy.¬†Bone Marrow Transplant. 2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ


жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљеЖЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂеЯЇеЫ†зїДе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДйЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РпЉИзЇ≥жЦѓиЊЊеЕЛдї£з†БпЉЪGTHпЉЙдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†|TзїЖиГЮеЕНзЦЂжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃзЦЊзЧЕжЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБTCR-TиНѓзЙ©еЉАеПСз≠Йеє≥еП∞зЃ°зЇњгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВ
иЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ


