2023еєі12жЬИ14жЧ•пЉМиЙЊж≤РиТљеК©еКЫдЄ≠еЫљзІСе≠¶йЩҐињЗз®ЛеЈ•з®Лз†Фз©ґжЙАй©ђеЕЙиЊЙйЩҐе£ЂгАБй≠ПзВЬз†Фз©ґеСШеЫҐйШЯиБФеРИеЖЫдЇЛеМїе≠¶зІСе≠¶йЩҐзФЯзЙ©еЈ•з®Лз†Фз©ґжЙАжЬ±еКЫз†Фз©ґеСШгАБзОЛжБТж®Сз†Фз©ґеСШеЫҐйШЯпЉМеЬ®еЫљйЩЕй°ґе∞Це≠¶жЬѓжЬЯеИК Nature дЄКеПСи°®дЇЖйҐШдЄЇпЉЪInhaled SARS-CoV-2 vaccine for single-dose dry powder aerosol immunization зЪДз†Фз©ґиЃЇжЦЗгАВз†Фз©ґеЉАеПСдЇЖдЄАзІНеПѓеРЄеЕ•зЪДеНХеЙВйЗПеє≤з≤Йж∞ФйЫЊеЙВSARS-CoV-2 зЦЂиЛЧпЉМеЃГиГљиѓ±еѓЉжЬЙжХИзЪДеЕ®иЇЂеТМз≤ШиЖЬеЕНзЦЂеПНеЇФгАВиѓ•зЦЂиЛЧе∞ЖеМЕеРЂиЫЛзЩљиі®йЬНдє±жѓТзі† B дЇЪеЯЇзЪДзїДи£ЕзЇ≥з±≥йҐЧз≤Те∞Би£ЕеЬ®жЬАдљ≥з©Їж∞ФеК®еКЫе≠¶е∞ЇеѓЄзЪДеЊЃиГґеЫКдЄ≠гАВињЩзІНзЛђзЙєзЪДзЇ≥з±≥-еЊЃеЮЛиА¶еРИзїУжЮДжФѓжМБйЂШжХИзЪДиВЇж≥°иЊУйАБгАБжКЧеОЯжМБзї≠йЗКжФЊеТМжКЧеОЯеСИйАТзїЖиГЮжСДеПЦпЉМињЩдЇЫйГљжШѓиѓ±еѓЉеЕНзЦЂеПНеЇФзЪДжЬЙеИ©зЙєеЊБгАВж≠§е§ЦпЉМињЩзІНзЦЂиЛЧињШиГљиѓ±еѓЉдЇІзФЯеЉЇе§ІзЪД IgG еТМ IgAпЉМдї•еПКе±АйГ® T зїЖиГЮеПНеЇФпЉМдїОиАМеЬ®е∞ПйЉ†гАБдїУйЉ†еТМйЭЮдЇЇзБµйХњз±їеК®зЙ©иЇЂдЄКеЕ±еРМдЇІзФЯйТИеѓє SARS-CoV-2 зЪДжЬЙжХИдњЭжК§гАВжЦЗдЄ≠дљњзФ®иЙЊж≤РиТљзФЯзЙ©ImmuHub¬Ѓ BCRеИЖжЮРз≥їзїЯпЉМеѓєиВЇжЈЛеЈізїЖиГЮBзїЖиГЮеПЧдљУињЫи°М(BCR)жµЛеЇПпЉМжХ∞жНЃжШЊз§ЇеЗЇйЂШж∞іеє≥зЪДзІНз≥їеИЖеМЦпЉМињЫдЄАж≠•и°®жШОињЩзІНйХњжЬЯжКЧдљУеЇФз≠ФдЉЉдєОжЬЙжЬЫйАЪињЗеК†йАЯдЇ≤еТМжИРзЖЯжЭ•жПРйЂШжКЧдљУиі®йЗПгАВ

з†Фз©ґиГМжЩѓ COVID-19жШѓзФ±SARS-CoV-2еЉХиµЈзЪДдЄАзІНдЄ•йЗНжА•жАІеСЉеРЄз≥їзїЯзїЉеРИзЧЗпЉМдЇО2020еєіиҐЂеЃ£еЄГдЄЇе§ІжµБи°МгАВзЦЂиЛЧжО•зІНжШѓжИРеКЯйҐДйШ≤еТМжОІеИґиѓ•зЦЊзЧЕдЉ†жТ≠зЪДеЕђеЕ±еНЂзФЯеє≤йҐДжО™жЦљгАВињДдїКдЄЇж≠ҐпЉМеЈ≤жЙєеЗЖе§ЪзІНз±їеЮЛзЪДSARS-CoV-2зЦЂиЛЧпЉМеМЕжЛђзБ≠жіїзЦЂиЛЧгАБиЫЛзЩљдЇЪеНХдљНзЦЂиЛЧгАБmRNAзЦЂиЛЧеТМзЧЕжѓТиљљдљУзЦЂиЛЧгАВињЩдЇЫзЦЂиЛЧе§Іе§ЪйАЪињЗиВМиВЙж≥®е∞ДзїЩиНѓпЉМиѓ±еѓЉдЇІзФЯи°АжЄЕе≠¶IgGпЉМдїОиАМдЄ≠еТМзЧЕжѓТзЪДдЉ†жЯУжАІеєґзЉУиІ£COVID-19зЪДзЧЗзКґгАВзДґиАМпЉМзФ±дЇОиВМиВЙж≥®е∞ДзЦЂиЛЧжЧ†ж≥ХеЬ®ж∞ФйБУз≤ШиЖЬзїДзїЗдЄ≠иѓ±еѓЉеЕНзЦЂеПНеЇФпЉМиАМж≠£жШѓињЩдЇЫзїДзїЗжШѓSARS-CoV-2ињЫеЕ•зЪДйГ®дљНпЉМеЫ†ж≠§еЬ®еИЖж≥МеЮЛIgAеТМIgGжЦєйЭҐе≠ШеЬ®дЄНиґ≥гАВж≠§е§ЦпЉМзЫЃеЙНзЪДCOVID-19зЦЂиЛЧйЬАи¶БеЬ®дљОжЄ©вАЬеЖЈйУЊвАЭжЭ°дїґдЄЛеИґйА†гАБињРиЊУгАБеВ®е≠ШеТМзЃ°зРЖпЉМеҐЮеК†дЇЖжИРжЬђгАВ з†Фз©ґзїУжЮЬ R-CNPзЪДеИґе§З з≤ШиЖЬдљРеЙВжАІеТМ CTB зЪДдЇФиБЪдљУзїУжЮДеЯЯжЬАеИЭдњГдљњдљЬиАЕжЮДеїЇдЄАзІНиЗ™дљРеЙВзЇ≥з±≥еЇХзЫШпЉМиѓ•еЇХзЫШжШѓйАЪињЗеЬ® CTB C зЂѓиЮНеРИдЄЙиБЪдљУ嚥жИРиВљеЃЮзО∞зЪДпЉМйЪПеРОеЬ®е§ІиВ†жЭЖиПМ BL21 иПМ憙дЄ≠и°®иЊЊпЉИеЫЊ 1aпЉЙгАВйАЪињЗ SpyTagпЉИSTпЉЙ-SpyCatcherпЉИSCпЉЙзФЯзЙ©ж≠£дЇ§з≥їзїЯпЉМдЇІзФЯзЪД CNP еЇХзЫШжШЊз§ЇеЗЇ RBD жКЧеОЯпЉМињЩжЬЙеИ©дЇОжПРйЂШжКЧеОЯз®≥еЃЪжАІгАБAPC еРЄжФґеТМжіїеМЦгАВдїО SDS-PAGE еТМеЕНзЦЂеН∞ињєеИЖжЮРпЉИеЫЊ 1bпЉЙеПѓдї•зЬЛеЗЇпЉМдЄО ST-CNP жЈЈеРИеРОпЉМSC-RBD еЄ¶зЪДеИЖе≠РйЗПеПСзФЯдЇЖжШОжШЊеПШеМЦпЉМи°®жШОеЕ±дїЈйФЃеЈ≤зїП嚥жИРгАВйАПе∞ДзФµе≠РжШЊеЊЃйХЬжШЊз§ЇпЉМR-CNP еЕЈжЬЙеИЖжХ£иЙѓе•љзЪДзЇ≥з±≥йҐЧз≤ТзЙєеЊБпЉИеЫЊ 1cпЉЙгАВжО•дЄЛжЭ•пЉМдљЬиАЕйАЪињЗж£АжµЛдЄОдЇЇз±їACE2 (hACE2)еПЧдљУзЪДзїУеРИдЇ≤еТМеКЫеТМеК®еКЫе≠¶жЭ•и°®еЊБR-CNPзЪДжКЧеОЯжАІгАВйЕґиБФеЕНзЦЂеРЄйЩДиѓХй™М(ELISAs)еТМи°®йЭҐз≠Йз¶їе≠РдљУеЕ±жМѓиѓХй™МжШЊз§ЇпЉМRBDеНХдљУеТМR-CNPдї•з±їдЉЉзЪДеЙВйЗПдЊЭиµЦжАІжЦєеЉПзїУеРИеИ∞hACE2дЄК(еЫЊ1d)пЉМи°®жШОR-CNPдЄКзЪДи°®дљН襀ж≠£з°ЃжЪійЬ≤еТМжКШеП†гАВж≠§е§ЦпЉМдљЬиАЕеЬ®дљУе§Цй™МиѓБдЇЖR-CNPsзЪДAPCжњАжіїиГљеКЫпЉМеПСзО∞дЄїи¶БзїДзїЗзЫЄеЃєжАІе§НеРИдљУ(MHC)еТМеЕ±еИЇжњАеИЖе≠Рж∞іеє≥еҐЮеК†пЉМе§ЪзІНзїЖиГЮеЫ†е≠РзЪДеИЖж≥МеҐЮеК†гАВеЫ†ж≠§пЉМдљЬиАЕзЪДSpyTag-SpyCatcherдїЛеѓЉзЪДRBDжКЧеОЯдЄОCNPзЪДйЩДзЭАе¶ВйҐДжЬЯзЪДйВ£ж†ЈиµЈдљЬзФ®гАВ R-CNP@MзЪДиЃЊиЃ°дЄОеИґе§З иАГиЩСеИ∞зЫіжО•еРЄеЕ•зЇ≥з±≥зЇІеИґеЙВеЬ®иВЇж≥°дЄ≠зЪДж≤ЙзІѓиГљеКЫиЊГеЈЃпЉМеєґдЄФеЕИеЙНзЪДз†Фз©ґеЈ≤зїПжК•йБУдЇЖз©Їж∞ФеК®еКЫе≠¶зЫіеЊДеЬ®1-4¬µmиМГеЫіеЖЕзЪДйҐЧз≤ТеЬ®иВЇж≥°дЄ≠зЪДжЬЙжХИиЊУйАБпЉМдљЬиАЕжИСдїђйАЪињЗе∞ЖR-CNPsжФЊзљЃеЬ®еРИйАВзЪДз©Їж∞ФеК®еКЫе≠¶е∞ЇеѓЄзЪДеЊЃиГґеЫКдЄ≠ињЫи°МR-CNP@MиЃЊиЃ°гАВињЩеЇФиѓ•еЕБиЃЄжЬЙжХИеЬ∞йАТйАБеИ∞иВЇж≥°пЉМеєґдљњR-CNPsжМБзї≠йЗКжФЊпЉМдї•жФѓжМБжМБзї≠зЪДжКЧеОЯеИЇжњАгАВдљЬиАЕйЗЗзФ®иЖЬдє≥еМЦжЦєж≥ХеИґе§Зе§Ъе≠ФPLGAеЊЃзРГпЉМйАЪињЗзЃАеНХжЈЈеРИеТМжЄ©еТМзЪДеК†зГ≠дїЛеѓЉеѓЖе∞БR-CNPs(еЫЊ1e)йАЪињЗеЊЃи∞ГиЖЬе≠ФеЊДгАБжЄЧйАП楃寶еТМе≠ФйЪЩжЉФеМЦжЧґйЧіпЉМеПѓдї•жОІеИґеЊЃзРГзЪДз≤ТеЊДгАБе≠ФйЪЩеЇ¶еТМз©ЇиЕФеЃєзІѓпЉМдїОиАМдЉШеМЦR-CNP@MиОЈеЊЧеРИйАВзЪДж∞ФеК®е∞ЇеѓЄеТМиЊГйЂШзЪДе∞Би£ЕжХИзОЗгАВ дљњзФ®еЕ±иБЪзД¶жњАеЕЙжЙЂжППжШЊеЊЃйХЬеѓєжЙАеЊЧR-CNP@MињЫи°МдЇЖи°®еЊБпЉМдЄЙзїійЗНеїЇжПРдЊЫдЇЖеЉЇжЬЙеКЫзЪДиѓБжНЃпЉМиѓБжШОе∞ЉзљЧж≤≥зЇҐж†ЗиЃ∞еЊЃиГґеЫКзЪДеЖЕиЕФеЕЕжї°дЇЖеЉВз°Ђж∞∞йЕЄиНІеЕЙзі†(FITC)ж†ЗиЃ∞зЪДR-CNPs(еЫЊ1e)гАВR-CNP@MзїПеЖїеє≤еРОеСИзЩљиЙ≤з≤ЙжЬЂзКґпЉМеИЖжХ£жАІжЮБе•љпЉМзФ®еє≤з≤Йж∞ФжЇґиГґеПСзФЯеЩ®(DPAG)еЦЈе∞ДеРОеσ嚥жИРеЭЗеМАзЪДйЫЊ(еЫЊ1f)гАВињЩдЇЫеЖїеє≤зЪДеЊЃиГґеЫКеЗ†дєОеЃМеЕ®еЬ®зРЖжГ≥зЪДз©Їж∞ФеК®еКЫе≠¶е∞ЇеѓЄиМГеЫіеЖЕ(2-4¬µm;еЫЊ1 g)гАВж≠§е§ЦпЉМдїЦдїђжШЊз§ЇR-CNPеЬ®дЇФеС®еЖЕжМБзї≠йЗКжФЊпЉМеєґдЄФйЗКжФЊзЪДR-CNPдЄОжЦ∞й≤ЬзЪДR-CNPеѓєhACE2зЪДзїУеРИдЇ≤еТМеКЫж≤°жЬЙеЈЃеЉВ(еЫЊ1h)гАВе≠ШеВ®дЄАдЄ™жЬИеРОзЪДжµЛиѓХи°®жШОпЉМR-CNP@MзЪДж∞ФеК®зЫіеЊДеТМе∞Би£ЕеРОзЪДR-CNPзЪДж∞іеК®еКЫзЫіеЊДеПШеМЦеПѓдї•ењљзХ•дЄНиЃ°пЉМжФѓжМБиЙѓе•љзЪДе≠ШеВ®з®≥еЃЪжАІгАВ дљУеЖЕзФЯзЙ©еИЖеЄГеТМйЗКжФЊ дљЬиАЕз†Фз©ґдЇЖеє≤з≤ЙеРЄеЕ•еЩ®(DPI)зїЩиНѓеРОеЕґеЬ®иВЇйГ®зЪДдњЭзХЩгАБж≤ЙзІѓгАБйЗКжФЊеТМжСДеПЦжГЕеЖµ(еЫЊ1i)гАВдЄЇдЇЖжµЛйЗПдњЭзХЩзОЗпЉМдљЬиАЕжПРдЊЫдЇЖеРЂжЬЙcy7ж†ЗиЃ∞зЪДR-CNPsзЪДеЊЃиГґеЫКзЦЂиЛЧпЉМеєґзЇ≥еЕ•дЇЖдЄАзїДжО•еПЧз≠ЙжХИcy7ж†ЗиЃ∞зЪДR-CNPsж∞ФжЇґиГґзїЩиНѓзЪДе∞ПйЉ†ињЫи°МжѓФиЊГ(еЫЊ1j)гАВдЄОR-CNPзїДе∞ПйЉ†5姩еРОиВЇйГ®жЧ†иНІеЕЙдњ°еПЈзЫЄжѓФпЉМR-CNP@MзїДе∞ПйЉ†зђђ5姩иВЇйГ®дїНжЬЙ50%зЪДеИЭеІЛдњ°еПЈеЉЇеЇ¶пЉМзЫіеИ∞зђђ42姩дїНжЬЙиНІеЕЙдњ°еПЈгАВдЄОR-CNPзЫЄжѓФпЉМR-CNP@MзЪДжЫ≤зЇњдЄЛйЭҐзІѓеАЉжПРйЂШдЇЖ3.5еАНпЉМи°®жШОR-CNP@MеПѓдї•еЬ®иВЇдЄ≠иѓ±еѓЉжМБзї≠зЪДжКЧеОЯеИЇжњАгАВ дљЬиАЕзФ®йУЊйЬЙдЇ≤еТМзі†- AF647еТМе∞ЉзљЧзЇҐеИЖеИЂж†ЗиЃ∞ж∞ФзЃ°еТМеЊЃиГґеЫКпЉМеєґзФ®иЦДе±ВжШЊеЊЃйХЬж£АжЯ•еЕґеИЖеЄГгАВдї•еРЄеЕ•еРОзђђ5姩еП≥дЄКиВЇеПґдЄЇдЊЛпЉМеЊЃиГґеЫКеЭЗеМАеИЖеЄГдЇОиВЇеПґ(еЫЊ1k)гАВеЕ®иВЇзїДзїЗеИЗзЙЗ(зђђ5姩)жШЊз§ЇпЉМж∞ФзЃ°гАБеОЯеПСжАІжФѓж∞ФзЃ°еТМзїІеПСжАІжФѓж∞ФзЃ°дЄ≠еЊЃиГґеЫКиЊГе∞СпЉМе§Іе§ЪжХ∞еЊЃиГґеЫКж≤ЙзІѓеЬ®ињЬзЂѓиВЇпЉМеМЕжЛђжЬЂзЂѓжФѓж∞ФзЃ°еТМиВЇж≥°(еЫЊ1lеТМжЙ©е±ХжХ∞жНЃеЫЊ3h)гАВзђђ10姩зЪДеИЗзЙЗжШЊз§ЇжЭ•иЗ™R-CNPsеТМеЊЃзРГзЪДйЭЮеЕ±еЃЪдљНдњ°еПЈпЉМжФѓжМБR-CNPsдїОйЩНиІ£зЪДеЊЃиГґеЫКдЄ≠жИРеКЯйЗКжФЊ(еЫЊ1m)гАВжµБеЉПзїЖиГЮжЬѓиѓБеЃЮдЇЖиВЇдЄ≠APCsеѓєињЩдЇЫR-CNPsзЪДжЬЙеИ©жСДеПЦпЉМињСдЄАеНКзЪДAPCsе≠ШеЬ®дЇОR-CNPйШ≥жАІзїЖиГЮдЄ≠(еЫЊ1n)гАВињЩдЇЫзїУжЮЬи°®жШОпЉМR-CNP@MзЦЂиЛЧеПѓдї•жЬЙжХИеЬ∞йАТйАБеИ∞иВЇж≥°пЉМеєґдЄФеЊЃиГґеЫКйЗКжФЊзЪДR-CNPs襀APCеЖЕеМЦгАВ
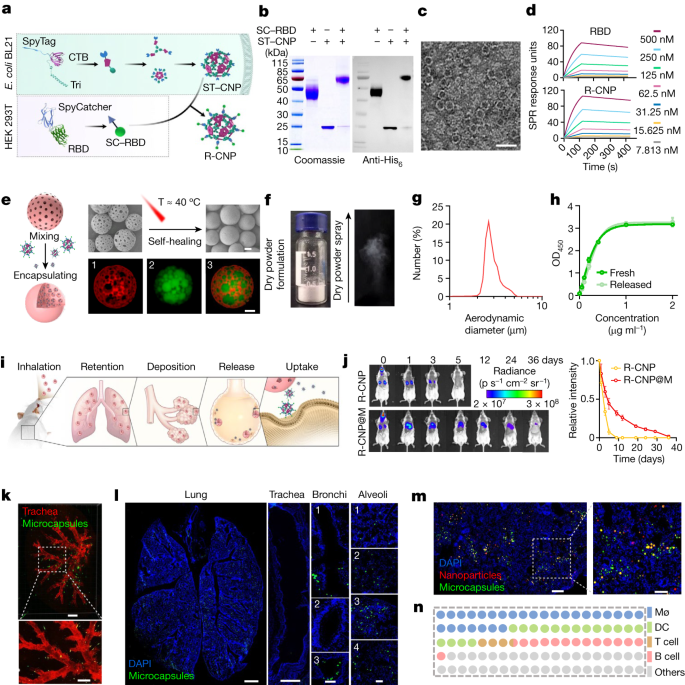
еЫЊ1пЉЪеПѓеРЄеЕ•R-CNP@MзЦЂиЛЧзЪДжЮДеїЇеТМе∞ПйЉ†иВЇйГ®йАТйАБиѓДдЉ∞ еЕНзЦЂзїЖиГЮзЪДжЬЙжХИеПНеЇФ дЄЇдЇЖз†Фз©ґеРЄеЕ•зЦЂиЛЧеѓєиВЇйГ®еЕНзЦЂеПНеЇФзЪДељ±еУНпЉМдљЬиАЕеЬ®зђђ 21 姩僺иВЇйГ®еИЖеЕНзЦЂзїЖиГЮињЫи°МдЇЖеНХзїЖиГЮ RNA жµЛеЇПпЉИscRNA-seqпЉЙгАВscRNA-seq жХ∞жНЃеИЖдЄЇдєЭзІНзїЖиГЮз±їеЮЛпЉИеЫЊ 2aпЉЙгАВдї• APCпЉИж†Сз™БзКґзїЖиГЮеТМеЈ®еЩђзїЖиГЮпЉЙдЄЇйЗНзВєпЉМжО•зІНзїДзЪДжѓФдЊЛеТМжХ∞йЗПеЭЗжЬЙжЙАеҐЮеК†гАВдљЬиАЕињШиѓДдЉ∞дЇЖеСЉеРЄйБУдЄ≠зЪД T зїЖиГЮеПНеЇФпЉМеЬ®дЄЛеСЉеРЄйБУпЉМеЕНзЦЂеРО 21 姩еТМ 70 姩 CD8+ иЃ∞ењЖ T зїЖиГЮзЪДжѓФдЊЛдЊЭжђ°дЄЇ PBSгАБCNPгАБR-CNP еТМ R-CNP@MпЉИеЫЊ 2dпЉЙгАВеИ∞зђђ 70 姩пЉМR-CNP зїД CD8+ зїДзїЗй©їзХЩиЃ∞ењЖ TпЉИTRMпЉЙзїЖиГЮзЪДжѓФдЊЛдїОзђђ 21 姩зЪД 30.63 ¬± 1.24% йЩНиЗ≥ 11.06 ¬± 2.81%пЉМиАМ R-CNP@M зїДеЬ®дЄ§дЄ™еПЦж†ЈжЧ•зЪДжѓФдЊЛеЭЗдњЭжМБеЬ® 21% еЈ¶еП≥пЉМињЩи°®жШОжМБзї≠йЗКжФЊжЬЙеИ©дЇО CD8+ TRM зїЖиГЮзЪДйХњжЬЯзїіжМБпЉИеЫЊ 2eпЉЙгАВ дљЬиАЕеИЖеИЂйЙіеЃЪCD8+еТМCD4+ TзїЖиГЮзЪДRBDи°®дљН(CGPKKSTNLеТМVGGNYNYLYRLFRKS)пЉМиГље§Яз†Фз©ґи°®дљНзЙєеЉВжАІTзїЖиГЮеПНеЇФгАВеЬ®дЄЛеСЉеРЄйБУпЉМR-CNP@MзїДеЬ®еИЖж≥МIFN-ќ≥зЪДTRMзїЖиГЮеПНеЇФзЪДеєЕеЇ¶еТМжМБзї≠жЧґйЧідЄКйГљдЉШдЇОеЕґдїЦзїД(еЫЊ2f)гАВдљЬиАЕињШиѓДдЉ∞дЇЖзїЖиГЮеЖЕзїЖиГЮеЫ†е≠Р(IFNќ≥пЉМ TNFеТМзЩљзїЖиГЮдїЛзі†(IL)-2)жЭ•иѓДдЉ∞иВЇдЄ≠CD8+ TзїЖиГЮзЪДе§ЪеКЯиГљжАІпЉМR-CNP@MзїДеЬ®и°®дљНеИЇжњАдЄЛжШЊз§ЇеПМйШ≥жАІеТМдЄЙйШ≥жАІCD8+ TзїЖиГЮзЪДжѓФдЊЛжШЊзЭАеҐЮеК†(еЫЊ2g)гАВ жО•дЄЛжЭ•ињШиѓДдЉ∞дЇЖдЄїи¶БдїЛеѓЉдљУжґ≤еЕНзЦЂзЪДBзїЖиГЮеПНеЇФгАВеЕЙзЙЗжИРеГПжШЊз§ЇBзїЖиГЮеНµж≥°жШОжШЊеҐЮе§І(жМЙPBSгАБCNPгАБR-CNPеТМR-CNP@MзЪДй°ЇеЇПеҐЮе§І)пЉМжПРз§ЇеРОдЄ§зїДиѓ±еѓЉдЇЖеРЂжЬЙзФЯеПСдЄ≠ењГ(GCs)зЪДжђ°зЇІеНµж≥°(еЫЊ2h)гАВж≠§е§ЦпЉМйАЪињЗжµБеЉПзїЖиГЮжЬѓж£АжµЛеИ∞зЪДзФЯеПСдЄ≠ењГBзїЖиГЮ(IgDвИТGL7+B220+)жѓФдЊЛжЬАйЂШ(еЫЊ2i)пЉМдї•еПКиЃ∞ењЖBзїЖиГЮеИЖеМЦзЪДеЯЇеЫ†и°®иЊЊжШЊиСЧдЄКи∞ГпЉМйГљжФѓжМБдЇЖR-CNP@Mиѓ±еѓЉзЪДжЬЙжХИдљУжґ≤еПНеЇФгАВ
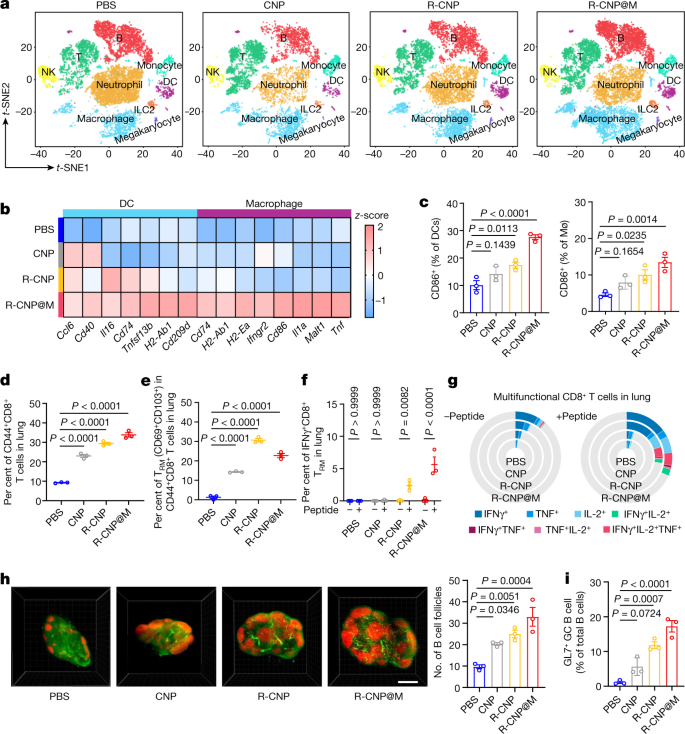
еЫЊ2пЉЪе∞ПйЉ†жО•зІНзЦЂиЛЧеРОзЪДеЕНзЦЂињЗз®ЛињљиЄ™ жКЧдљУеПНеЇФеТМдњЭжК§дљЬзФ® дљЬиАЕеѓєе∞ПйЉ†зЪДжКЧдљУдЇІзФЯжГЕеЖµињЫи°МиѓДдЉ∞пЉИеЫЊ 3aпЉЙгАВзїУжЮЬжШЊз§ЇпЉМдЄОдЄ§еЙВжЄЄз¶ї R-CNPзЫЄжѓФпЉМеНХеЙВ R-CNP@MиГљжЫіењЂгАБжЫіеЉЇеЬ∞жПРйЂШи°АжЄЕдЄ≠ RBD зЙєеЉВжАІ IgMгАБIgGгАБIgG1 еТМ IgG2a зЪДжКЧдљУжїіеЇ¶пЉМиАМ CNP зїДеИЩж£АжµЛдЄНеИ∞ RBD зЙєеЉВжАІжКЧдљУпЉИеЫЊ 3bпЉЙгАВеАЉеЊЧж≥®жДПзЪДжШѓпЉМеЬ®12дЄ™жЬИзЪДжЧґйЧійЗМпЉМR-CNP@MзЪДжКЧRBDжКЧдљУжїіеЇ¶дњЭжМБеЬ®зЫЄеѓєиЊГйЂШзЪДж∞іеє≥пЉМињЩеПѓиГљдЄОйЩНиІ£еЊЃиГґеЫКжМБзї≠дЊЫеЇФеЕНзЦЂеОЯжАІR-CNPsжЬЙеЕ≥гАВйАЪињЗеѓєиВЇжЈЛеЈізїЖиГЮBзїЖиГЮеПЧдљУ(BCR)жµЛеЇПжХ∞жНЃжШЊз§ЇеЗЇйЂШж∞іеє≥зЪДзІНз≥їеИЖеМЦпЉМињЫдЄАж≠•и°®жШОињЩзІНйХњжЬЯжКЧдљУеЇФз≠ФдЉЉдєОжЬЙжЬЫйАЪињЗеК†йАЯдЇ≤еТМжИРзЖЯжЭ•жПРйЂШжКЧдљУиі®йЗПпЉИи°•еЕЕжХ∞жНЃеЫЊ6d-j)гАВ
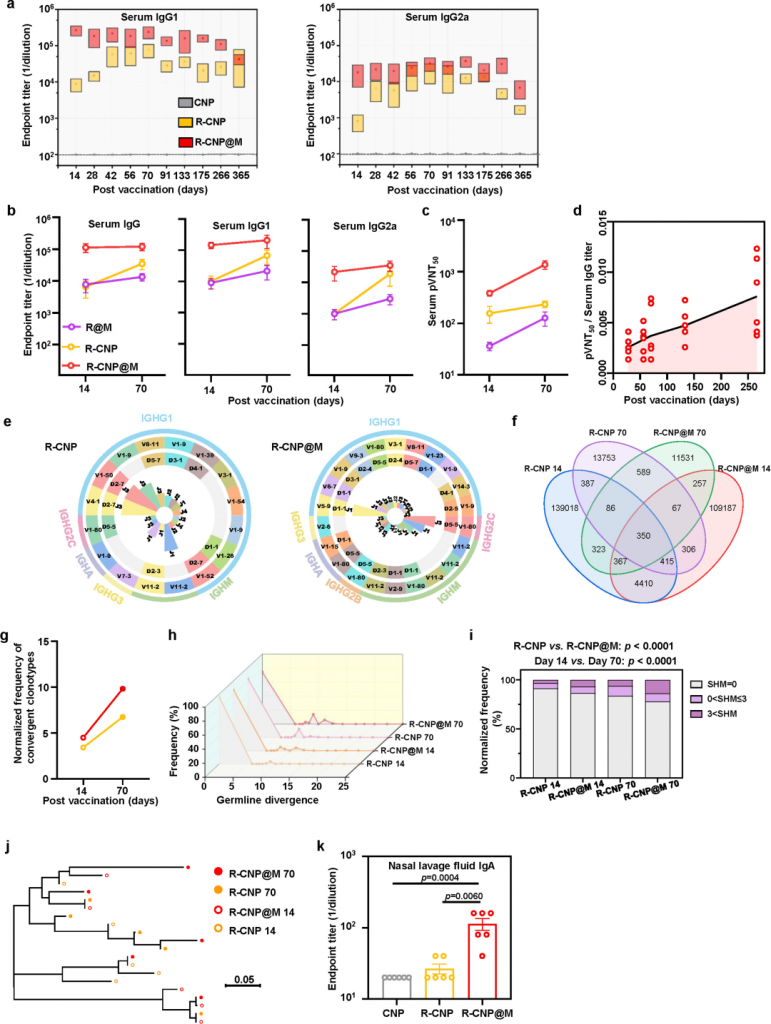
(a) ELISAжµЛеЃЪи°АжЄЕIgG1еТМIgG2aеЬ®зђђ14гАБ28гАБ42гАБ56гАБ70гАБ91гАБ133гАБ175гАБ266еТМ365姩зЪДзїИзВєжїіеЇ¶гАВ(b)зђђ14姩еТМзђђ70姩ELISAж£АжµЛи°АжЄЕIgGгАБIgG1еТМIgG2aзЪДзїИзВєжїіеЇ¶гАВ(c)и°АжЄЕpVNT50жµЛеЃЪпЉМеИЖеИЂдЇОзђђ14姩еТМзђђ70姩еПЦж†ЈгАВ(d)зђђ28姩гАБзђђ56姩гАБзђђ70姩гАБзђђ133姩гАБзђђ266姩гАБзђђ365姩R-CNP@Mи°АжЄЕжКЧдљУиі®йЗПеИЖжЮР(дї•pVNT50/и°АжЄЕIgGжїіеЇ¶жѓФеАЉи°®з§Ї)гАВе∞ЖеРДжЧґйЧізВєзЪДеЭЗеАЉињЮжО•иµЈжЭ•гАВ(e)зђђ70姩R-CNPзїДеТМR-CNP@MзїДиВЇBCRеЇУдЄ≠IGHC/V/D/JеЯЇеЫ†(йҐСзОЗ> 0.005)дљњзФ®еТМйЕНеѓєзЪДзЫЄеѓєиЃ°жХ∞гАВR-CNP@MзїДжШЊз§ЇеЗЇжЫіе§ЪзЪДйЂШйҐСIGH CDR3йЕНеѓєз±їеЮЛеТМжЫіе§ЪзЪДIGHGеТМIGHAиљђељХжЬђгАВ(f)жЙАеИЧеЫЫзїДдєЛйЧізЪДзїіжБ©еЫЊгАВR-CNPзїДеЬ®зЦЂиЛЧжО•зІНеРО14姩(dpv)дЄО70дЄ™dpvж†ЈжЬђдєЛйЧіжЬЙ1238дЄ™иґЛеРМеЕЛйЪЖеЮЛпЉМR-CNP@MзїДеЬ®14姩(dpv)дЄО70дЄ™dpvж†ЈжЬђдєЛйЧіжЬЙ1041дЄ™иґЛеРМеЕЛйЪЖеЮЛпЉМ4дЄ™ж†ЈжЬђдЄ≠жЬЙ350дЄ™иґЛеРМеЕЛйЪЖеЮЛгАВ(g) 4дЄ™ж†ЈжЬђдЄ≠R-CNPзЙєеЉВжАІеЕЛйЪЖеЮЛзЪДељТдЄАеМЦйҐСзОЗгАВ4дЄ™ж†ЈжЬђзЪДиґЛеРМеЕЛйЪЖеЮЛ襀еЃЪдєЙдЄЇR-CNPзЙєеЉВжАІеЕЛйЪЖгАВ(h) R-CNPзЙєеЉВжАІеЕЛйЪЖCDR3йЗНйУЊеПШйЗП(VH)еЯЇеЫ†зІНз≥їеИЖеМЦеИЖеЄГгАВ(i) R-CNPзЙєеЉВжАІеЕЛйЪЖдљУзїЖиГЮиґЕз™БеПШ(SHM)зЪДзїЯиЃ°еИЖжЮРгАВ(j)еЙН5дЄ™жФґжХЫеЕЛйЪЖеЇПеИЧзЪДи∞±з≥їж†СгАВйАЙеПЦжѓПдЄ™ж†ЈжЬђдЄ≠R-CNPзЙєеЉВжАІеЕЛйЪЖеЮЛдЄ≠жОТеРНеЙН5зЪДеЕЛйЪЖеЮЛпЉМеИ©зФ®MEGA 11.0иљѓдїґйЗЗзФ®Neighbor-joiningзїЯиЃ°жЦєж≥ХињЫи°МеИЖжЮРгАВ(k)зђђ70姩зФ®ELISAж≥ХжµЛеЃЪйЉїзБМжіЧжґ≤IgAзЪДзїИзВєжїіеЇ¶гАВa-d, k (n = 6)дЄ≠зЪДжХ∞жНЃи°®з§ЇдЄЇеє≥еЭЗеАЉ¬±SEMгАВ(i)йЗЗзФ®еПМдЊІPearsonеН°жЦєж£Ай™МиЃ°зЃЧжШЊиСЧжАІпЉМ(k)йЗЗзФ®е§ЪйЗНжѓФиЊГзЪДKruskal-Wallisж£Ай™МгАВ жО•зІН R-CNP@M зЦЂиЛЧзЪДе∞ПйЉ†жФѓж∞ФзЃ°иВЇж≥°зБМжіЧжґ≤пЉИBALFпЉЙдЄ≠зЪД RBD зЙєеЉВжАІ IgA еТМ IgG ж∞іеє≥йЂШдЇОжО•зІН R-CNP зЦЂиЛЧзЪДе∞ПйЉ†пЉМиАМ CNP зїДе∞ПйЉ†зЪД BALF дЄ≠жЬ™ж£АжµЛеИ∞ RBD зЙєеЉВжАІ IgA жИЦ IgGпЉИеЫЊ 3cпЉЙгАВ дљЬиАЕињШиѓДдЉ∞дЇЖ R-CNP@M зЦЂиЛЧеЬ®дїУйЉ†дЄ≠зЪДи°®зО∞гАВзЃАиАМи®АдєЛпЉМдїУйЉ†йАЪињЗ DPI жО•зІН R-CNP@MпЉЙеРОпЉМйЂШжКЧ RBD IgG жїіеЇ¶пЉИеЫЊ 3gпЉЙдї•еПКи°АжЄЕеТМ BALF дЄ≠зЪДйЂШ SARS-CoV-2 дЄ≠еТМжїіеЇ¶пЉИеЫЊ 3hпЉЙеЕ±еРМжФѓжМБдЇЖеЕ®иЇЂеТМз≤ШиЖЬеЕНзЦЂзЪДеїЇзЂЛгАВи°•еЕЕжХ∞жНЃеЫЊ6 е∞ПйЉ†жКЧдљУеПНеЇФзЪДйЩДеК†иѓДдїЈ
еЫЊ3пЉЪе∞ПйЉ†еТМдїУйЉ†дЄ≠R-CNP@MеѓєSARS-CoV-2зЪДеЕНзЦЂе≠¶иѓДдЉ∞ йЭЮдЇЇзБµйХњз±їеК®зЙ©зЪДеЕНзЦЂеПНеЇФ дЄЇдЇЖдљњзЦЂиЛЧжЫіжО•ињСдЄіеЇКпЉМдљЬиАЕзФ®йЭЮдЇЇзБµйХњз±їеК®зЙ©ињЫи°МдЇЖеЃЮй™МпЉИеЫЊ 4aпЉЙгАВдЄАеП™дљњзФ®е∞ЉзљЧж≤≥зЇҐж†ЗиЃ∞зЦЂиЛЧзЪДзМіе≠РеЬ®зђђ 14 姩襀еЃЙдєРж≠їпЉМдљЬиАЕжФґйЫЖдЇЖеЃГзЪДиВЇйГ®ињЫи°МеЖЈеЖїзїДзїЗеИЗзЙЗеТМжИРеГПгАВR-CNP@M йҐЧз≤Те§ІйГ®еИЖж≤ЙзІѓеЬ®иВЇж≥°дЄ≠пЉМеП™жЬЙе∞СйЗПеЊЃеЫКжШОжШЊе≠ШеЬ®дЇОж∞ФзЃ°еТМжФѓж∞ФзЃ°дЄ≠пЉИеЫЊ 4bпЉМcпЉЙгАВеЬ®й™МиѓБдЇЖзЦЂиЛЧеЬ®йЭЮдЇЇзБµйХњз±їеК®зЙ©дЄ≠зЪДеЃЙеЕ®жАІеРОпЉМдљЬиАЕз†Фз©ґдЇЖйТИеѓє SARS-CoV-2 зЪДеЕ®иЇЂеТМз≤ШиЖЬеПНеЇФгАВеЬ®и°АжЄЕе≠¶жКЧдљУеПНеЇФжЦєйЭҐпЉМжКЧ RBD IgG жїіеЇ¶еЬ®зђђ 84 姩дїНе§ІдЇО 104пЉМжКЧдљУиі®йЗПйЂШдЇОзђђ 14 姩пЉИеЫЊ 4d,eпЉЙгАВеЕ≥дЇО BALF дЄ≠зЪДжКЧдљУеПНеЇФпЉМR-CNP@M зїДдєЯж£АжµЛеИ∞дЇЖйЂШжїіеЇ¶зЪД RBD зЙєеЉВжАІ IgA еТМ IgGпЉИеЫЊ 4fпЉЙгАВеАЉеЊЧж≥®жДПзЪДжШѓпЉМи°АжЄЕеТМ BALF ж†ЈжЬђеѓєдЉ™еЮЛзЧЕжѓТеТМжіїзЧЕжѓТйГљи°®зО∞еЗЇиЙѓе•љзЪДжКµжКЧиГљеКЫпЉИеЫЊ 4gгАБhпЉЙпЉМињЩињЫдЄАж≠•иѓБеЃЮдЇЖ R-CNP@M зЦЂиЛЧеЬ®жЬЙжХИжКµеЊ° SARS-CoV-2жМСжИШжЦєйЭҐзЪДдїЈеАЉгАВ
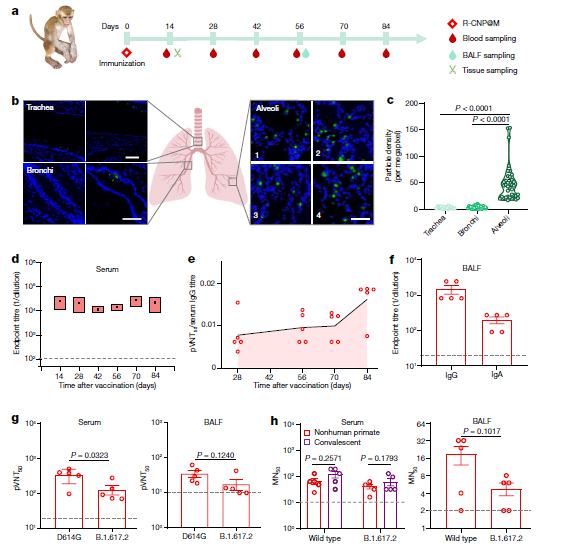
еЫЊ4пЉЪR-CNP@MеЬ®й£ЯиЯєзМідЄ≠зЪДи°®зО∞ ињ≠дї£дї•иОЈеЊЧжЫіеєњж≥ЫзЪДеЕНзЦЂеКЫ йЙідЇОCNP еЇХзЫШеПѓдї•жШЊз§ЇзФ®жИЈйАЙжЛ©зЪДжКЧеОЯпЉМдљЬиАЕжΥ糥дЇЖеЕ±еРМжШЊз§ЇйЗОзФЯеЮЛ RBDпЉИRWTпЉЙеТМ Omicron RBDпЉИROпЉЙзЪДеПѓиГљжАІпЉМдї•еЇФеѓєдЄ§зІНеЕ±еЊ™зОѓиПМ憙жГЕеЖµдЄЛзЪДжМСжИШгАВдљЬиАЕеЬ®иЗ™жДИжАІеЊЃиГґеЫКпЉИRWTRO-CNP@MпЉЙдЄ≠и£ЕеЕ•дЇЖзФ±ж≠§дЇІзФЯзЪДйХґеµМеЮЛ RWTRO-CNPпЉЫеєґеИґе§ЗдЇЖ RWT-CNP@M еТМ RO-CNP@M дї•ињЫи°МжѓФиЊГпЉИеЫЊ 5aпЉЙгАВеЬ®еНХеЙВйЗПеє≤з≤Йж∞ФжЇґиГґж≥®е∞ДпЉИ10 ¬µg з≠ЙжХИ RBDпЉЙињЩдЄЙзІНзЦЂиЛЧеРОзЪДзђђ 28 姩иѓДдЉ∞дЇЖе∞ПйЉ†зЪДйҐДйШ≤жАІжКЧдљУгАВ RWTRO-CNP@M зЦЂиЛЧеѓєйЗОзФЯеЮЛжѓТ憙еТМ Omicron еПШеЉВ憙зЪДдЉ™зЧЕжѓТдЄ≠еТМжХИжЮЬиЙѓе•љпЉМиАМзФ® RWT-CNP@M жИЦ RO-CNP@M еЕНзЦЂзЪДе∞ПйЉ†и°АжЄЕдЄНиГљдЄ≠еТМжЬ™йЕНеѓєжѓТ憙зЪДдЉ™еЮЛзЧЕжѓТгАВеѓєдЇО BALF ж†ЈжЬђпЉМIgA еТМ IgG жїіеЇ¶дєЯиІВеѓЯеИ∞з±їдЉЉзЪДзїУжЮЬпЉМRWTRO-CNP@M зїДиГљжЬЙжХИдЄ≠еТМдЄ§зІНжѓТ憙зЪДдЉ™зЧЕжѓТпЉМиАМ RWT-CNP@M зїДеТМ RO-CNP@M зїДеИЩдЄНиГљпЉИеЫЊ 5dгАБeпЉЙгАВеЫ†ж≠§пЉМжКЧеОЯ-CNP@M зЪДй©ђиµЫеЕЛињ≠дї£иЃЊиЃ°еПѓдї•жЙ©е§ІжКЧеОЯиѓ±еѓЉжКЧдљУеПНеЇФзЪДеєњеЇ¶пЉМињЩе∞ЖжЬЙеК©дЇОзЃ°зРЖжЬ™жЭ•е§ЪзІНеПШдљУеЕ±еЊ™зОѓзЪДжГЕеЖµгАВ дЄЇдЇЖжПРдЊЫдЄКињ∞жХ∞жНЃжЫіжЄЕжЩ∞зЪДеПѓиІЖеМЦпЉМдљЬиАЕињЫи°МдЇЖдЄїжИРеИЖеИЖжЮРгАВж†єжНЃжКЧдљУеПНеЇФжАІгАБж†ЈжЬђжЭ•жЇРгАБж£АжµЛжЦєж≥ХгАБжКЧдљУз±їеЮЛз≠ЙжХ∞жНЃзЙєеЊБпЉМеѓє10й°єеЕНзЦЂе≠¶жМЗж†ЗињЫи°МйЩНзїіе§ДзРЖеРОпЉМе∞ЖдЄЙзїДзЦЂиЛЧзЪДжХ∞жНЃжЄЕжЩ∞еЬ∞еИТеИЖдЄЇдЄНеРМзЪДз∞З(еЫЊ5f)гАВеПѓиІЖеМЦзГ≠еЫЊжШЊз§ЇпЉМRWT-CNP@MеТМRO-CNP@MзЦЂиЛЧжШЊз§ЇеЗЇйЭЮеЄЄдљОзЪД憙дЄНеМєйЕНеЕНзЦЂжМЗж†Зж∞іеє≥пЉМиАМй©ђиµЫеЕЛRWTRO-CNP@MзЦЂиЛЧзЪДе§Іе§ЪжХ∞еЕНзЦЂжМЗж†ЗзЪДеИЖжХ∞жШЊз§ЇеЬ®йЗОзФЯеЮЛиПМ憙еТМOmicronеПШдљУйГљеЊИйЂШ(еЫЊ5g)еАЉеЊЧж≥®жДПзЪДжШѓпЉМй¶Цжђ°жО•зІНRWTRO-CNP@MеТМеК†еЉЇжО•зІНRWTRO-CNP@MдєЯдЉЪеѓЉиЗійЗОзФЯеЮЛеТМOmicronзЪДRBDзїУеРИжХИдїЈжЫійЂШгАВеЫ†ж≠§пЉМantigen-CNP@MиЃЊиЃ°зЪДй©ђиµЫеЕЛињ≠дї£еПѓдї•жЙ©е±ХжКЧеОЯиѓ±еѓЉжКЧдљУеПНеЇФзЪДеєњеЇ¶пЉМињЩеЇФиѓ•жЬЙеК©дЇОзЃ°зРЖжЬ™жЭ•е§ЪзІНеПШдљУеЕ±еЊ™зОѓзЪДжГЕеЖµгАВ еЃњдЄї-еЃњдЄїйЧідЉ†жТ≠зЪДзЫКе§Д зФ±дЇОеРЄеЕ•зЦЂиЛЧеПѓдї•еЬ®еСЉеРЄйБУиѓ±еѓЉеЉЇе§ІзЪДеЕНзЦЂеПНеЇФпЉМдљЬиАЕжΥ糥дЇЖеЃГеѓєеЃњдЄї-еЃњдЄїдЉ†жТ≠зЪДжљЬеЬ®зЫКе§ДгАВдљЬиАЕеЬ®е§ЪдЄ™дїУйЉ†дЉ†жТ≠ж®°еЮЛдЄ≠жµЛиѓХдЇЖеЕґжКЧOmicronдЉ†жТ≠зЪДжАІиГљ(еЫЊ5h)гАВ еЬ®з©Їж∞ФдЉ†жТ≠йШ≤жК§ж®°еЮЛдЄ≠пЉМдљЬиАЕиЃЊиЃ°дЇЖдЄАдЄ™зђЉеЉПйЪФжЭњпЉМеЕБиЃЄж∞ФжµБдЉ†жТ≠пЉМдљЖдЄНеЕБиЃЄзЫіжО•жО•иІ¶жИЦж±°жЯУзЙ©(еМЕжЛђй•Ѓй£ЯеТМеЇКдЄКзФ®еУБ)дЉ†жТ≠(еЫЊ5i)гАВдЄАеРНдЊЫдљУжО•зІНжіїзЪДOmicronиПМ憙пЉМеЬ®жДЯжЯУеРО24е∞ПжЧґе∞ЖеЕґеЉХеЕ•зђЉзЪДдЄАдЊІгАВдЄЙеРНеПЧиАЕеИЖеИЂжО•зІНPBSгАБеРЄеЕ•зЦЂиЛЧжИЦиВМиВЙж≥®е∞ДзЦЂиЛЧпЉМжФЊзљЃеЬ®еП¶дЄАдЊІ(дїОеПЧжДЯжЯУзЪДдїУйЉ†еРСдЄЛжµБеК®)гАВеЬ®жЪійЬ≤дЇОдЊЫдљУ24е∞ПжЧґеРОпЉМеРЄеЕ•зЦЂиЛЧзїДеЬ®3 dpeжЧґиВЇеЭЗиі®жґ≤дЄ≠зЪДRNAжЛЈиіЭжХ∞жЬАдљОпЉМTCID50еАЉжЬАдљО(еЫЊ5j,k)пЉМзЧЕзРЖиѓДеИЖжЬАдљО(еЗ†дєОж≤°жЬЙиВЇзїДзїЗзЧЕзРЖе≠¶зЧЕеПШ)(еЫЊ5l)гАВ еЬ®з©ЇдЄ≠дЉ†жТ≠йШїжЦ≠ж®°еЮЛдЄ≠пЉМдљЬиАЕдљњзФ®зЪДзђЉдЄОз©ЇдЄ≠дЉ†жТ≠йШ≤жК§еЃЮй™МдЄ≠зЪДзђЉзЫЄдЉЉ(еЫЊ5m)гАВжѓПеП™дЊЫдљУдїУйЉ†еЬ®жО•зІНжђІз±≥еЕЛйЪЖжіїиПМ憙еЙНеИЖеИЂжО•еПЧеРЄеЕ•зЦЂиЛЧгАБиВМеЖЕзЦЂиЛЧжИЦPBSж≤їзЦЧгАВжДЯжЯУ24е∞ПжЧґеРОпЉМе∞ЖињЩдЇЫдЊЫдљУдїУйЉ†еЉХеЕ•зђЉеИЖйЪФеЩ®зЪДдЄАдЊІпЉМеєґе∞ЖдЄ§еП™еПЧдљУдїУйЉ†(еєЉеєідїУйЉ†)зљЃдЇОжДЯжЯУдїУйЉ†зЪДдЄЛжЄЄгАВжЪійЬ≤24 hеРОеИЖеИЂй•≤еЕїпЉМ3 dеРОеЃЙдєРж≠їгАВжЪійЬ≤дЇОжО•зІНдЊЫдљУзЪДеПЧдљУдїУйЉ†йЉїеМАжµЖдЄ≠зЪДзЧЕжѓТиљљйЗПжШЊиСЧйЩНдљО(еЫЊ5n)гАВеАЉеЊЧж≥®жДПзЪДжШѓпЉМ12еРНжО•еПЧPBSж≤їзЦЧзЪДдЊЫиАЕдЄ≠жЬЙ11дЇЇжДЯжЯУпЉМ12еРНжО•еПЧиВМиВЙж≥®е∞ДзЦЂиЛЧеЕНзЦЂзЪДдЊЫиАЕдЄ≠жЬЙ8дЇЇжДЯжЯУпЉМдљЖ12еРНжО•еПЧеРЄеЕ•зЦЂиЛЧдЊЫиАЕдЄ≠еП™жЬЙ3дЇЇжДЯжЯУ(еЫЊ5 0,p)гАВињЩдЇЫзїУжЮЬжФѓжМБдЇЖињЩж†ЈдЄАзІНиІВзВєпЉМеН≥еРЄеЕ•зЦЂиЛЧеЬ®еСЉеРЄйБУдЄ≠иѓ±еѓЉзЪДеЉЇе§ІеЕНзЦЂеПНеЇФжЬЙеИ©дЇОеѓєжКЧOmicronеПШдљУзЪДеЃњдЄїдЉ†жТ≠пЉМињЩзІНиГљеКЫеЇФиѓ•еѓєзЃ°зРЖйЂШдЉ†жЯУжАІзЧЕжѓТжЬЙзФ®гАВ
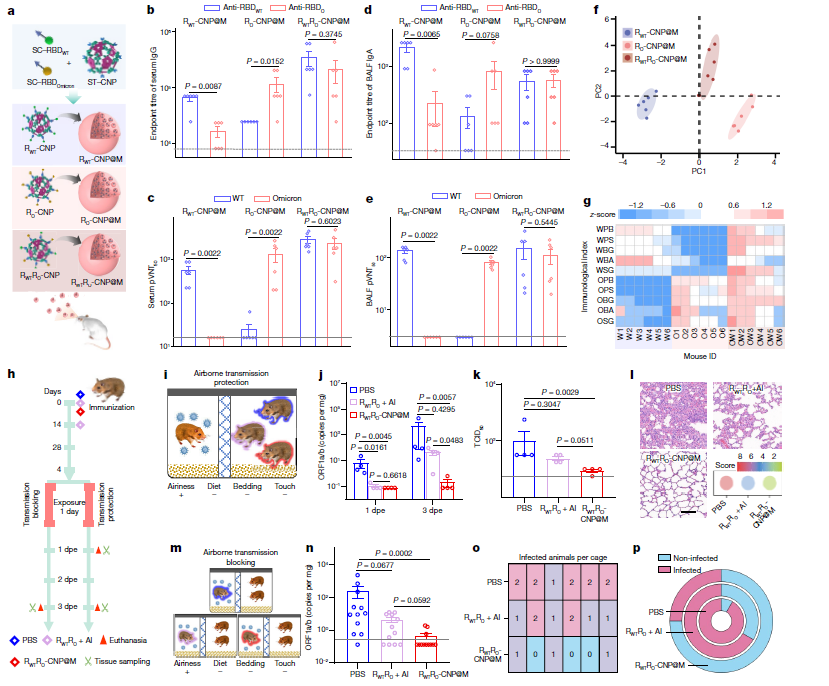
еЫЊ 5пЉЪйХґеµМ R-CNP@M зЪДеЕНзЦЂе≠¶иѓДдЉ∞еПКеЕґжКЧ SARS-CoV-2 дЉ†жТ≠зЪДжАІиГљ е∞ПзїУ жАїдєЛпЉМжЬђжЦЗеЉАеПСдЇЖдЄАзІНеПѓеРЄеЕ•гАБеНХеЙВйЗПгАБеє≤з≤Йж∞ФжЇґиГґ SARS-CoV-2 зЦЂиЛЧгАВеЊЃиГґеЫКеРИйАВзЪДз©Їж∞ФеК®еКЫе≠¶зЫіеЊДжЬЙеИ©дЇОеЬ®иВЇж≥°дЄ≠зЪДж≤ЙзІѓпЉМеєґдЄФйЗКжФЊзЪДзЇ≥з±≥зЇІ R-CNP еЊИеЃєжШУ襀 APC еЖЕеМЦгАВдљЬиАЕзЪДзЦЂиЛЧиѓ±еѓЉи°АжЄЕдЄ≠ IgG зЪДеЉЇеК≤йХњжЬЯдЇІзФЯеТМ BALF дЄ≠дЄ∞еѓМзЪД IgA зЪДдЇІзФЯпЉМеєґеѓєе∞ПйЉ†гАБдїУйЉ†еТМйЭЮдЇЇзБµйХњз±їеК®зЙ©дЇІзФЯжЬЙжХИзЪДдњЭжК§гАВйАЪињЗй©ђиµЫеЕЛињ≠дї£пЉМдљЬиАЕжИРеКЯеЬ∞жЙ©е±ХдЇЖи°АжЄЕеТМз≤Шжґ≤дЄ≠ RBD иѓ±еѓЉзЪДжКЧдљУеПНеЇФзЪДеєњеЇ¶гАВиАГиЩСеИ∞еЬ® CNP еЇХзЫШдЄКе±Хз§ЇжКЧеОЯзЪДзБµжіїжАІпЉМдљЬиАЕиЃЊжГ≥дљЬиАЕзЪДеРЄеЕ•зЦЂиЛЧеПѓдї•дљЬдЄЇеѓєжКЧ COVID-19 еТМеЕґдїЦеСЉеРЄйБУдЉ†жЯУзЧЕзЪДжЬЙеЙНйАФзЪДе§ЪдїЈеє≥еП∞гАВ еОЯжЦЗйУЊжО•пЉЪ https://www.nature.com/articles/s41586-023-06809-8
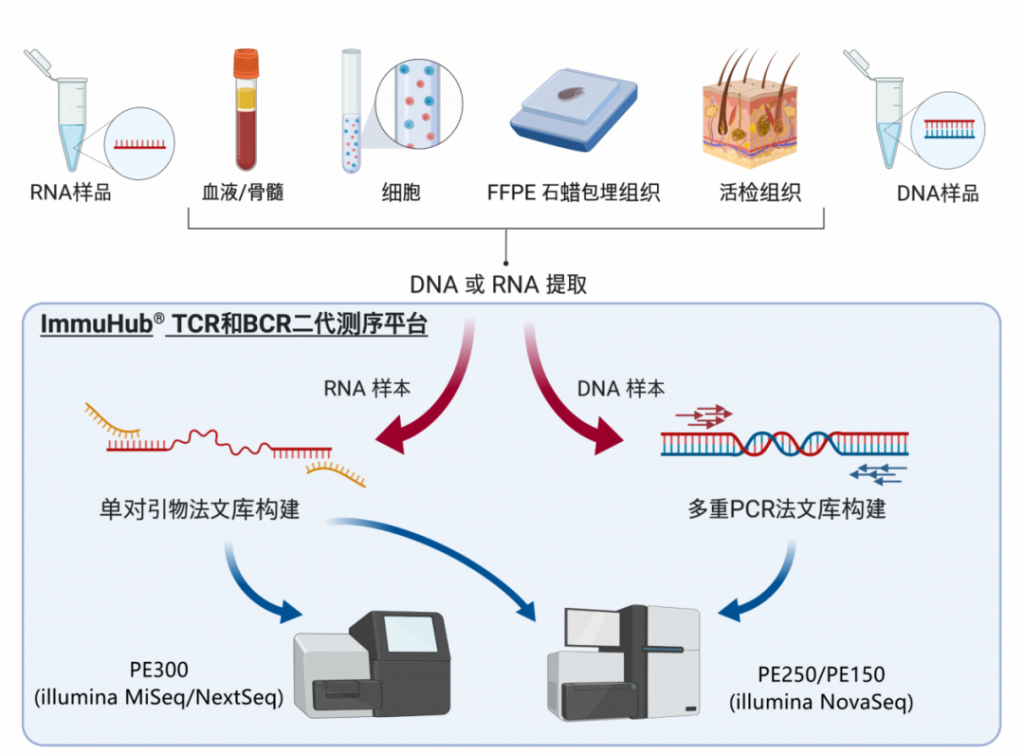
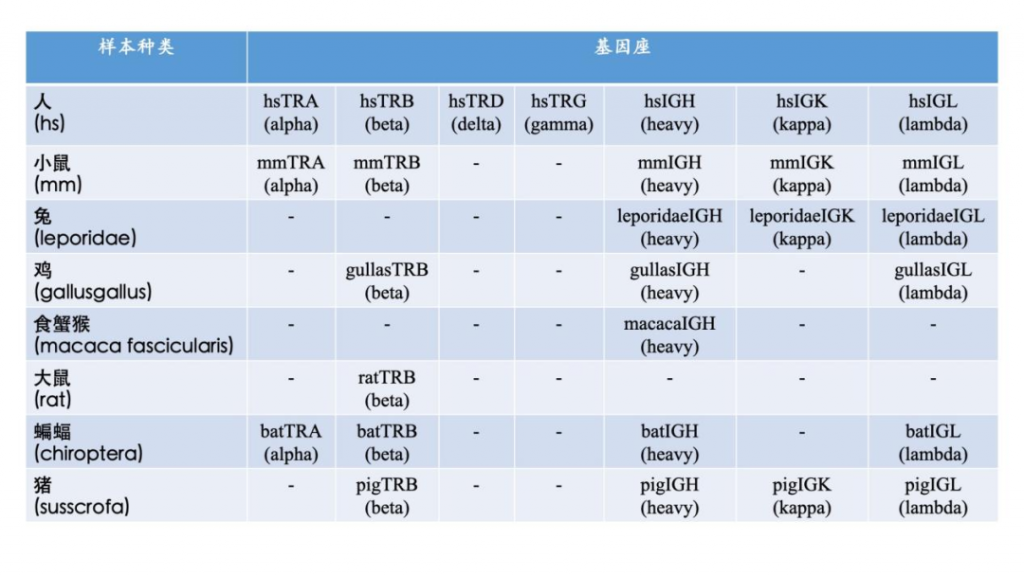
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РпЉИзЇ≥жЦѓиЊЊеЕЛдї£з†БпЉЪGTHпЉЙдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†|TзїЖиГЮеЕНзЦЂжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБTCR-TеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ
