
2024 EHA. Abstract#S205 题目:Ciltacabtagene autoleucel ± lenalidomide maintenance in newly diagnosed multiple myeloma with suboptimal response to frontline autologous stem cell transplant: Cartitude-2 cohort D背景及研究方法:Cartitude-2是一项2期多队列研究,D队列评估新诊断的多发性骨髓瘤(NDMM)患者Ciltacabtagene autoleucel(cilta-cel)±来那度胺维持治疗的疗效和安全性。17例患者在诱导化疗、自体干细胞移植(ASCT)±巩固治疗之后,接受了cilta-cel(联合来那度胺,n=12;未联合来那度胺,n=5)治疗,来那度胺维持治疗≥21天后cilta-cel治疗≤2年,主要终点是基于NGS或下一代流式的MRD阴性(cutoff为10-5)。研究结果:在15例MRD可评价患者中,12例(80%)达到MRD阴性(<10-5),至MRD阴性的中位时间为1个月(范围1-6)。总缓解率为94%(n=16/17),18个月时的无进展生存率和总生存率均为94%。结论:在ASCT一线治疗后达不到完全缓解的NDMM患者中,单次cilta-cel输注±来那度胺维持治疗显示出持久的深度反应,具有良好的疗效和安全性。 2024 EHA. Abstract#S203 题目:Randomized phase 3 study of isatuximab (isa) plus lenalidomide and dexamethasone (rd) with bortezomib (v) versus isard in patients with newly diagnosed transplant ineligible multiple myeloma (NDMM TI)背景及研究方法:CD38靶向免疫疗法已获批与来那度胺和地塞米松(Rd)联合治疗不符合移植条件(TI)的NDMM,并被视为当前的标准治疗(SOC)。在BENEFIT/IFM 2020-05研究(NCT 04751877)中,作者研究了伊沙妥昔单抗(isa)+来那度胺和地塞米松(rd)+硼替佐米(v)(IsaVRd)在NDMM TI中的疗效和安全性。主要终点是治疗开始后18个月时的NGS MRD阴性率(<10-5),次要终点包括生存时间(OS、PFS、EFS、TTNT)、缓解率和持续时间、MRD终点和安全性。研究结果:招募了270例患者(每组135例),各组患者的基线特征均衡。与IsaRd组相比,Isa-VRd组在18个月时的MRD阴性率显著更高(47% vs 24%),各亚组的MRD获益一致。在21.2个月的中位随访时,33例(12%)患者复发,20例(7%)患者死亡,但各组间未观察到显著差异。结论:与IsaRd相比,Isa-VRd显著加深了反应,MRD阴性率(10-5)显著增加。本研究支持将Isa-VRd作为NDMM TI非虚弱患者的新护理标准。 2024 EHA. Abstract#S201 题目:Daratumumab+bortezomib /lenalidomide / dexamethasone in transplant-eligible patients with newly diagnosed multiple myeloma: analysis of minimal residual disease in the perseus trial 背景及研究方法:在3期PERSEUS研究中,分析了在符合移植条件(TE)的NDMM患者中,与VRd诱导/巩固后R维持治疗相比,Daratumumab+VRd(D-VRd)诱导/巩固治疗后D-R维持治疗的疗效。NDMM TE患者以1:1的比例随机分配至D-VRd或VRd组,采用NGS技术检测MRD,评估MRD阴性率(10-5或10-6)。 研究结果:MRD阴性率随时间推移增加,在第1周期第1天后12、24和36个月,D-VRd组的MRD阴性率均高于VRd组(均P <0.0001)。D-VRd组MRD持续阴性≥ 12个月的发生率高于VRd组(cutoff为10-5时:64.8% vs 29.7%; cutoff为10-6时:47.3% vs 18.6%)。在巩固治疗结束时MRD阳性的患者中,维持治疗期间MRD阴性率D-VRd组患者比例显著高于VRd组(10-5:68.8%对52.7%;10-6:62.3%vs31.0%),维持期间MRD持续阴性≥12个月的发生率D-VRd组显著高于VRd组(10-5:44.2%vs22.6%;10-6:34.4%vs12.7%)。在巩固治疗和总体研究结束时10-5和10-6的MRD阴性与PFS改善相关。 结论:与VRd诱导/巩固后再进行R维持治疗相比,D-VRd诱导/巩固后再进行D-R维持治疗的MRD阴性持续性和深度更好,从而在改善PFS方面更有临床意义。 2024 EHA. Abstract#P2059 题目:Minimal residual disease (MRD), pharmacokinetic (pk), and pharmacodynamic (pd) assessment of epcoritamab 2- vs 3-step step-up dosing in patients with relapsed/refractory follicular lymphoma (R/R FL)背景及研究方法:Epcoritamab治疗复发/难治性(R/R)滤泡性淋巴瘤(FL)患者的EPCORE™ NHL1试验(I/II期;NCT03625037)中,使用两步阶梯给药(SUD)方案,实现了82%的总缓解率和63%的完全缓解率,安全性可控,细胞因子释放综合征(CRS)事件主要为低级别。然而,进一步降低CRS的发生率可能会提高epcoritamab在R/R FL治疗中的可及性。因此在R/R FL患者中评估C1周期 2步SUD方案与C1 3步优化方案(C1 OPT)的效果。使用NGS MRD方法,首先对肿瘤活检组织进行检测,鉴定肿瘤克隆,然后对在预先指定时间点收集的外周血单核细胞进行MRD追踪监测。按照Lugano标准评估总体缓解率和无进展生存期(PFS)。研究结果:两步SUD队列在第15天(C1D15)首次全剂量给药后24小时,IL-6水平中位数显著升高,而C1 OPT队列在C1及之后显示较低的IL-6水平,支持C1 OPT队列中CRS的减少。2步SUD队列的MRD阴性率为67%(61/91),C1 OPT队列的MRD阴性率为64%(28/44),无明显差异。结论:3步SUD(C1 OPT)和2步SUD方案的MRD阴性率接近,但C1 OPT方案IL-6水平显著降低,这对于降低CRS发生风险具有价值。 2024 EHA. Abstract#S234 题目:Epcoritamab induces deep responses in relapsed or refractory (r/r) follicular lymphoma (fl): safety and pooled efficacy data from epcore nhl-1 pivotal and cycle (c) 1 optimization (opt) fl cohorts背景及研究方法:在EPCORE™NHL1关键队列中,epcoritamab治疗在R/R FL患者中产生了深度、持久的缓解。在C1 OPT队列中研究CRS增强缓解策略的效果和安全性。主要终点为任何级别和G≥2 CRS事件的发生率,次要终点包括缓解率、外周血MRD(NGS,10−6cutoff)和安全性/耐受性。研究结果:C1 OPT队列中有86例R/R FL患者接受了epcoritamab治疗,92%为III-IV期FL,63%为双重难治性疾病,44%为原发性难治性疾病,42%为POD 24。总缓解率(ORR)为84%,CR率为65%(图A)。在NHL1关键队列和C1 OPT队列的135例MRD可评估患者中,89例患者(66%)实现MRD阴性,总体的和C3D1(预定时间点)的MRD阴性率均与PFS改善相关(图B)。欧洲血液学会(EHA)年会作为欧洲血液学领域规模最大的国际会议,每年都吸引着来自世界各地的专家学者,一起分享并探讨有关血液学的创新理念及最新的科学和临床研究成果。在今年的EHA年会上,报告了多篇二代测序(NGS)技术在淋系血液肿瘤微小残留病(MRD)检测中的最新研究成果,覆盖多发性骨髓瘤、急慢性淋巴细胞白血病、淋巴瘤等多个病种。这说明NGS MRD技术已在全球范围内得到广泛应用,尤其是在药物临床试验中担当重要角色。下面跟随小编来了解EHA2024大会上发表的NGS MRD技术的最新研究成果吧!

结论:epcoritamab单药治疗在接受Tcell-engaging治疗的最大的R/R FL人群中显示了早期、深刻的缓解。CR和MRD阴性与PFS的改善相关。C1 OPT显著降低了CRS率和严重程度,很少有G2和G≥3事件。这表明,强制住院进行CRS监测是不必要的,可以门诊进行监测和评估。 2024 EHA. Abstract# P1137 题目:Minimal Residual Disease (MRD) Status Predicts Outcomes in Patients with Follicular Lymphoma (FL) Treated with Chemo-Immunotherapy on SWOG S0016背景及研究方法:SWOG S 0016是一项III期随机研究,比较了R-CHOP(利妥昔单抗、环磷酰胺、多柔比星、长春新碱、泼尼松)与CHOP-RIT(CHOP + I133-tositumomab)的安全性和有效性。这里通过NGS MRD分析预测了入组SWOG S0016临床试验的晚期FL患者的前瞻性队列的结局。531例既往未经治疗的晚期FL患者任何病理级别的(巨大II期、III-IV期)被随机分配接受6个周期的R-CHOP或CHOP-RIT。采用NGS对肿瘤活检组织进行癌细胞克隆鉴定,然后对一年的骨髓样本进行MRD评估。基线显著性克隆定义为≥10个基因组数量(ENG),频率≥5%。MRD阳性状态(MRDp)定义为患者的治疗后样本文库中的最小汉明距离(HD)≤6,并且保留了预先存在的SHM(如果HD>0)。无法检测到的MRD(MRDu,<10-4)定义为在深度>10000ENG的治疗后文库中CDR3 HD>6。研究结果:在具有可追踪克隆的116名患者中,83名是MRDu,33名是MRDp。MRDp和MRDu患者的基线特征相似,但MRDp患者更可能表现出FL的形态学基线骨髓受累(82% vs. 55%)。MRDu患者和MRDp患者的5年PFS估计值分别为72%和30%(如下图),10年PFS分别为56%和17%,5年OS没有差异。MRDu患者的最佳总体缓解率显著高于MRDp患者(96% vs 79%,p=0.005)。无论MRD状态如何,接受CHOP-RIT的患者的PFS均更好,而OS无统计学差异。
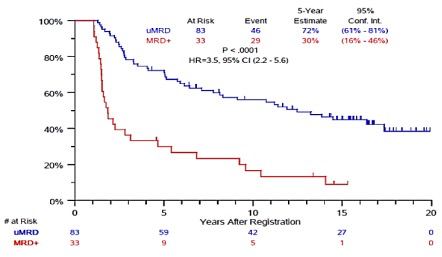
结论:该研究首次证明,MRDu状态预测了接受化疗免疫治疗的FL患者的5年和10年PFS的改善。1年时间点骨髓中的MRD+状态与POD24相关。NGS的MRD评估是一种很有前途的预后工具。 2024 EHA. Abstract#S118 题目:Comprehensive next generation sequencing-based profiling of immunoglobulin (ig) and t-cell receptor (tr) rearrangements in all identifies clonal evolution and age-related patterns背景及研究方法:利用IG/TR NGS数据,作者全面分析了儿童和成人ALL诊断中的重排情况,重点关注显著性重排计数和类别、克隆进化(ClEvo)模式和机制。并进一步探讨了与年龄和免疫表型的相关性,以确定潜在的临床生物学关联。在1212名ALL患者(573名儿童患者,639名成人患者)队列使用NGS检测试剂盒进行了常规IG/TR标记筛查。为了增强该方法在区分白血病相关重排中的特异性,实施了一种新的标记评估算法Marksman,其结合克隆丰度和生理背景分布。研究结果:与成人患者相比,儿童ALL患者具有更多IG/TR标志物(图A),只有0.4%的儿童患者与6%的成人患者没有标志物。55%的儿童B-ALL病例显示终末期IGK-KDE重排,只有23%的成人B-ALL携带这种重排。IGH ClEvo在44%的儿童和23%的成人B-ALL中被观察到,在Pro-B病例中具有明显的活性(75%的儿童,57%的成人)。根据已发表的数据(Darzentas,Hemasphere 2023),作者证实了VtoDJ机制驱动了pro-B的进化(80%),而V-replacement主导了其他亚型的进化。此外,与成人(14%)相比,TRB ClEvo在儿童B-ALL(52%)中更常见,而在T-ALL中的频率更低(13%儿童,6%成人)。作者进一步检查了B-ALL样本中扩增的生理T细胞克隆(Kelm,Hemasphere 2023)(丰度≥5%的生产性TRD-VJ或TRB-VJ1重排)的存在,并显示检出率随年龄增加而增加(图B)。
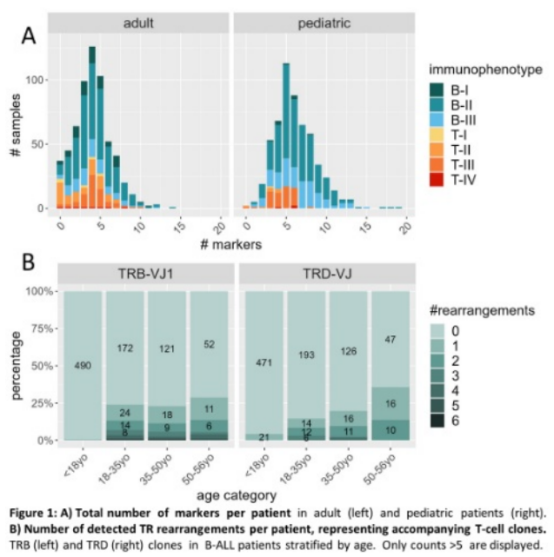
结论:这项基于NGS的研究为所有亚型和年龄组的IG/TR重排模式提供了前所未有的特征。儿童B-ALL较高的免疫遗传成熟度与儿童期该疾病较好的预后一致。NGS有助于检测ALL样本中的ClEvo,这是一种在不成熟的B-ALL免疫表型和儿科患者中最普遍的现象,IG重排似乎比TR重排更频繁地驱动ClEvo。这一发现具有显著的临床相关性,因为ClEvo可能导致MRD标志物丢失,从而导致随访期间的假MRD阴性。另外作者发现在老年患者中,扩增的生理性T细胞克隆的比率较高,这突出表明需要谨慎避免将生理性重排误解为MRD标志物,特别是在成年人群中。 2024 EHA. Abstract#S164 题目:Combined pirtobrutinib, venetoclax, and obinutuzumab in first-line treatment of patients with chronic lymphocytic leukemia (cll): a phase 2 trial背景及研究方法:既往研究报告了在CLL患者中,联合使用共价BTK抑制剂(cBTKi)和BCL 2抑制剂venetoclax +/-CD 20单克隆抗体obinutuzumab的治疗时,检测不到的MRD(U-MRD)缓解率较高。在这里作者报告了非共价BTKi、pirtoclutinib、venetoclax和obinutuzumab联合治疗作为CLL患者一线治疗的研究结果(NCT 05536349)。入组40例从未治疗过的CLL患者接受对应的治疗,在C7和C13结束时,通过NGS技术评估外周血和骨髓中的MRD。所有患者在停止治疗后的前12个月内每3个月通过NGS进行一次外周血MRD监测,然后每6个月监测一次。主要终点是C7结束时的骨髓U-MRD率。研究结果:40例患者中75%IGHV未突变。在C7结束时,在达到该时间点的25例患者中,19/25例(76%)的骨髓NGS结果为U-MRD(<10-6),4/25例患者MRD ≥10-6但<10-4,2例患者MRD ≥10-4。C7结束时的外周血NGS MRD显示22/25(88%)为U-MRD(10-6),2例患者MRD ≥10-6但<10-4,1例患者MRD ≥10-4。结论:作者报告了一线联合pirtoclutinib、venetoclax和obinutuzumab治疗CLL患者的首次结果。在联合治疗6个月时,骨髓U-MRD(cutoff为10-6)的比例非常高。 艾沐蒽专注于免疫组二代测序领域多年,是全国首家推出血液肿瘤NGS MRD检测产品Seq-MRD®的公司。Seq-MRD®适用于B/T系白血病、B/T系淋巴瘤、多发性骨髓瘤,能够帮助临床医生预测长期疗效、评估治疗效果、监测缓解状态以及检测早期复发。经过多年的积累和发展,Seq-MRD®在临床检测和科学研究上均取得不少成果,并获得国际市场认可。 获得欧盟CE资质认证 获得三项发明专利 艾沐蒽推出的Seq-MRD®血液癌症MRD检测是最早批实现商业化的产品,自2016年研发专利技术至今,艾沐蒽Seq-MRD®已经获得3项国家发明专利:[1]“一种应用于高通量测序检测T细胞白血病微小残留病的引物组合及试剂盒”(专 利 号: 2016 11204857.0,授权公告号:CN 106957906 B)[2]“一种检测微小残留病MRD的试剂盒”(专 利 号: 2018 1 1550133.0,授权公告号: CN 109652518 B)[3]“一种检测微小残留病MRD的方法”(专 利 号: 2018 1 1549203.0,授权公告号: CN 109680062 B) 获得相关软件著作 [2]“Seq-MRD检测自动化分析系统(DiscTermite)[简称:DiscTermite]0.4.6“(登记号:2019SR1131517) [3]“基于免疫组库二代测序的微小残留病(MRD)检测数据处理系统”(登记号:2020SR0507594) 获得荣誉证书 艾沐蒽申报的“免疫组TCR/Ig高通量测序技术/血液肿瘤微小残留病(MRD)检测/Seq-MRD®”因其创新性、前沿性、市场实用性荣获“2022年度CCTB中国肿瘤标志物产业创新大会创新技术/产品评选”项目二等奖。 发表相关文献 Seq-MRD®发表相关文献1、Huang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H. Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. Bone Marrow Transplant. 2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.(点击链接可查看文章内容) 2、Chen H, Gu M, Liang J, Song H, Zhang J, Xu W, Zhao F, Shen D, Shen H, Liao C, Tang Y, Xu X. Minimal residual disease detection by next-generation sequencing of different immunoglobulin gene rearrangements in pediatric B-ALL. Nat Commun. 2023 Nov 17;14(1):7468. doi: 10.1038/s41467-023-43171-9. (点击链接可查看文章内容) 3、Min’er Gu,Yahong Xia, Jingying Zhang, Yongmin Tang, Weiqun Xu, Hua Song Xiaojun Xu. The effectiveness of blinatumomab in clearing measurable residual disease in pediatric B-cell acute lymphoblastic leukemia patients detected by next-generation sequencing. Cancer Med. 2023 Dec;12(24):21978-21984. doi:10.1002/cam4.6771. (点击链接可查看文章内容) 获得国际市场认可 杭州艾沐蒽生物科技有限公司成立于2016年,是国际前沿的专注于免疫驱动医学技术的国家高新技术企业。创始人团队来自美国芝加哥大学,在2010年开始使用免疫组基因高通量测序技术开展各种疾病相关研究,于2016年通过自主研发,全国首家推出NGS-MRD血液肿瘤微小残留病(MRD)检测Seq-MRD®,并授权泛生子使用。同时,公司拥有Immun-Traq®肿瘤治疗伴随诊断、Immun-Cheq® |T细胞免疫测评以及ImmuHub®免疫组测序科研服务产品,并布局有基于AI机器学习算法的T-classifier®肿瘤早筛、单细胞测序、TCR-T和抗体发现等平台管线。目前为止发表了数十篇论文,其中包括:The New England Journal of Medicine(IF:158.5), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)等多篇高分杂志。公司构建几十项发明专利和软件著作权为核心的自主知识产权体系,为医院临床、生命科学研究、新药开发等提供解决方案和产品。艾沐蒽专注于通过解码适应性免疫系统来改变疾病的诊断和治疗,并致力于推进免疫驱动医学领域发展。4、Yan N, Wang ZL, Wang XJ, et,al. Measurable residual disease testing by next generation sequencing is more accurate compared with multiparameter flow cytometry in adults with B-cell acute lymphoblastic leukemia. Cancer Lett. 2024 Jul 4;598:217104. doi: 10.1016/j.canlet.2024.217104.
