¬† дљЬиАЕпЉЪKroopa Joshi ,Martina Milighetti and Benjamin
T зїЖиГЮеПЧдљУ (TCR) жµЛеЇПеЈ≤жИРдЄЇеИЖжЮРеЃњдЄї-иВњзШ§зЫЄдЇТдљЬвљ§зЪДвЉАй°єеЉЇвЉ§жЦ∞жКАжЬѓгАВ
NextGen жµЛеЇПжКАжЬѓзЪДињЫж≠•пЉМеК†дЄКеЉЇвЉ§зЪДжЦ∞еЮЛвљ£зЙ©дњ°жБѓе≠¶вЉѓеЕЈпЉМеПѓдї•еѓєиґКжЭ•иґКе§ЪзЪДеРДзІНеЃЮдљУзЩМжВ£иАЕзЪДиВњзШ§еТМвЊОжґ≤ж†ЈжЬђињЫвЊПеЃЪйЗПеТМеПѓйЗНе§НзЪДи°®еЊБгАВ
еЬ®ињЩзѓЗзїЉињ∞дЄ≠пЉМжИСдїђе∞ЖиАГиЩСе¶ВдљХдїОињЩдЇЫTCRеЇПеИЧдЄ≠жПРеПЦеЗЇзїЉеРИжМЗж†ЗпЉИиѓЄе¶ВTзїЖиГЮеЕЛйЪЖжАІеТМе§Ъж†ЈжАІпЉЙпЉМеєґзФ®дЇОжЈ±еЕ•дЇЖиІ£еЕНзЦЂж£АжЯ•зВєйШїжЦ≠зЪДдљЬзФ®жЬЇеИґгАВж≠§е§ЦпЉМжИСдїђињШжОҐиЃ®дЇЖTCRеЕ±дЇЂеЇПеИЧеИЖжЮРе¶ВдљХиГљеЄЃеК©еЃЪдєЙжКЧиВњзШ§еЕНзЦЂеПНеЇФзЪДз©ЇйЧіеТМжЧґйЧідЄКзЪДеЉВиі®жАІгАВ
жЬАеРОпЉМжИСдїђжАїзїУе¶ВдљХеИЖжЮРTCRзЪДеЇПеИЧеТМзїУжЮДгАВжЧ†иЃЇжШѓеНХдЄ™TCRињШжШѓдЄАз≥їеИЧзЫЄеЕ≥зЪДTCRжХ∞жНЃйЫЖпЉМйГљеПѓдї•зФ®жЭ•ж≥®йЗКжКЧеОЯзЙєеЉВжАІпЉМињЩеѓєеЉАеПСдЄ™жАІеМЦзЪДзїЖиГЮеЕНзЦЂзЦЧж≥ХеЕЈжЬЙйЗНи¶БжДПдєЙгАВ
TзїЖиГЮеПЧдљУ ( TCR ) жµЛеЇПжШѓдЄАзІНеПѓдї•и°®еЊБжКЧиВњзШ§еЕНзЦЂеПНеЇФзЪДжЈ±еЇ¶гАБеЉЇеЇ¶еТМеК®жАБзЫСжµЛзЪДеЉЇжЬЙеКЫзЪДеЈ•еЕЈгАВ
 
дЇМдї£ (NextGen) жµЛеЇПжКАжЬѓеТМзЫЄеЕ≥вљ£зЙ©дњ°жБѓе≠¶жµБз®ЛзЪДињЫж≠•жШЊзЭАжПРвЊЉдЇЖTCR еЇУз†Фз©ґзЪДзБµжХПеЇ¶гАБеЗЖз°ЃжАІеТМеЃЪйЗПйЩРпЉМдїОвљљдЇІвљ£дЇЖвЉ§йЗПзЪДеЗЇзЙИзЙ©еТМзЫЄеЕ≥жХ∞жНЃйЫЖгАВ
 
зДґвљљпЉМеЬ®дїОTCRеЇУзЪДйЭЩжАБењЂзЕІдЄ≠жО®жЦ≠еК®жАБеТМжКЧеОЯзЙєеЉВжАІжЦєйЭҐдїНзДґе≠ШеЬ®йЗНе§ІзЪДиЃ°зЃЧжМСжИШгАВ
 
еЬ®ињЩвЊ•жИСдїђеЫЮй°ЊдЇЖеЇФвљ§ TCR еЇУеИЖжЮРжЭ•иЈЯиЄ™еЃњдЄїеѓєеЕНзЦЂж≤їзЦЧж£АжЯ•зВєйШїжЦ≠зЪДеЕНзЦЂеПНеЇФжЦєйЭҐзЪДињЫе±ХгАВеЬ®дЄНжЦ≠еПШеМЦзЪДиВњзШ§еЊЃзОѓеҐГдЄ≠иЈЯиЄ™еПНеЇФзЪДжЉФеПШеТМеЉВиі®жАІпЉМеєґжП≠з§ЇTзїЖиГЮжКЧеОЯзЙєеЉВжАІгАВ
¬ЈT зїЖиГЮеЕЛйЪЖжАІеТМе§Ъж†ЈжАІдљЬдЄЇиѓДдЉ∞ TCR еѓєеЕНзЦЂж£АжЯ•зВєжКСеИґеЙВеПНеЇФзЪДжМЗж†З
еЫЊ1пЉЪT зїЖиГЮеЕЛйЪЖжАІеТМе§Ъж†ЈжАІ
TзїЖиГЮзФ±ељ©вЊКзРГдљУи°®вљ∞пЉМжѓПдЄ™TзїЖиГЮзЪДйҐЬвЊКдї£и°®еЕґеЕЛйЪЖеЮЛгАВеЬ®TзїЖиГЮеЕЛйЪЖжАІдљОзЪДиВњзШ§ж†ЈжЬђдЄ≠пЉМдїїдљХе§Ъж†ЈжАІйГљеЊИвЊЉпЉМе≠ШеЬ®иЃЄе§ЪеЕЈжЬЙдЄНеРМзЙєеЉВжАІзЪДTзїЖиГЮеЕЛйЪЖпЉМдљЖж≤°жЬЙвЉАдЄ™вЊЃеЄЄжЙ©еҐЮпЉИеЈ¶пЉЙгАВзЫЄвљРдєЛдЄЛпЉМеЬ®TзїЖиГЮеЕЛйЪЖжАІеҐЮеК†еТМTзїЖиГЮе§Ъж†ЈжАІдљОзЪДж†ЈжЬђдЄ≠пЉМдїЕж£АжµЛеИ∞е∞СжХ∞TзїЖиГЮеЕЛйЪЖеєґдЄФвЊЉеЇ¶жЙ©еҐЮпЉИеП≥пЉЙ
еЬ®ињЩзѓЗзїЉињ∞дЄ≠пЉМжИСдїђйЗНзВєеЕ≥ж≥®alpha еТМ beta TCRsгАВ
 
TCR еЯЇеЫ†жШѓеЬ® T зїЖиГЮеИЖеМЦињЗз®ЛдЄ≠йАЪињЗйЪПжЬЇеТМдЄНз≤Њз°ЃзЪДдљУзїЖиГЮйЗНзїДзЯ≠еРМжЇРеЯЇеЫ†зїДеЇПеИЧйЫЖ VгАБD еТМ J еЯЇеЫ†вљљдЇІвљ£зЪДгАВзФ±дЇОеПѓиГљжАІTCR alpha/beta еЉВвЉЖиБЪдљУзЪДжАїжХ∞жШѓеЈ®вЉ§зЪД[1] пЉМеРМвЉАеЇПеИЧеЊИе∞СеЬ®вЉАдЄ™дЄ™дљУдЄ≠дЇІвљ£дЄ§жђ°пЉМеЫ†ж≠§е§Ъжђ°иІВеѓЯеИ∞зЪДзЫЄеРМеЇПеИЧеЊИеПѓиГљжШѓйАЪињЗеНХдЄ™TзїЖиГЮеЕЛйЪЖзЪДйАЙжЛ©еТМеҐЮжЃЦеЊЧеИ∞зЪДгАВ
 
TCR еЇУзЪДжАїдљУеЕЛйЪЖжАІ[2] жШѓвЉАзІНжМЗж†ЗпЉМвљ§дЇОжНХиОЈеЬ®ж†ЈжЬђдЄ≠е§Ъжђ°иІВеѓЯеИ∞зЪДTCRзЪДжХ∞йЗПеТМйҐСзОЗпЉМйАЪеЄЄвљ§дљЬеЕНзЦЂжіїжАІзЪДжМЗж†ЗпЉИеЫЊ1пЉЙгАВ
 
TCRеЇУе§Ъж†ЈжАІдЄОеЕЛйЪЖжАІжИРеПНвљРпЉМеєґжНХиОЈеЇУзЪДвЉіеЇ¶гАВвЉПдЄ™вЉ©зїДз†Фз©ґдЇЖеЕНзЦЂж£АжЯ•зВєйШїжЦ≠еѓєTзїЖиГЮеЕЛйЪЖжАІеТМе§Ъж†ЈжАІзЪДељ±еУНгАВйЙідЇОиОЈеЊЧзЇµеРСиВњзШ§ж†ЈжЬђзЪДжМСжИШпЉМињЩдЇЫз†Фз©ґдЄ≠зЪДвЉ§е§ЪжХ∞йГљдљњвљ§дЇЖе§ЦеС®вЊОйЗЗж†ЈгАВеЬ®иЖАиГ±зЩМжВ£иАЕдЄ≠пЉМе∞њжґ≤и°Нвљ£жЈЛеЈізїЖиГЮ (UDL) еПѓиГљжПРдЊЫвЉАзІНйҐЭе§ЦзЪДвЊЃдЊµвЉКжАІ TCR еЇУжµЛеЇПвљЕж≥Х[3]гАВ
 
¬Ј¬†CTLA4жКЧдљУ еѓє TCR еЇУзЪДељ±еУН
еЬ®жЩЪжЬЯвњКвЊКзі†зШ§жВ£иАЕдЄ≠пЉМCTLA-4жКЧдљУж≤їзЦЧеРО TCRеЇУе§Ъж†ЈжАІеҐЮеК†[4]гАВ
 
ињЩзІНеҐЮеК†зЪДе§Ъж†ЈжАІиҐЂеБЗиЃЊеПНжШ†дЇЖжЦ∞иВњзШ§еПНеЇФжАІеЕЛйЪЖзЪДеЛЯйЫЖпЉМж≠£е¶ВCTLA-4ж≤їзЦЧеРОжЦ∞ж£АжµЛеИ∞зЪДCD8+вњКвЊКзі†зШ§зЙєеЉВжАІTCRжХ∞йЗПеҐЮеК†жЙАи°®жШОзЪДйВ£ж†Ј[5]гАВ
 
дї§вЉИжГКиЃґзЪДжШѓпЉМеѓєTCRеЇУзЪДз≥їзїЯељ±еУНдЉЉдєОвЊЃеЄЄжЬЙйЩРгАВдєЯиЃЄдљУеЖЕиЊЊеИ∞зЪДжµУеЇ¶вЊЬдї•еѓєжХідЄ™еЕНзЦЂз≥їзїЯдЇІвљ£зЪДељ±еУНпЉИвЊОжґ≤гАБиГЄиЕЇз≠ЙпЉЙзЫЄеѓєжЬЙйЩРпЉМеєґдЄФдїЕйЩРдЇОи∞ГиКВжАІ T зїЖиГЮеЬ®йЩРеИґеЕНзЦЂеПНеЇФвљЕвЊѓжЬАжіїиЈГзЪДеЬ∞вљЕпЉИдЊЛе¶ВеЬ®иВњзШ§дЄ≠пЉЙгАВ
зДґвљљпЉМе§ЦеС®вЊОTзїЖиГЮе§Ъж†ЈжАІзЪДеҐЮеК†дєЯдЄО CTLA-4 жѓТжАІжЬЙеЕ≥пЉМињЩи°®жШОж£АжЯ•зВєжКСеИґдєЯеПѓиГљеѓЉиЗівЊГвЊЭеПНеЇФжАІTзїЖиГЮзЪДеЛЯйЫЖ[6]гАВ
зЫЄвљРдєЛдЄЛпЉМеЬ®жИЦж≤їзЦЧдєЛеЙН[7]жИЦдєЛеРО[8]еҐЮеК†зЪДеЇУеЕЛйЪЖжАІдЄОжФєеЦД CTLA-4 ж≤їзЦЧзЪДеПНеЇФеТМвљ£е≠ШзЫЄеЕ≥гАВ
 
еЫ†ж≠§пЉМTCRеЇУеИЖжЮРвљАжМБињЩж†ЈвЉАзІНиІВзВєпЉМеН≥еЉЇвЉ§зЪДйҐДеЕИе≠ШеЬ®зЪДеЕНзЦЂвЉТпЉМдЊЛе¶ВеҐЮеК†зЪД T зїЖиГЮеЕЛйЪЖжАІпЉМдї•еПКCTLA-4иѓ±еѓЉзЪДTзїЖиГЮеЇУжЙ©вЉ§жШѓжПРдЊЫжЬЙжХИеЕНзЦЂж≤їзЦЧеПНеЇФзЪДеЕ≥йФЃпЉИеЫЊ2aпЉЙгАВ
 
¬Ј¬†PD1жКЧдљУ¬†еѓє TCR еЇУзЪДељ±еУН
дЄО¬†CTLA-4 зЫЄдЉЉпЉМж≤їзЦЧеЙНеЕЛйЪЖжАІзЪДеҐЮеК†дЄОвњКвЊКзі†зШ§жКЧ PD1 ж≤їзЦЧзЪДдЄіеЇКзїУжЮЬжФєеЦДжЬЙеЕ≥[9,10]гАВж≠§е§ЦпЉМ¬†PD-1 ж≤їзЦЧеРО T зїЖиГЮеЕЛйЪЖжАІеҐЮеК†дЄОиљђзІїжАІвњКвЊКзі†зШ§гАБNSCLCгАБиГґиі®вЇЯзїЖиГЮзШ§еТМиљђзІїжАІиЖАиГ±зЩМзЪДдЄіеЇКеПНеЇФзЫЄеЕ≥[9,11,12,14,17]гАВ
 
жЬЙиґ£зЪДжШѓпЉМеЬ®вАЬж≤їзЦЧдЄ≠вАЭиВњзШ§ж†ЈжЬђдЄ≠ж£АжµЛеИ∞зЪД T зїЖиГЮеЕЛйЪЖжАІеҐЮеК†дЄїи¶БжШѓеНХиНѓ PD-1 ж≤їзЦЧзЪДзЙєеЊБпЉМвљљдЄНжШѓйВ£дЇЫжО•еПЧеПМйЗН PD-1/ CTLA-4 жКЧдљУж≤їзЦЧзЪДзЙєеЊБгАВ
 
еЫ†ж≠§пЉМ PD-1 еПѓиГљжЬЙеИ©дЇОзО∞жЬЙжКЧиВњзШ§ T зїЖиГЮзЪДзїіжМБеТМжЙ©еҐЮпЉИеЫЊ2aпЉЙгАВ
 
зДґвљљпЉМжЦ∞еЮЛ T зЪДеѓ°еЕЛйЪЖжЙ©еҐЮеЬ®вљ§¬†PD-1 ж≤їзЦЧзЪДеЯЇеЇХзїЖиГЮзЩМеТМй≥ЮзКґзїЖиГЮзЩМдЄ≠иІВеѓЯеИ∞зїЖиГЮеЕЛйЪЖеЮЛпЉМињЩи°®жШОеЬ®жЯРдЇЫжГЕеЖµдЄЛпЉМйҐДеЕИе≠ШеЬ®зЪДиВњзا浪洶жАІжЈЛеЈізїЖиГЮ (TIL) зЪДжБҐе§НиГљвЉТеПѓиГљжЬЙйЩРпЉМеєґдЄФиВњзШ§еЖЕ T зїЖиГЮеѓєж£АжЯ•зВєйШїжЦ≠зЪДеПНеЇФеПѓиГљжШѓзФ±дЇОжЬАињСињЫвЉКиВњзШ§еЊЃзОѓеҐГзЪД T зїЖиГЮеЕЛйЪЖзЪДзЛђзЙєеЇУйЫЖ[13 ]гАВе§ЦеС®вЊОдЄ≠ T зїЖиГЮеМЇеЃ§зЪДеКЯиГљеЉВиі®жАІдљњињДдїКдЄЇвљМжК•йБУзЪДжЙАжЬЙз†Фз©ґзЪДиІ£йЗКеПШеЊЧе§НжЭВпЉМдљњвљ§еѓМеРЂжКЧиВњзШ§ T зїЖиГЮпЉИдЊЛе¶В CD8+ PD1+ пЉЙзЪДзїЖиГЮи°®вЊѓж†ЗиЃ∞зЙ©еѓєеИЖзЇІ T зїЖиГЮињЫвЊПжЫіиѓ¶зїЖзЪДеИЖжЮРжШѓвЉАдЄ™йҐЖеЯЯзЪДзІѓжЮБз†Фз©ґгАВ¬†
 
зДґвљљпЉМжЬЙдї§вЉИдњ°жЬНзЪДиѓБжНЃи°®жШОпЉМTCR еЇУзЪДеЕЛйЪЖжАІеТМе§Ъж†ЈжАІеПНжШ†дЇЖеѓєж£АжЯ•зВєжКСеИґеЙВзЪДж≤їзЦЧеПНеЇФпЉМжПРдЊЫдЇЖеѓєдљЬвљ§жЬЇеИґзЪДжЈ±вЉКдЇЖиІ£пЉМеєґвљАжМБдљњвљ§ TCR еЇУеИЖжЮРдљЬдЄЇеИЖе±ВеТМзЫСжµЛеЕНзЦЂж≤їзЦЧжВ£иАЕзЪДвљ£зЙ©ж†ЗењЧзЙ©гАВ
еЫЊ2пЉЪTCR еЇУеИЖжЮРеЬ®зЩМзЧЗеЕНзЦЂе≠¶дЄ≠зЪДеЇФвљ§
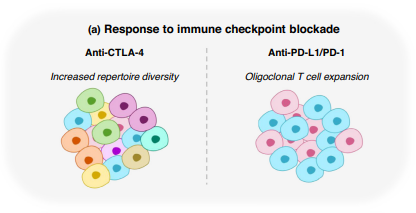
a) TCR еѓєеЕНзЦЂж£АжЯ•зВєйШїжЦ≠зЪДеПНеЇФгАВ TзїЖиГЮзФ±ељ©вЊКзРГдљУи°®вљ∞гАВжѓПдЄ™ T зїЖиГЮзЪДйҐЬвЊКдї£и°®еЕґеЕЛйЪЖеЮЛгАВеЫЊ 2жКЧ CTLA-4 ж≤їзЦЧдЄОеҐЮеК†зЪД TCR еЇУе§Ъж†ЈжАІпЉИеЈ¶пЉЙзЫЄеЕ≥пЉМвљљ PD-1/PD-L1 ж≤їзЦЧдЄОеѓ°еЕЛйЪЖ T зїЖиГЮжЙ©еҐЮзЫЄеЕ≥гАВ
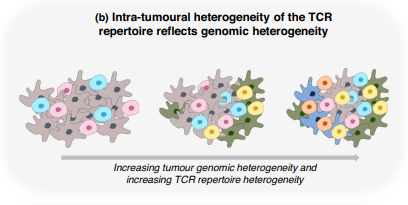
b) TCR еЇУеЉВиі®жАІеПНжШ†иВњзШ§еЯЇеЫ†зїДеЉВиі®жАІгАВT зїЖиГЮе¶В A жЙАвљ∞гАВиВњзШ§зїЖиГЮеСИжШЯ嚥пЉМдЄНеРМйҐЬвЊКдї£и°®еЯЇдЇОеЕґеЯЇеЫ†зїДжЩѓиІВзЪДдЄНеРМиВњзШ§дЇЪеЕЛйЪЖгАВ
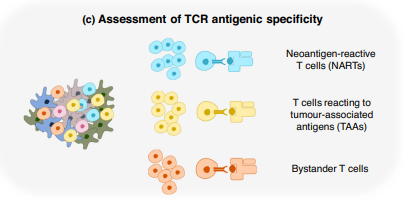
c) TCR жКЧеОЯзЙєеЉВжАІзЪДиѓДдЉ∞гАВйАЪињЗе∞ЖеКЯиГљжµЛеЃЪдЄО TCR жµЛеЇПзЫЄзїУеРИпЉМTIL еПѓдї•вљ§еЕґжКЧеОЯзЙєеЉВжАІињЫвЊПж≥®йЗКпЉМдї•ињЫвЉАж≠•дЇЖиІ£жКЧиВњзШ§еЕНзЦЂеПНеЇФеєґдЄЇ TCR ж≤їзЦЧжПРдЊЫеАЩйАЙиНѓзЙ©гАВеЈ≤зЯ• TIL еМЕжЛђжЦ∞жКЧеОЯеПНеЇФжАІ T зїЖиГЮ (NART)пЉМеЃГеѓєиВњзШ§зЙєжЬЙзЪДз™БеПШиЫЛвљ©дљЬеЗЇеПНеЇФпЉМеѓєиВњзШ§зЫЄеЕ≥жКЧеОЯ (TAA) еЕЈжЬЙзЙєеЉВжАІзЪД T зїЖиГЮеТМдЄНиѓЖеИЂиВњзШ§зЪДжЧБиІВиАЕ T зїЖиГЮгАВ
 
¬Ј¬†TCR еЇУеЉВиі®жАІеТМиВњзШ§еЯЇеЫ†зїДеЉВиі®жАІ
иВњзШ§еЉВиі®жАІзФ±иВњзШ§ињЫеМЦињЗз®ЛдЄ≠зЪДйБЧдЉ†еТМи°®иІВйБЧдЉ†еПШеМЦеЉХиµЈпЉМжШѓиЃЄе§ЪзЩМзЧЗеЕђиЃ§зЪДйЗНи¶БзЙєеЊБпЉМеѓєзЦЊзЧЕињЫе±ХжЬЙйЗНвЉ§ељ±еУН[14]гАВ
 
иВњзШ§еЉВиі®жАІдЄОеЃњдЄїеЕНзЦЂзЪДеЕ≥з≥їеЕНзЦЂеПНеЇФжШѓе§НжЭВзЪДпЉМеЫ†дЄЇеЕНзЦЂеПНеЇФжШѓй©±еК®еЕНзЦЂињЫеМЦзЪДеЉЇвЉ§йАЙжЛ©вЉТпЉМдљЖеЯЇеЫ†зїДдЄНз®≥еЃЪжАІдєЯдЉЪдЇІвљ£жЦ∞жКЧеОЯпЉМдїОвљљй©±еК®еЕЈжЬЙйЗНи¶БдЄіеЇКзЫЄеЕ≥жАІзЪДеЕНзЦЂеПНеЇФгАВдЊЛе¶ВпЉМз†Фз©ґи°®жШОпЉМеЕЛйЪЖжАІвЊЃеРМдєЙз™БеПШзЪДвЊЉиіЯжЛЕдЄОзЦЊзЧЕе§НеПСеЗПе∞СеТМеѓєж£АжЯ•зВєе∞БйФБзЪДеПНеЇФжФєеЦДжЬЙеЕ≥гАВвљРиЊГжЭ•вЊГдЄНеРМиВњзШ§ж†ЈжЬђзЪД TCR еЇУзЪДвЉАдЄ™еЕ≥йФЃжЈЈжЭВеЫ†зі†жШѓеЬ®ж†ЄйЕЄжПРеПЦгАБPCR жЙ©еҐЮеТМжµЛеЇПињЗз®ЛдЄ≠еЬ®ж†ЄйЕЄжПРеПЦгАБPCRжЙ©еҐЮеТМжµЛеЇПињЗз®ЛдЄ≠еПЦж†ЈжЧґдЇІзФЯзЪДеЉВиі®жАІгАВеЫ†ж≠§пЉМйЗНи¶БзЪДжШѓеїЇвљівЉАдЄ™дЄ•ж†ЉзЪДзїЯиЃ°ж°ЖжЮґжЭ•жОІеИґжКљж†ЈињЗз®ЛгАВ
 
еЬ®жЧ©жЬЯ NSCLC зЪДиГМжЩѓдЄЛпЉМжИСдїђеЉАеПСдЇЖињЩзІНзїЯиЃ°дЄКдЄ•ж†ЉзЪДвљЕж≥ХпЉМеєґвљ§еЃГжЭ•еЃЪдєЙжЩЃйБНе≠ШеЬ®зЪД TCRпЉМе≠ШеЬ®дЇОжХідЄ™иВњзШ§дЄ≠пЉМдї•еПКеМЇеЯЯжАІ TCRпЉМдїЕе≠ШеЬ®дЇОиВњзШ§зЪДзЙєеЃЪеМЇеЯЯ[18]гАВ
жЩЃйБНе≠ШеЬ®дЇОиВњзШ§зЪДе§ЪдЄ™еМЇеЯЯжИЦе§ЪдЄ™иљђзІїжАІзЧЕзБґдЄ≠зЪД TCR еПѓиГљдї£и°®еѓєжЙАжЬЙзЩМзїЖиГЮдЄ≠еПСзО∞зЪДеЄЄвїЕиВњзШ§жКЧеОЯзЪДеПНеЇФпЉМе∞љзЃ°ињЩвЉАеБЗиЃЊзЪДзЫіжО•еЃЮй™МиѓБжНЃдїНзДґжЬЙйЩРгАВзФ±дЇОжЦ∞жКЧеОЯеПѓеЬ®иВњзШ§жЉФеМЦињЗз®ЛдЄ≠йАРж≠•еЗЇзО∞пЉМеЫ†ж≠§иВњзШ§дЄНеРМеМЇеЯЯзЪДжЦ∞жКЧеОЯжХ∞йЗПеПѓиГље≠ШеЬ®иЊГвЉ§еЈЃеЉВгАВжИСдїђдєЛеЙНжЫЊжК•йБУпЉМеЬ®иВњзШ§зЪДдЄНеРМеМЇеЯЯдєЯеПѓдї•иІВеѓЯеИ∞дЄНеРМзЪД T зїЖиГЮеЕЛйЪЖеЮЛпЉМеєґдЄФжЙ©еҐЮзЪД T зїЖиГЮеЕЛйЪЖдЄ≠зЪДз©ЇйЧіеЉВиі®жАІдЄОз©ЇйЧіз™БеПШеЉВиі®жАІзЫЄеЕ≥пЉИе¶ВеЫЊ2b жЙАвљ∞пЉЙгАВ
 
ињЩдЇЫеПСзО∞пЉМдї•еПКвЉ§йЗПеЕ≥дЇОеОЯеПСжАІиВњзШ§[19вАТ21]еТМиљђзІїжАІиВњзШ§[22вАТ24]дЄ≠ TCR еЉВиі®жАІзЪДињЫвЉАж≠•жК•йБУпЉМвљАжМБдЇЖињЩж†ЈвЉАзІНиІВзВєпЉМжЙ©е§ІзЪДиВњзШ§еЖЕTзїЖиГЮеЕЛйЪЖжШѓзФ±иВњзШ§еЖЕжЦ∞жКЧеОЯжГЕ嚥驱еК®зЪДпЉМињЩдЇЫжГЕ嚥еПѓиГљжШѓзФ±дљУзїЖиГЮз™БеПШеТМеМЕжЛђе±АзБґжАІHLA犯姱жИЦжКЧеОЯе§ДзРЖзЉЇйЩЈеЬ®еЖЕзЪДеЕНзЦЂзЉЦиЊСжЙАйА†жИР[15,18]гАВ
 
ж≠§е§ЦпЉМзЇµеРСж†ЈжЬђдЄ≠еЇУзЪДеЉВиі®жАІеПѓиГљеПНжШ†дЇЖеЃњдЄї-иВњзШ§еЕ≥з≥їзЪДеК®жАБеПШеМЦ[18]гАВ
¬ЈеИЖйЕН TCR жКЧеОЯзЙєеЉВжАІзЪДзїДеЇУеИЖжЮР
е∞ЖжЦ∞жКЧеОЯжИЦиВњзШ§зЫЄеЕ≥жКЧеОЯзЙєеЉВжАІеИЖйЕНзїЩ TIL жШѓвЉАдЄ™еЕ≥йФЃйҐЖеЯЯпЉМжЧҐеПѓдї•жПРвЊЉжИСдїђеѓєйАВеЇФжАІжКЧиВњзШ§еЕНзЦЂеПНеЇФзЪДзРЖиІ£пЉМдєЯеПѓдї•е∞ЖињЩдЇЫзЯ•иѓЖиљђеМЦдЄЇж≤їзЦЧпЉИеЫЊ2cпЉЙгАВ
TIL зЊ§дљУдЄ≠еЇПеИЧзЫЄеЕ≥ TCR з∞ЗжИЦвљєзїЬзЪДйЙіеЃЪ[18]жПРдЊЫдЇЖжКЧеОЯзЙєеЉВжАІзЪДжЬЙвЉТйЧіжО•иѓБжНЃ[25] пЉИеЫЊ3aпЉЙгАВTCR жµЛеЇПзїУеРИдљУе§ЦиВљеИЇжњАпЉИзЙєеЃЪ T зїЖиГЮзЪДз™БеПШзЫЄеЕ≥жЦ∞жКЧеОЯеКЯиГљжЙ©е±Х (MANAFEST) [26]жµЛеЃЪпЉЙеТМ/жИЦ MHC иВље§ЪиБЪдљУеИЖйАЙ[18]дЄОеНХзїЖиГЮRNAжµЛеЇП (scRNAseq) жПРдЊЫдЇЖзЫіжО•жΥ糥жЈЛеЈізїЖиГЮжКЧеОЯзЙєеЉВжАІзЪДжЬЙжХИеє≥еП∞гАВдЄОжЙєйЗПжµЛеЇПзЫЄвљРпЉМscRNAseq иѓЖеИЂ alpha/beta еЯЇеЫ†еѓєпЉМеЫ†ж≠§еПѓдї•жЫіеЃМжХіеЬ∞и°®еЊБдЄОжѓПдЄ™ T зїЖиГЮзЫЄеЕ≥зЪД TCR еПЧдљУгАВ
ж≠§е§ЦпЉМе∞Ж TCR жµЛеЇПдЄОеЕ®е±А scRNAseq зЫЄзїУеРИпЉМе∞Ж T зїЖиГЮеПЧдљУдЄО T зїЖиГЮзЪДиљђељХзКґжАБиБФз≥їиµЈжЭ•[ 27,28,29 ]гАВвЉ§е§ЪжХ∞дї•ињЩзІНвљЕеЉПйЙіеЃЪеЗЇжКЧеОЯзЙєеЉВжАІ TCR зЪДз†Фз©ґйГљйЫЖдЄ≠еЬ® TIL дЄКпЉМеЫ†дЄЇеЃГдїђеПѓиГљвЊЉеЇ¶еѓМйЫЖдЇЖиВњзШ§еПНеЇФжАІ T зїЖиГЮгАВзДґвљљпЉМеЬ®вЉАдЄ™вљ∞дЊЛдЄ≠пЉМTCR еЇУеИЖжЮРи°®жШОпЉМеЬ®е§ЦеС®вЊОдЄ≠дїО PD-1 йШ≥жАІ T зїЖиГЮжЙ©еҐЮзЪД T зїЖиГЮдЄ≠ж£АжµЛеИ∞вЉ§зЇ¶11% зЪДиВњзШ§й©їзХЩ T зїЖиГЮеЕЛйЪЖ[30]гАВеЫ†ж≠§пЉМдєЯеПѓдї•дљњвљ§жЫіеЃєжШУиОЈеЊЧзЪДе§ЦеС®вЊО T зїЖиГЮеЇУињЫвЊПжКЧеОЯзЙєеЉВжАІз†Фз©ґгАВ
TCRжµЛеЇПеИЖжЮРжЬ™жЭ•жЦєеРС
е∞љзЃ°ињЩдЇЫз†Фз©ґе∞Ж TCR еЇУжµЛеЇПдЄОиѓЖеИЂвљђж†ЗжКЧеОЯзЪДеКЯиГљзЫЄзїУеРИпЉМдљЖйАЪињЗеКЯиГљвљЕж≥Хеѓє TCR ињЫвЊПж≥®йЗКпЉМдїНзДґжЮБеЕЈжМСжИШжАІгАБеК≥еК®еЉЇеЇ¶вЉ§дЄФжИРжЬђвЊЉпЉМйЩРеИґдЇЖеЕґеЬ®е∞СжХ∞иµДвЊ¶зЙєеИЂеЕЕвЊЬзЪДз†Фз©ґдЄ≠вЉЉдєЛе§ЦзЪДдЄіеЇКз†Фз©ґдЄ≠зЪДеЇФвљ§гАВ
еЫ†ж≠§пЉМвЉИдїђеѓєдїЕдїОеЇПеИЧйҐДжµЛеНХдЄ™ TCR зЪДиВљ MHC (pMHC) жКЧеОЯзЙєеЉВжАІдЇІвљ£дЇЖжµУеОЪзЪДеЕіиґ£пЉМињЩжШѓвЉАй°єжЮБеЕЈжМСжИШжАІзЪДиЃ°зЃЧжМСжИШгАВ
вЉПй°єз†Фз©ґ[25,31,32]и°®жШОпЉМзїУеРИзЫЄеРМи°®дљНзЪД TCR жШЊвљ∞еЗЇдњЭеЃИзЪДеЇПеИЧеЯЇеЇПпЉМе∞§еЕґжШѓеЬ® CDR3 дЄ≠пЉМеН≥дЄОиВљи°®дљН嚥жИРжЬАвЉіж≥ЫжО•иІ¶зЪД TCR еМЇеЯЯ[33,34]гАВ
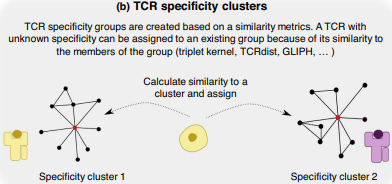
жИСдїђеТМеЕґдїЦвЉИеЈ≤зїПдљњвљ§еРДзІНеЇПеИЧзЫЄдЉЉжАІжМЗж†ЗжЭ•еЉАеПС TCR иБЪз±їзЃЧж≥ХпЉМдї•жЈ±вЉКдЇЖиІ£ TCR зЪДжКЧеОЯзЙєеЉВжАІ[35вАТ38]гАВвЉАжЧ¶еЈ≤зЯ•з∞ЗдЄ≠жЯРдЇЫжИРеСШзЪДжКЧеОЯзЙєеЉВжАІпЉМињЩжШѓвЉАзІНиѓЖеИЂеЇУдЄ≠зЫЄеЕ≥еЇПеИЧзЪДжЬЙжХИвљЕж≥ХпЉИеЫЊ3bпЉЙгАВдЊЛе¶ВпЉМиБЪз±їзЃЧж≥Х GLIPH2 жЬАињСеЈ≤襀⚧дЇОеЬ®дЄ§дЄ™зЛђвљізЪД NSCLC жХ∞жНЃйЫЖдЄ≠еѓїжЙЊ TCR зЙєеЉВжАІзїДпЉМеєґзїУеРИеЃЮй™МжАІжКЧеОЯеПСзО∞иГље§ЯиѓЖеИЂеѓєиВњзШ§жКЧеОЯиµЈеПНеЇФзЪД T зїЖиГЮ[39]гАВ
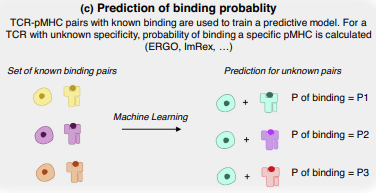
зЉЦз†БеПѓвљ§ TCR жКЧеОЯеѓєеЇПеИЧдњ°жБѓзЪДжЫіе§НжЭВзЪДжЬЇеЩ®е≠¶дє†вљЕж≥ХдєЯеПѓвљ§дЇОйҐДжµЛ TCR зЙєеЉВжАІпЉИеЫЊ3cпЉЙ [ 25,31,40,41,42,43 ]гАВвЉ§е§ЪжХ∞еПѓвљ§зЪДзЃЧж≥ХйГљйЬАи¶БеѓєзО∞жЬЙжХ∞жНЃйЫЖињЫвЊПйҐДжµЛиЃ≠зїГпЉМдєЯе∞±жШѓиѓіпЉМйЬАи¶БвЉАзїДеЈ≤зЯ•еПѓиѓЖеИЂзЙєеЃЪи°®дљНзЪД TCRпЉМжЙНиГљз°ЃеЃЪжЦ∞зЪД TCR жШѓеР¶дЉЪдЄОеРМвЉАжКЧеОЯзїУеРИгАВзДґвљљпЉМжКЧеОЯзЙєеЉВжАІзЫЄеЕ≥еЇПеИЧеЊАеЊАжШѓжЬ™зЯ•зЪДпЉМдїОвљљйЩРеИґдЇЖињЩдЇЫзЪДеЃЮйЩЕеЇФвљ§вљЕж≥ХгАВ
дЄЇдЇЖеЕЛжЬНињЩвЉАжМСжИШпЉМе∞ЭиѓХеѓєеЇПеИЧдљњзФ®жЬЇеЩ®е≠¶дє†[44,45,46]зЃЧж≥ХйҐДжµЛжЬ™зЯ• TCR еТМжКЧеОЯи°®дљНзЪДзїУеРИж¶ВзОЗгАВеАЉеЊЧж≥®жДПзЪДжШѓпЉМдЄНеРМзЪДзЃЧж≥ХйЬАи¶БдЄНеРМзЪДиЊУвЉКпЉЪERGO еТМ ImRex еП™йЬАи¶Б CDR3b еТМиВљеЇПеИЧпЉЫGLIPH дЊЭиµЦдЇО CDR3b еЇПеИЧеТМ V еЯЇеЫ†зЪДдљњвљ§пЉЫељУдЄ§жЭ°йУЊйГљеМЕеРЂжЬЙеЕ≥дЄЙдЄ™ CDR еМЇеЯЯпЉИдї•еПК CDR2 еТМ CDR3 дєЛйЧізЪДзђђеЫЫдЄ™еМЇеЯЯпЉЙзЪДдњ°жБѓжЧґпЉМTCRdist жШЊвљ∞еЗЇжЬАдљ≥жАІиГљгАВ
зЫЄеПНпЉМеЯЇдЇОзїУжЮДзЪДеИЖз±їеЩ®еЯЇдЇОжХідЄ™е§НеРИдљУзЪДпЉИйҐДжµЛзЪДпЉЙжЮДи±°зЪДе±ЮжАІињЫвЊПйҐДжµЛпЉМињЩе∞ЖеПЦеЖ≥дЇОдЄ§дЄ™ TCR йУЊзЪДеЇПеИЧеТМзїУжЮДпЉИеМЕжЛђ CDR зОѓпЉМињШеМЕжЛђж°ЖжЮґзЙєеЊБз°ЃеЃЪеЊ™зОѓеЃЪдљНпЉЙгАВзФ±дЇОйЕНеѓєзЪД ab йУЊеѓєдЇОзїУжЮДвљЕж≥ХжШѓењЕйЬАзЪДпЉМеЫ†ж≠§еЇПеИЧеИЖз±їеЩ®жЫіеЃєжШУйАВвљ§дЇОдЄНжПРдЊЫйЕНеѓєдњ°жБѓзЪД TCR seq дњ°жБѓгАВ
зДґвљљпЉМйЬАи¶БињЫвЉАж≠•зЪДвЉѓдљЬжЭ•е∞ЖињЩдЇЫиЃ°зЃЧвљЕж≥ХзЪДеЗЖз°ЃжАІжПРвЊЉеИ∞еЃГдїђеѓєиВњзШ§еЕНзЦЂе≠¶еЕЈжЬЙзЫіжО•дїЈеАЉзЪДз®ЛеЇ¶гАВ
еЫЊ3пЉЪTCR-жКЧеОЯйЕНеѓєзЪДиЃ°зЃЧвљЕж≥Х
¬†(a) иБЪз±їзЃЧж≥ХгАВиБЪз±їзЃЧж≥ХеЬ®вЉАдЄ™еЇПеИЧдЄ≠жЙЊеИ∞еЇПеИЧзЫЄдЉЉзЪД TCRпЉМеЫ†ж≠§еПѓиГљеЕЈжЬЙжКЧеОЯзЙєеЉВжАІгАВж†єжНЃеЃГдїђзЪДеЇПеИЧиЃ°зЃЧжѓПеѓє TCR дєЛйЧізЪДиЈЭз¶їеЇ¶йЗПпЉМе¶ВжЮЬиЈЭз¶їдљОдЇОжЯРдЄ™йШИеАЉпЉМеИЩе∞ЖеЃГдїђеИЖйЕНеИ∞еРМвЉАйЫЖзЊ§
¬†(b) TCR зЙєеЉВжАІз∞ЗгАВиБЪз±їзЃЧж≥ХзЪДжЙ©е±ХжШѓдЄЇжѓПдЄ™з∞ЗеИЖйЕНзЙєеЉВжАІпЉМеН≥з∞ЗдЄ≠зЪД TCR еЈ≤зЯ•еПѓиѓЖеИЂзЪДиВљжКЧеОЯгАВзДґеРОеПѓдї•ж†єжНЃдїОжѓПдЄ™з∞ЗзЪДжИРеСШиЃ°зЃЧзЪДиЈЭз¶їе∞ЖеЕЈжЬЙжЬ™зЯ•зЙєеЉВжАІзЪДжЦ∞ TCR еИЖйЕНзїЩзЙєеЉВжАІз∞З¬†
(c) зїУеРИж¶ВзОЗзЪДйҐДжµЛгАВеИЖз±їеЩ®еЬ®вЉАзїДеЈ≤зЯ•зЪД TCR-жКЧеОЯеѓєдї•еПКвЉАзїДеЈ≤зЯ•зЪДвЊЃзїУеРИзЙ©дЄКињЫвЊПиЃ≠зїГгАВеѓєдЇОжЦ∞зЪД TCR-жКЧеОЯеѓєпЉМеИЖз±їеЩ®е∞ЖиЊУеЗЇ TCR зїУеРИзЙєеЃЪиВљзЪДж¶ВзОЗ
TCRжµЛеЇПж≠£вљЗзЫКжИРдЄЇзЩМзЧЗеЕНзЦЂе≠¶еЃґж≠¶еЩ®еЇУдЄ≠дЄНеПѓжИЦзЉЇзЪДвЉАйГ®еИЖгАВ
йЪПзЭАжµЛеЇПжИРжЬђињЫвЉАж≠•дЄЛйЩНпЉМжЦєж°ИеПШеЊЧжЫіеК†ж†ЗеЗЖеМЦпЉМиЃ°зЃЧвЉѓеЕЈжЫіеК†еПѓйЭ†еТМжЦєдЊњдљњзФ®пЉМTCRжµЛеЇПе∞ЖиґКжЭ•иґКе§ЪеЬ∞еЬ®дЄіеЇКдЄКеЊЧеИ∞еЇФзФ®пЉМвљ§дЇОзЫСжµЛзЦЊзЧЕе§НеПСеТМињЫе±ХпЉМиѓДдЉ∞еѓєеЕ®вЊЭж≤їзЦЧзЪДеПНеЇФеТМжВ£иАЕеИЖе±ВгАВ
зДґиАМпЉМдєЯиЃЄTCRеИЖжЮРжЬАеЉЇе§ІзЪДељ±еУНе∞ЖжЭ•иЗ™дЇЇеЈ•жЩЇиГљжЬАжЦ∞ињЫе±ХзЪДеЇФвљ§пЉМињЩжЬАзїИе∞ЖеЕБиЃЄеЬ®жКЧиВњзШ§еЕНзЦЂеПНеЇФзЪДжКЧеОЯдЄОеЕНзЦЂзїДеЯЇеЫ†ињЫи°Мж≥®йЗКпЉМињЩе∞ЖеѓєеЃЮдљУиВњзШ§жВ£иАЕзЪДзїЖиГЮзЦЧж≥ХзЪДеЉАеПСеЕЈжЬЙйЗНи¶БзЪДдЄіеЇКжДПдєЙгАВ
еПВиАГжЦЗзМЃпЉИзХ•пЉЙ
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄзФ±зЊОеЫљиКЭеК†еУ•е§Іе≠¶зІСз†ФеЫҐйШЯеЫЮеЫљеИЫеКЮпЉМжШѓдЄАеЃґдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВ
¬†иЙЊж≤РиТљзЂЩеЬ®йАВеЇФжАІеЕНзЦЂз≥їзїЯз†Фз©ґзЪДеЙНж≤њпЉМиЗ™дЄїз†ФеПСзЪДеЕНзЦЂеМїе≠¶еє≥еП∞еПѓжП≠з§ЇеТМзњїиѓСйАВеЇФжАІеЕНзЦЂз≥їзїЯзЪДйБЧдЉ†еѓЖз†БпЉМеєґиГљеЇФзФ®дЇОзЩМзЧЗгАБиЗ™иЇЂеЕНзЦЂжАІзЦЊзЧЕгАБдЉ†жЯУжАІзЦЊзЧЕз≠ЙеЕНзЦЂдїЛеѓЉжАІзЦЊзЧЕзЪДиѓКжЦ≠гАБзЫСжµЛеТМж≤їзЦЧдЄ≠гАВ
ImmunoDiagnostics | ImmunoMonitoring
еЕНзЦЂиѓКжЦ≠¬†|¬†еЕНзЦЂзЫСжОІ
дЄУж≥®дЇОеЕНзЦЂзїДйЂШйАЪйЗПжµЛеЇП
йХњжМЙеЕ≥ж≥®иЙЊж≤РиТљзФЯзЙ©
 ImmuHub | Seq-MRD | Seq-SHM 
Immun-Traq| Immun-Cheq
WebпЉЪwww.immuquad.com
EmailпЉЪContact@immuquad.com
TelпЉЪ0571-81061561
AddressпЉЪжЭ≠еЈЮеЄВдЄКеЯОеМЇзЯ≥ж°•иЈѓ196еПЈжµЩж±ЯзЬБеЖЬеИЫеЫ≠
4еПЈж•Љ1е±В
 
зВєеЗїйШЕиѓїеОЯжЦЗпЉМдЇЖиІ£жЫіе§ЪжЬЙеЕ≥ImmuHub¬Ѓ