вЧПиВЊзІїж§НжШѓж≤їзЦЧзїИжЬЂжЬЯиВЊиДПзЦЊзЧЕзЪДжЦєж≥ХдєЛдЄАпЉМзДґиАМпЉМжВ£иАЕеЬ®жО•еПЧиВЊзІїж§НеРОдїНзДґйЭҐдЄізЭАеЕНзЦЂжОТжЦ•еТМеЕНзЦЂзЫЄеЕ≥еєґеПСзЧЗзЪДй£ОйЩ©гАВеЕНзЦЂеПНеЇФзЪДеПСзФЯеТМжЉФеМЦжШѓиВЊзІїж§НеРОжВ£иАЕйҐДеРОеТМзІїж§НеЩ®еЃШзФЯе≠ШзЪДеЕ≥йФЃеЫ†зі†гАВдЉ†зїЯзЪДз†Фз©ґжЦєж≥ХеЊАеЊАжЧ†ж≥ХжПРдЊЫеѓєеЕНзЦЂеПНеЇФеЕ®йЭҐзЪДдЇЖиІ£пЉМеЫ†ж≠§йЬАи¶БйЗЗзФ®жЫіеК†еЕИињЫзЪДжКАжЬѓжЭ•жП≠з§ЇеЕґдЄ≠зЪДзїЖиКВгАВ
вЧПеЕНзЦЂзїДеЇУжКАжЬѓеЬ®иВЊзІїж§НеРОеЕНзЦЂеПНеЇФз†Фз©ґдЄ≠зЪДеЇФзФ®:
еЕНзЦЂзїДеЇУжКАжЬѓеЯЇдЇОйЂШйАЪйЗПжµЛеЇПжКАжЬѓпЉМиГље§ЯеѓєеЕНзЦЂз≥їзїЯдЄ≠зЪДTзїЖиГЮеТМBзїЖиГЮеПЧдљУињЫи°МеЕ®йЭҐзЪДеИЖжЮРгАВйАЪињЗеЕНзЦЂзїДеЇУжКАжЬѓпЉМеПѓдї•иОЈеЊЧе§ІйЗПзЪДTзїЖиГЮеПЧдљУеТМBзїЖиГЮеПЧдљУзЪДеЇПеИЧдњ°жБѓпЉМеєґеѓєеЕґе§Ъж†ЈжАІеТМеЕЛйЪЖеК®жАБињЫи°МеИЖжЮРгАВињЩдљњеЊЧжИСдїђиГље§ЯжЈ±еЕ•дЇЖиІ£иВЊзІїж§НеРОеЕНзЦЂеПНеЇФзЪДеПСзФЯдЄОжЉФеМЦгАВ
#1

ж†ЗйҐШпЉЪCharacterizing pre-transplant and post-transplant¬†kidney rejection risk by B cell immune repertoire¬†sequencing
йАЪињЗBзїЖиГЮеЕНзЦЂеЇУжµЛеЇПжППињ∞зІїж§НеЙНеТМзІїж§НеРОзЪДиВЊжОТжЦ•й£ОйЩ©
еПСи°®жЬЯеИКпЉЪNature Communications
еПСи°®жЧ•жЬЯпЉЪ2019еєі4жЬИ
ељ±еУНеЫ†е≠РпЉЪ17.694
01
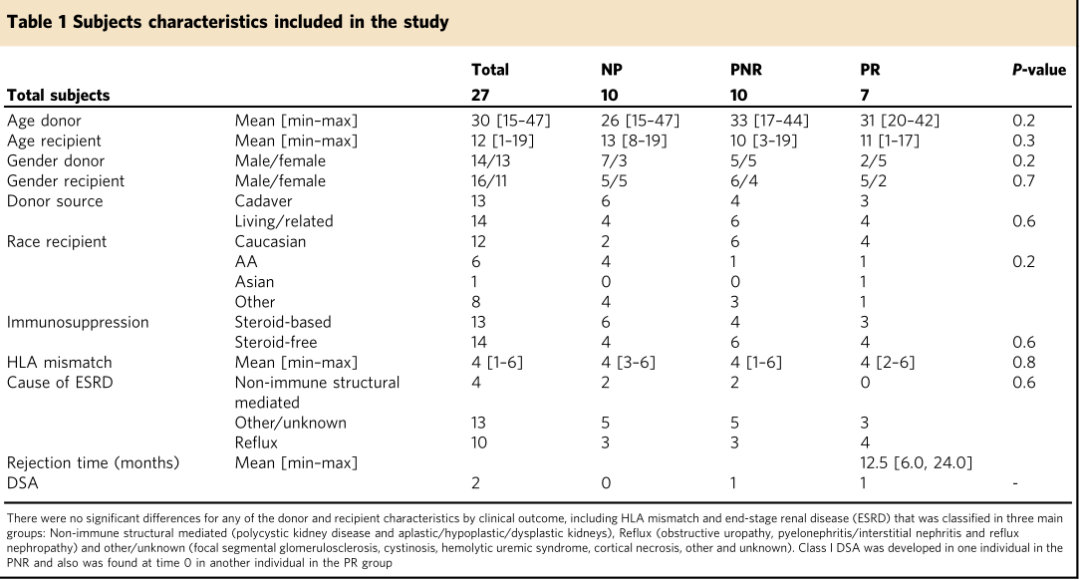
ж†ЈжЬђ
жЭ•иЗ™27дЊЛзЙєжЃКжВ£иАЕзЪД83дїље§ЦеС®и°Аж†ЈжЬђ
02
иГМжЩѓ
еЬ®з†Фз©ґдЄ≠йАЪињЗBCRseqжЭ•жППињ∞е§ЦеС®и°АеЕНзЦЂеЇУпЉМзІїж§НеРОеПСзФЯжОТжЦ•еПНеЇФзЪДдЄ™дљУеЬ®зІїж§НеЙНеЕНзЦЂеЇУеЕЈжЬЙжЫійЂШе§Ъж†ЈжАІпЉМеЬ®24дЄ™жЬИзЪДйЪПиЃњдЄ≠дєЯжШЊз§ЇеЗЇжЯРдЇЫеЕЛйЪЖеТМIGHVеЯЇеЫ†зЪДжЙ©еҐЮгАВињЩдЇЫзїУжЮЬдЄНдїЕжЬЙеК©дЇОйҐДжµЛзІїж§НеЙНжОТжЦ•й£ОйЩ©пЉМињШеѓєж£АжµЛеЉХиµЈжОТжЦ•еПНеЇФзЪДзЙєеЃЪжКЧеОЯжЬЙеЕЈжЬЙдЄіеЇКжДПдєЙгАВ
03
еЃЮй™МжЦєж≥Хе≠¶
BCRseq
еИЖжЮР
04
зїУжЮЬ
1
BзїЖиГЮеЕНзЦЂеЇУжµЛеЇП
еЫЊ1
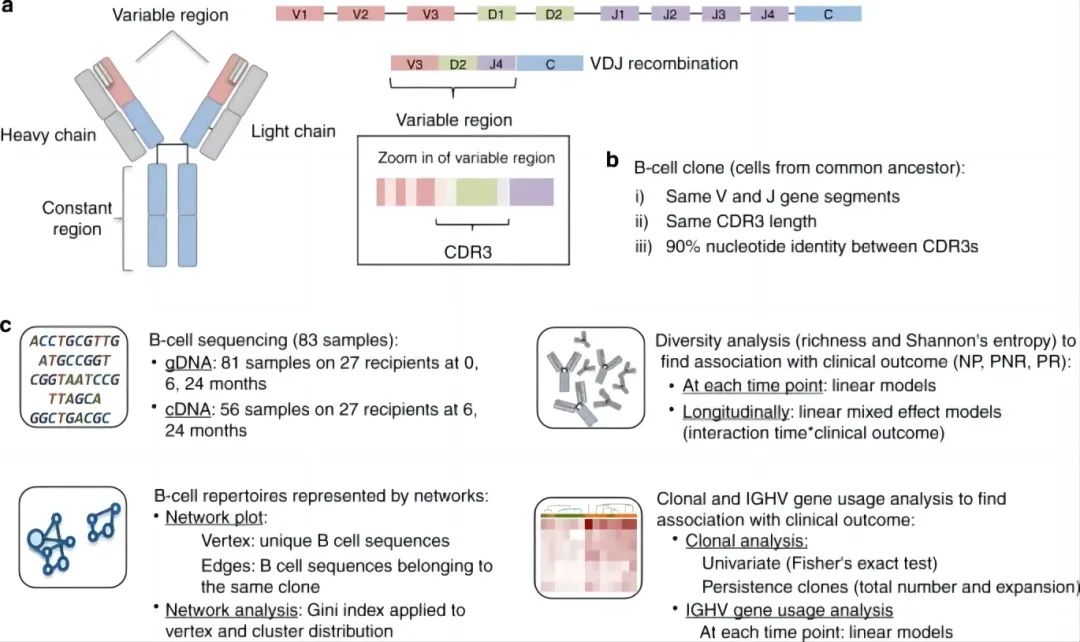
е¶ВеЫЊ1CжЙАз§ЇпЉМдљЬиАЕдљњзФ®зЇњжАІеЫЮељТж®°еЮЛпЉМе∞ЖеЕЛйЪЖжХ∞йЗПжИЦзЖµдљЬдЄЇеЫ†еПШйЗПпЉМдЄіеЇКзїУжЮЬжИЦSHMдљЬдЄЇзЛђзЂЛеЫ†зі†еПШйЗПпЉМиАГиЩСзЙ©зІНдЄ∞еѓМеЇ¶(зЛђзЙєеЕЛйЪЖжХ∞йЗП)еТМй¶ЩеЖЬзЖµ(жЦєж≥ХдЄ≠зЪДжЦєз®Л(1))иЈ®жЧґйЧізВєеТМдЄіеЇКзїУжЮЬпЉМж£АжЯ•дЇЖBзїЖиГЮеЕНзЦЂеЇУе§Ъж†ЈжАІгАВ
2
зІїж§НеЙНBзїЖиГЮе§Ъж†ЈжАІдЄОиВЊеЩ®еЃШжОТжЦ•еПНеЇФжЬЙеЕ≥гАВ
еЫЊ2
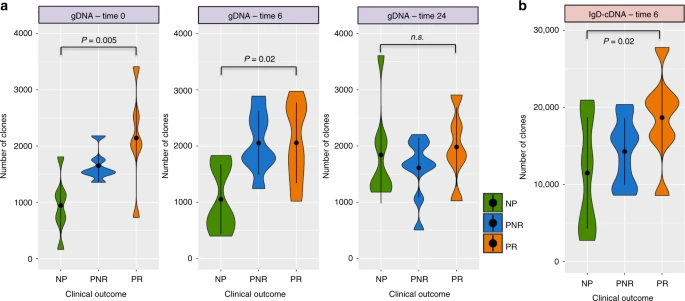
иВЊзІїж§НеЙНпЉМPRзїДзЪДеЩ®еЃШе§Ъж†ЈжАІжШЊиСЧйЂШдЇОNPзїД(дЄ∞еѓМеЇ¶:pеАЉ= 0.005пЉМзЖµеАЉ:pеАЉ= 0.01)пЉМзІїж§НеРО6дЄ™жЬИпЉМPRзїДзЪДеЩ®еЃШе§Ъж†ЈжАІдєЯжШЊиСЧйЂШдЇОNPзїД(дЄ∞еѓМеЇ¶:pеАЉ= 0.02пЉМзЖµеАЉ:0.01)гАВpеАЉ= 0.02)пЉМзІїж§НеРО2еєіж≤°жЬЙжШОжШЊзЪДзїДйЧіеЈЃеЉВ(еЫЊ2aеТМи°•еЕЕеЫЊ2)гАВ
зІїж§НеРОзЪДcDNAжµЛеЇПжХ∞жНЃжШЊз§ЇпЉМзІїж§НеРО6дЄ™жЬИзЪДеЕНзЦЂеЇУе§Ъж†ЈжАІдєЯжЬЙеРМж†ЈзЪДиґЛеКњпЉМдЄїи¶БжШѓIgDеРМзІНеЮЛ(дЄ∞еѓМеЇ¶:pеАЉ= 0.02пЉМзЖµеАЉ:pеАЉ= 0.03)(еЫЊ2bеТМи°•еЕЕеЫЊ2)гАВ
дЄНеРМзЪДдЇЇеП£зїЯиЃ°е≠¶еТМдЄіеЇКеПШйЗПпЉМе¶ВеПЧдљУеєійЊДгАБжАІеИЂгАБзІНжЧПгАБдЊЫдљУжЭ•жЇРгАБеЕНзЦЂжКСеИґз±їеЮЛгАБHLAйФЩйЕНеТМиВЊеКЯиГљи°∞зЂ≠зЪДеОЯеЫ†з≠ЙжХ∞жНЃж≤°жЬЙжЈЈжЭВжХИеЇФгАВзФ±дЇО1е≤БеДњзЂ•(жХ∞жНЃдЄ≠зЪДжЬАе∞ПеєійЊД)еТМ19е≤БеДњзЂ•(жХ∞жНЃдЄ≠зЪДжЬАе§ІеєійЊД)зЪДBзїЖиГЮеПНеЇФдЄНеРМпЉМйЪПеРОињЫи°МдЇЖжОТйЩ§ињЩдЄ§еРНжВ£иАЕзЪДжХПжДЯжАІеИЖжЮРпЉМзїУжЮЬдїНзДґжШЊиСЧ(NP vs. PRеЬ®жЧґйЧі0:дЄ∞еѓМеЇ¶:pеАЉ= 0.01пЉМзЖµеАЉ:pеАЉ= 0.03)гАВеЬ®еЕНзЦЂеЇУе§Ъж†ЈжАІзЪДеП¶дЄАй°єжµЛйЗПдЄ≠пЉМйАЪињЗиѓДдЉ∞SHMпЉМеЃЪдєЙдЇЖжѓПдЄ™VеЯЇеЫ†зЙЗжЃµзЪДз™БеПШйҐСзОЗпЉМеПСзО∞зІїж§НеЙНPRзЪДSHMжХ∞йЗПеСИиЊГйЂШиґЛеКњпЉМзІїж§НеРО6дЄ™жЬИPRзЪДIgDеРМеЮЛSHMжХ∞йЗПеСИиЊГйЂШиґЛеКњ(pеАЉ= 0.06)гАВ
3
BзїЖиГЮе§Ъж†ЈжАІдЄіеЇКзїУжЮЬдЉЪйЪПжЧґйЧіеПШеМЦгАВ
еЫЊ3
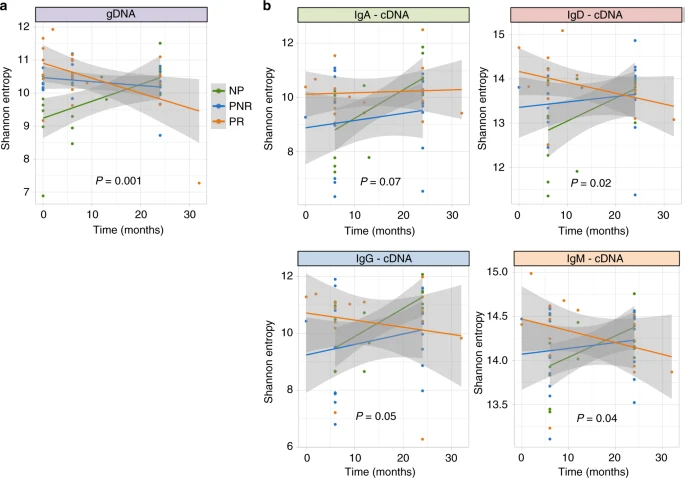
еЕНзЦЂеЇУе§Ъж†ЈжАІдЄіеЇКзїУжЮЬеПѓиГљйЪПзЭАжЧґйЧізЪДжО®зІїиАМжФєеПШпЉМиАГиЩСдЄіеЇКзїУжЮЬеТМжЧґйЧідєЛйЧіе≠ШеЬ®зЫЄдЇТдљЬзФ®пЉМдљЬиАЕдљњзФ®зЇњжАІжЈЈеРИжХИеЇФж®°еЮЛеѓєзЇµеРСжХ∞жНЃињЫи°МеїЇж®°гАВ
зїУжЮЬеПСзО∞пЉМNPеТМPRеЬ®зІїж§НеРОзЪДдЄНеРМжЧґйЧіи°®зО∞дЄНеРМпЉМNPзЪДе§Ъж†ЈжАІеҐЮеК†пЉМPRзЪДе§Ъж†ЈжАІеЗПе∞СпЉМиАМPNRзЪДе§Ъж†ЈжАІеЬ®дЄНеРМжЧґйЧідњЭжМБдЄНеПШгАВињЩеЬ®gDNA(дЄ∞еѓМеЇ¶:pеАЉ=0.007пЉМзЖµеАЉ:pеАЉ=0.001пЉМеЫЊ3a)еТМcDNAзЪДжЙАжЬЙеРМеЮЛдЄ≠йГљиІВеѓЯеИ∞дЇЖпЉМеЕґдЄ≠IgMеТМIgDзЪДзЖµеАЉеЈЃеЉВжЬАжШЊиСЧ(IgA: pеАЉ=0.07,IgD: pеАЉ=0.02,IgG: pеАЉ=0.05,IgM: pеАЉ=0.04пЉМеЫЊ3b)гАВ
еЕЈжЬЙзЫЄеЇФpеАЉзЪДдЄ∞еѓМеЇ¶еЫЊе¶ВеЫЊ3жЙАз§ЇгАВе¶ВеЫЊдЄ≠жЙАз§ЇпЉМжѓПдЄ™дЇЇеЬ®32дЄ™жЬИзЪДжЧґеАЩе≠ШеЬ®е§ЪеЗЇзЪДж†ЈжЬђпЉМињЩдЇЫж†ЈжЬђеПѓиГљдЉЪжЙ≠жЫ≤зїУжЮЬпЉМеЫ†ж≠§ињЫи°МжХПжДЯжАІеИЖжЮРпЉМе∞Жиѓ•ж†ЈжЬђдїОеИЖжЮРдЄ≠жОТйЩ§пЉМеєґиІВеѓЯеИ∞йЩ§дЇЖIgGеТМIgMдЇЪеЮЛе§ЦзЪДз±їдЉЉзїУжЮЬпЉМеЈ≤зїПж≤°жЬЙжДПдєЙ(gDNA-зЖµ:pеАЉ=0.004)гАВcDNA entropy: IgA: pеАЉ=0.1,IgD: pеАЉ=0.05,IgG: pеАЉ=0.08,IgM: pеАЉ=0.1)гАВ
4
BзїЖиГЮзљСзїЬеЬ®еЕЛйЪЖжЙ©еҐЮдЄКе≠ШеЬ®еЈЃеЉВ
еЫЊ4
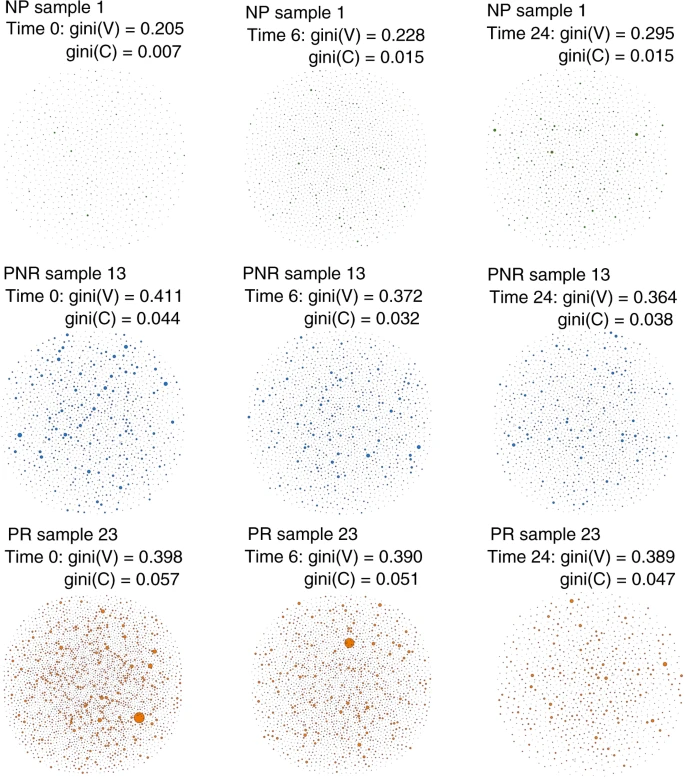
BзїЖиГЮеЇУеПѓдї•е±Хз§ЇдЄЇеЇПеИЧе§Ъж†ЈжАІзЪДзљСзїЬгАВеЬ®жХ∞жНЃдЄ≠пЉМдљЬиАЕдЄЇжѓПдЄ™ж†ЈжЬђеЉАеПСдЇЖдЄАдЄ™иІЖиІЙзљСзїЬ(еЫЊ4еТМи°•еЕЕеЫЊ5-7)пЉМеЕґдЄ≠жѓПдЄ™й°ґзВєдї£и°®дЄАдЄ™еФѓдЄАзЪДBCRпЉМеєґдЄФеЯЇдЇОеЕґж†ЄиЛЈйЕЄеЇПеИЧзЪДзЫЄеРМBCRзЪДжХ∞йЗПеЃЪдєЙдЇЖй°ґзВєе§Іе∞ПгАВ
ељУеЃГдїђе±ЮдЇОеРМдЄАдЄ™еЕЛйЪЖжЧґпЉМй°ґзВєдєЛйЧіе≠ШеЬ®дЄАжЭ°иЊєпЉМеЫ†ж≠§BзїЖиГЮйЫЖзЊ§еПѓдї•жШЊз§ЇдЄЇдЄАзїДзЫЄдЇТињЮжО•зЪДй°ґзВєпЉМ嚥жИРдЄАдЄ™еЕЛйЪЖгАВдЄЇдЇЖйЗПеМЦзљСзїЬпЉМдљњзФ®дЇЖеЯЇе∞ЉжМЗжХ∞пЉМињЩжШѓдЄАзІНеЇФзФ®дЇОй°ґзВєеТМиБЪз±їеИЖеЄГзЪДдЄНеЭЗеМАеЇ¶йЗПгАВељУеЇФзФ®дЇОй°ґзВєе§Іе∞ПGini(V)жЧґпЉМи°®з§ЇжХідљУеЕЛйЪЖжАІиі®гАВе¶ВжЮЬGini(V)жО•ињСдЇО1пЉМй°ґзВєжШѓдЄНзЫЄз≠ЙзЪДпЉМи°®жШОеЕґдЄ≠дЄАдЇЫй°ґзВєжШѓжЙ©е±ХзЪДпЉМеР¶еИЩжО•ињСдЇО0гАВељУеЇФзФ®дЇОз∞Зе§Іе∞ПжЧґпЉМеЯЇе∞Љ(C)и°®з§ЇеЕЛйЪЖдЉШеКњгАВе¶ВжЮЬжО•ињС1пЉМйЫЖзЊ§жШѓдЄНзЫЄз≠ЙзЪДпЉМеЫ†ж≠§дї£и°®дЉШеКњеЕЛйЪЖпЉМе¶ВжЮЬжО•ињС0пЉМжЙАжЬЙйЫЖзЊ§е§Іе∞ПзЫЄз≠ЙгАВ
еЬ®еЫЊ4дЄ≠пЉМе±Хз§ЇдЇЖдЄЙдЄ™дЄіеЇКзїУжЮЬзїДеЬ®дЄЙдЄ™дЄНеРМжЧґйЧізВє(зІїж§НеЙНгАБзІїж§НеРО6дЄ™жЬИеТМ24дЄ™жЬИ)дї£и°®жАІBзїЖиГЮеЇУдєЛйЧіиІЖиІЙеТМжХ∞йЗПжШЊиСЧеЈЃеЉВгАВеЬ®PRеЇУдЄ≠пЉМдЄОNPзЫЄжѓФпЉМе§ІйЗП嚥жИРжЫіе§ЪжЫіе§ІеЕЛйЪЖз∞ЗзЪДBзїЖиГЮеЇПеИЧе≠ШеЬ®пЉМиАМPNRдљНдЇОдЄ§иАЕдєЛйЧігАВйЪПзЭАжЧґйЧізЪДжО®зІїпЉМPRзїДдЄОNPзїДзЫЄжѓФпЉМBCRеТМзЙєжЃКеЕЛйЪЖзЪДжХ∞йЗПжЬЙжЙАеЗПе∞СгАВжЬђз†Фз©ґдЄ≠жѓПдЄ™дЄ™дљУзЪДиѓ¶зїЖBзїЖиГЮзљСзїЬе¶ВеЫЊ5-7жЙАз§ЇгАВеЬ®NPзїДеПСзФЯPTLDзЪДдЄ™дљУдЄ≠пЉМиІВеѓЯеИ∞йЭЮеЄЄе§Ъж†ЈеМЦзЪДBзїЖиГЮзљСзїЬж®°еЉП(и°•еЕЕеЫЊ5)пЉМзІїж§НеЙНж≤°жЬЙBзїЖиГЮжЙ©еҐЮпЉМ6дЄ™жЬИеРОBзїЖиГЮеҐЮеК†пЉМзІїж§НеРО24дЄ™жЬИеЗЇзО∞жШОжШЊзЪДеЕЛйЪЖжЙ©еҐЮпЉМеРМжЧґе§Ъж†ЈжАІдЄЛйЩНгАВ
еЫЊ5
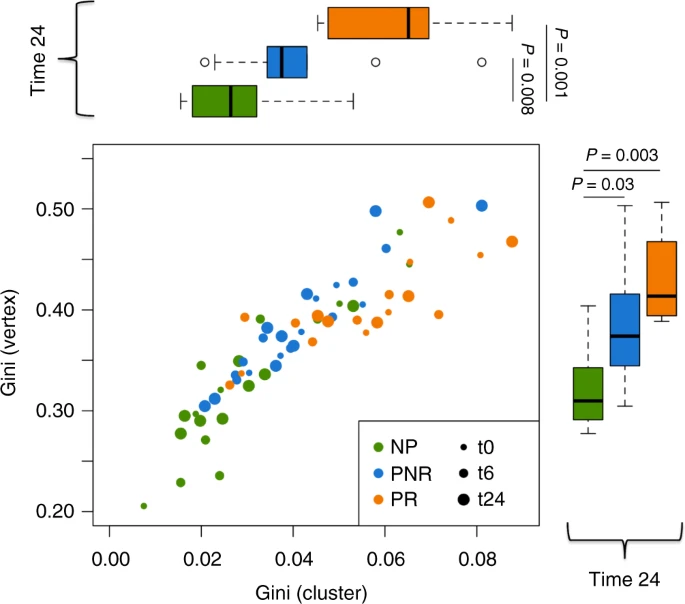
еЬ®еЯЇе∞ЉжМЗжХ∞жµЛйЗПзЪДињЫдЄАж≠•иѓДдЉ∞дЄ≠(еЫЊ5)пЉМPRзїДеЬ®й°ґзВєеТМз∞ЗзЪДжµЛйЗПеАЉеЭЗжШОжШЊйЂШдЇОNPзїДпЉМињЩи°®жШОPRзїДжВ£иАЕеЬ®еЯЇзЇњжЧґеЕЈжЬЙжЫійЂШзЪДеЕЛйЪЖжЙ©еҐЮгАВ
дї•еПКзІїж§НеРОдЉШеКњеЕЛйЪЖе≠РйЫЖзЪДињЫдЄАж≠•жЙ©е±Х(pеАЉ[зЇњжАІеЫЮељТ]<0.05пЉМеЫЊ5)гАВе¶ВеЙНжЙАињ∞пЉМPNRзїДдїЛдЇОNPеТМPRдєЛйЧіпЉМе∞љзЃ°еЬ®time24жЧґпЉМињЩдЄАжЧґйЧідЄОNPзїДжЬЙжШЊиСЧеЈЃеЉВ(pеАЉ[зЇњжАІеЫЮељТ]<0.05)гАВиЩљзДґеЫЊ5зЪДжХ∞жНЃжШѓзФ±gDNAжХ∞жНЃзФЯжИРзЪДпЉМдљЖcDNAзЪДIgMеРМеЮЛжШЊз§ЇеЗЇзЫЄеРМзЪДеЈЃеЉВ(pеАЉ[зЇњжАІеЫЮељТ]=0.05)(и°•еЕЕеЫЊ8)гАВ
5
жЯРдЇЫеЕЛйЪЖеТМIGHVеЯЇеЫ†дЄОеЩ®еЃШжОТжЦ•еПНеЇФжЬЙеЕ≥гАВ
дљЬиАЕдЄНдїЕйАЪињЗдЄіеЇКзїУжЮЬжЭ•жППињ∞BзїЖиГЮеЇУпЉМињШжПРдЊЫзІїж§НеЙНеТМзІїж§НеРОеЕНзЦЂеПНеЇФзЪДеЕ®е±АеЫЊеГПпЉМжХ∞жНЃдєЯдљњдљЬиАЕиГље§ЯеЬ®еЕЛйЪЖеТМIGHVеЯЇеЫ†ж∞іеє≥дЄКињЫи°МIgеЇПеИЧзЙєеЉВжАІеИЖжЮРгАВ
еѓєдЇОеЕЛйЪЖеИЖжЮРпЉМйАЪињЗиѓДдЉ∞дЇЖжѓПдЄ™жЧґйЧізВєе≠ШеЬ®жИЦдЄНе≠ШеЬ®жѓПдЄ™зЙєеЃЪеЕЛйЪЖ(еЕ±118,223дЄ™еЕЛйЪЖ)дЄОдЄіеЇКзїУжЮЬ(PR, PNR, NR)зЪДеЕ≥з≥їгАВеЇФзФ®Fisherз≤Њз°Ѓж£Ай™МпЉМеИЖеИЂеПСзО∞8дЄ™гАБ4дЄ™еТМ21дЄ™еЕЛйЪЖеЬ®еРНдєЙдЄКдЄО0гАБ6еТМ24дЄ™жЬИзЪДдЄіеЇКзїУжЮЬзЫЄеЕ≥(и°•еЕЕи°®1)гАВдљЖж≤°жЬЙдЄАдЄ™еЕЛйЪЖйАЪињЗе§Ъжђ°жµЛиѓХдњЃж≠£пЉМзФ±дЇОеЬ®еЕЈжЬЙжХ∞еНГдЄ™еПВжХ∞(еЕЛйЪЖ)зЪДеИЖжЮРдЄ≠ж†ЈжЬђйЗПжЬЙйЩРпЉМжЙАдї•зЉЇдєПжЬЙжХИжАІгАВеПѓдї•иІВеѓЯеИ∞пЉМеП™жЬЙPRзїДжВ£иАЕдєЛйЧіе≠ШеЬ®е∞СжХ∞жО•ињСжШЊиСЧжАІ(pеАЉ< 0.05)зЪДеЕЛйЪЖпЉМеєґеЬ®зІїж§НеРО24дЄ™жЬИеѓМйЫЖгАВ
дљЬиАЕињШиАГиЩСдЇЖеЬ®жѓПдЄ™дЄіеЇКзїУжЮЬдЄ≠жШѓеР¶жЬЙдЄАдЇЫеЕЛйЪЖеЬ®йЗЗж†ЈжЧґйЧіеЖЕжМБзї≠е≠ШеЬ®пЉМиАМдЄНжШѓеЕґдїЦеЕЛйЪЖ(и°•еЕЕеЫЊ9)гАВиАГиЩСдЇЖдЄ§зІНдЄНеРМзЪДжµЛйЗПжЦєж≥Х:(1)жМБзї≠еЕЛйЪЖзЪДжХ∞йЗПеТМ(2)еЕЛйЪЖжЙ©еҐЮгАВиІВеѓЯеИ∞пЉМеЬ®PRдЄ≠жМБзї≠е≠ШеЬ®зЪДжЧ†жАІз≥їжХ∞йЗПжШЊиСЧеҐЮеК†(pеАЉ[зЇњжАІеЫЮељТ]= 0.01,PR vs. NP)пЉМеєґеСИзО∞еЗЇжМБзї≠е≠ШеЬ®жЧ†жАІз≥їжХ∞йЗПеҐЮеК†зЪДиґЛеКњ(pеАЉ[зЇњжАІеЫЮељТ]= 0.09)гАВ
йАЪињЗињЫдЄАж≠•з†Фз©ґдЇЖеЬ®жѓПдЄ™дЄіеЇКзїУжЮЬпЉМињЩдЇЫжМБдєЕеЕЛйЪЖеПѓиГље≠ШеЬ®дЄНеРМдЄ™дљУдєЛйЧіеЕ±дЇЂгАВеЬ®ж£АжµЛеИ∞зЪД263дЄ™жМБдєЕжАІеЕЛйЪЖдЄ≠пЉМжЬЙ23дЄ™жШѓиЈ®дЄ™дљУеЕ±дЇЂзЪДгАВ5дЄ™еЬ®еРМдЄАPNRдЄ≠еЕ±дЇЂпЉМ6дЄ™еЬ®PRзїДдЄ≠еЕ±дЇЂпЉМNPзїДдєЛйЧіж≤°жЬЙеЕ±дЇЂеЕЛйЪЖгАВжАїзЪДжЭ•иѓіпЉМйЪПзЭАжЧґйЧізЪДжО®зІїпЉМдЄ§зїДињЫи°МжАІжЕҐжАІзІїж§НжНЯдЉ§еТМзЇ§зїіеМЦжВ£иАЕ(PRеТМPNR)еЕ±жЬЙ12дЄ™еЕ±дЇЂеЕЛйЪЖгАВ
жО•дЄЛжЭ•ињЫи°МIGHVеЯЇеЫ†еИЖжЮРпЉМжЯ•зЬЛжѓПдЄ™ж†ЈжЬђзЪДIGHVеЯЇеЫ†дљњзФ®жГЕеЖµпЉМеЃЪдєЙжѓПдЄ™IGHVеЯЇеЫ†дљњзФ®зЪДжђ°жХ∞пЉМйАЪињЗеЕЛйЪЖжХ∞йЗПељТдЄАеМЦ(дї•йБњеЕНжЯРдЇЫIGHVеЯЇеЫ†зЪДйЗЗж†ЈеБПеЈЃ)пЉМињЗжї§жОЙдљОи°®иЊЊеЯЇеЫ†(иЗ≥е∞С10%зЪДж†ЈжЬђдЄ≠IGHVеЯЇеЫ†дљњзФ®> 0.05)пЉМеєґеЇФзФ®зЇњжАІеЫЮељТж®°еЮЛеЬ®жѓПдЄ™жЧґйЧізВєжЙЊеИ∞дЄОжѓПдЄ™дЄіеЇКзїУжЮЬзЫЄеЕ≥зЪДеЯЇеЫ†гАВ
еЫЊ6
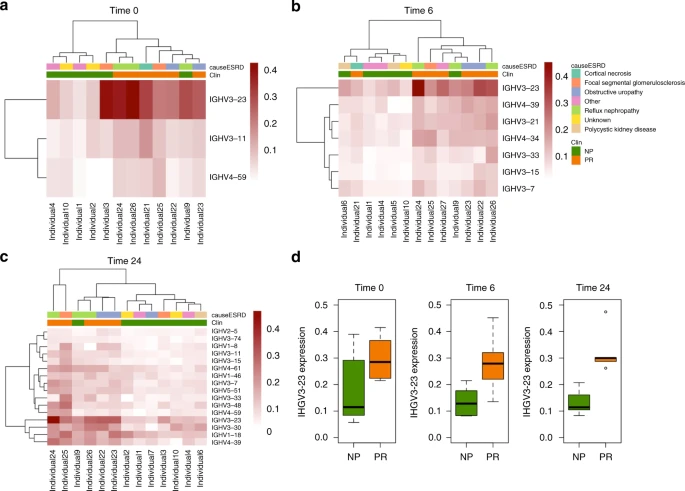
дїО27дЄ™дљОи°®иЊЊIGHVеЯЇеЫ†дЄ≠з≠ЫйАЙпЉМеПСзО∞PRзїДеТМNPзїДдєЛйЧіе≠ШеЬ®жШЊиСЧеЯЇеЫ†(pеАЉ< 0.05)пЉМеЕґдЄ≠time 0жЬЙ3дЄ™еЯЇеЫ†,time 6жЬЙ7дЄ™еЯЇеЫ†,time 24жЬЙ16дЄ™еЯЇеЫ†(еЫЊ6a-c)гАВеЬ®ињЩдЇЫеЯЇеЫ†дЄ≠пЉМзђђ0жЧґжЬЙ1дЄ™еЯЇеЫ†(IGHV3-11)пЉМзђђ6жЧґжЬЙ5дЄ™еЯЇеЫ†(IGHV3-7гАБIGHV3-15гАБIGHV3-21гАБIGHV3-23гАБIGHV4-39)пЉМзђђ24жЧґжЬЙ16дЄ™еЯЇеЫ†(IGHV1-8гАБIGHV1-18гАБIGHV1-46гАБIGHV25гАБIGHV3-7гАБIGHV3-11гАБIGHV3-15гАБIGHV3-30гАБIGHV3-33гАБIGHV3-74гАБIGHV4-39гАБIGHV4-59гАБIGHV4-61гАБIGHV5-51)гАВ
йАЪињЗдЇЖйФЩиѓѓеПСзО∞зОЗ(FDR)е§Ъжђ°ж£АжµЛж†°ж≠£гАВеПСзО∞еЬ®NPдЄОPRзЪДжѓФиЊГдЄ≠пЉМIGHV3-23еЬ®жЙАжЬЙдЄЙдЄ™жЧґйЧізВєдЄКйГљжШѓжЬАжШЊиСЧеТМжЬАдЄ∞еѓМзЪДеЯЇеЫ†(жЧґйЧі0:pеАЉ=0.04пЉМжЧґйЧі6:pеАЉ=0.003пЉМжЧґйЧі24:pеАЉ=0.02)(еЫЊ6d)гАВ
ж≠§е§ЦпЉМдЄЇдЇЖиѓДдЉ∞дєЛеЙНеЕЛйЪЖеИЖжЮРдЄ≠еЕ±дЇЂеЇПеИЧIGHV3-23еЇПеИЧињЗеЇ¶и°®иЊЊгАВдљњзФ®Fisherз≤Њз°Ѓж£Ай™МзЪДеѓМйЫЖеИЖжЮРпЉМIGHV3-23еЇПеИЧеЬ®дЄ™дљУйЧіеЕ±дЇЂзЪДжМБдєЕеЕЛйЪЖ(и°•еЕЕи°®2)(pеАЉ<2.2√Ч10вИТ16)еТМзђђ24жЧґйЧідЄіеЇКзїУжЮЬзЫЄеЕ≥зЪДеЕЛйЪЖ(и°•еЕЕи°®1)(pеАЉ<2.2√Ч10вИТ16)дЄ≠еЭЗжШЊиСЧи°®иЊЊгАВйАЪињЗиІВеѓЯеИ∞NRзїДдЄ≠зЪДдЄ™дљУ9пЉМеЬ®дєЛеЙНзЪДеИЖжЮРдЄ≠еПСзО∞дЄОињЫе±ХиАЕеЕ±дЇЂдЄАдЇЫжМБдєЕеЕЛйЪЖпЉМеЬ®жЙАжЬЙжЧґйЧізВєйГљељТдЄЇPRзїДгАВдЄНеРМзЪДдЇЇеП£зїЯиЃ°е≠¶еТМдЄіеЇКеПШйЗПпЉМе¶ВеПЧдљУеєійЊДгАБжАІеИЂгАБзІНжЧПгАБдЊЫдљУжЭ•жЇРгАБеЕНзЦЂжКСеИґз±їеЮЛгАБHLAйФЩйЕНеТМиВЊеКЯиГљи°∞зЂ≠зЪДеОЯеЫ†з≠ЙжХ∞жНЃж≤°жЬЙжЈЈжЭВжХИеЇФгАВж≠§е§ЦпЉМиѓ•еЯЇеЫ†еЬ®зІїж§НеРО24дЄ™жЬИеЯЇдЇОcDNAзЪДIgM (pеАЉ[зЇњжАІеЫЮељТ]=0.008)еТМIgD (pеАЉ[зЇњжАІеЫЮељТ]=0.05)еРМеЮЛдЄ≠дєЯжШЊиСЧе≠ШеЬ®пЉМдЄОдєЛеЙНзЪДзїУжЮЬдЄАиЗіпЉМPRзїДдЄ≠ињЩдЄ§дЄ™еРМеЮЛзЪДеѓМйЫЖз®ЛеЇ¶жЬАйЂШгАВеЬ®IgDеТМIgMеРМзІНеЮЛдЄ≠пЉМеП™жЬЙ3дЄ™еЯЇеЫ†еЬ®зІїж§НеРО24дЄ™жЬИзЪДcDNAеИЖжЮРдЄ≠еЕЈжЬЙжШЊиСЧжАІ(IgDдЄ≠зЪДIGHV3-15еТМIGHV461, IgMдЄ≠зЪДIGHV4-39)гАВ
05
иЃ®иЃЇ
дљЬиАЕзЪДжХ∞жНЃжШЊз§ЇпЉМеЬ®дЄ™дљУдЄ≠зІїж§НеЙНе§Ъж†ЈжАІиґКйЂШпЉМе≠ШеЬ®жОТжЦ•еАЊеРСиґКйЂШпЉМињЩеѓєйҐДжµЛзІїж§НеЙНжОТжЦ•й£ОйЩ©пЉМеЕНзЦЂжКСеИґйАЙжЛ©еТМдЄіеЇКжК§зРЖеЃЮиЈµеЕЈжЬЙйЗНи¶БзЪДжДПдєЙгАВзїПињЗ24дЄ™жЬИзЪДйЪПиЃњпЉМеЬ®жОТжЦ•зїДдЄ≠иІВеѓЯеИ∞йЪПзЭАжЧґйЧізЪДжО®зІїпЉМе§Ъж†ЈжАІжАїдљУеЗПе∞СпЉМеРМжЧґжЯРдЇЫеЕЛйЪЖзЪДжМБзї≠е≠ШеЬ®еТМжЙ©еҐЮпЉМдї•еПКеЗ†зІНIGHVеЯЇеЫ†зЪДйЂШдљњзФ®пЉМињЩдєЯжЪЧз§ЇдЇЖзЙєеЃЪзЪДеЕ±еРМжКЧеОЯеПѓиГљеѓЉиЗіжОТжЦ•гАВйЬАи¶БзЙєеИЂеЕ≥ж≥®зЪДжШѓIGHV3-23еЯЇеЫ†зЪДеЬ®жОТжЦ•жВ£иАЕдЄ≠дљњзФ®еҐЮеК†пЉМеЫ†дЄЇеЃГдї•еЙНдЄОиВЊзІїж§НжЬЙеЕ≥пЉМеєґдЄФдєЯжШѓеПѓиГљеѓЉиЗіжОТжЦ•ињЗз®ЛзЪДйЗНи¶БзїДжИРйГ®еИЖгАВжЬђз†Фз©ґеѓєеЩ®еЃШзІїж§НдЄ≠зЪДBзїЖиГЮеЕНзЦЂеЇУињЫи°МдЇЖеИЖжЮРпЉМињРзФ®дЇЖжЫіе§ЪзЪДз†Фз©ґжЭ•иѓБеЃЮињЩдЇЫеПСзО∞пЉМеЫ†дЄЇеЃГдїђеПѓиГљеЬ®йҐДжµЛгАБжОІеИґгАБзЫСжµЛеТМж≤їзЦЧиВЊжОТжЦ•еПНеЇФжЦєйЭҐеЕЈжЬЙдЄіеЇКжДПдєЙгАВ
#2

ж†ЗйҐШпЉЪEffects of Reduced-Dose Anti-Human¬†T-Lymphocyte Globulin on Overall¬†and Donor-Specific T-Cell Repertoire¬†Reconstitution in Sensitized Kidney¬†Transplant Recipients
дљОеЙВйЗПжКЧдЇЇTжЈЛеЈізїЖиГЮзРГиЫЛзЩљеѓєжКЧдљУжХПжДЯзЪДиВЊзІїж§НеПЧиАЕжХідљУеТМдЊЫиАЕзЙєеЉВжАІTзїЖиГЮеЇУйЗНеїЇзЪДељ±еУН
еПСи°®жЬЯеИКпЉЪFrontiers in Immunology
еПСи°®жЧ•жЬЯпЉЪ2022еєі2жЬИ
ељ±еУНеЫ†е≠РпЉЪ8.79
01
ж†ЈжЬђ
еѓє5дЊЛжО•еПЧ1.5 mg/kg ATLGиѓ±еѓЉж≤їзЦЧ7姩зЪДиВЊзІїж§НеПЧиАЕеТМ5дЊЛжО•еПЧ2 √Ч 20 mg basiliximabпЉИеЈіеИ©жШФеНХжКЧпЉЙиѓ±еѓЉж≤їзЦЧзЪДжВ£иАЕпЉМеЬ®зІїж§НеЙНеТМзІїж§НеРО1гАБ3еТМ12дЄ™жЬИеЖЕе§ЦеС®еНХж†ЄзїЖиГЮеПЦж†ЈгАВ
02
иГМжЩѓ
иВЊзІїж§НеЙНеЈ≤襀иЗіжХПзЪДжВ£иАЕеЬ®иВЊзІїж§НеРОеПСзФЯжОТжЦ•еПНеЇФзЪДй£ОйЩ©жЫійЂШпЉМеЫ†ж≠§жО•еПЧжКЧдЇЇTжЈЛеЈізїЖиГЮзРГиЫЛзЩљ(ATLG)зЪДжЈЛеЈіжґИиАЧиѓ±еѓЉж≤їзЦЧпЉМиАМиЃЄе§ЪеЬ∞жЦє,йЭЮиЗіжХПзЪДжВ£иАЕеИЩжО•еПЧbasiliximabпЉИеЈіеИ©жШФеНХжКЧпЉЙзЪДиѓ±еѓЉж≤їзЦЧгАВзДґиАМпЉМеЕНзЦЂзїЖиГЮеЖНзФЯзЪДжЧґйЧіеТМжХідљУдї•еПКеѓєдЊЫдљУеПНеЇФжАІTзїЖиГЮеПЧдљУ(TCR)зЙєеЉВжАІзЪДељ±еУНдїНдЄНжЄЕж•ЪгАВ
03
еЃЮй™МжЦєж≥Хе≠¶
aпЉЙTзїЖиГЮи°®еЮЛзЙєеЊБеИЖжЮР
bпЉЙжЈЈеРИжЈЛеЈізїЖиГЮеПНеЇФпЉИMLRпЉЙ
cпЉЙTCRжµЛеЇП
dпЉЙзЙєеЉВжАІиѓЖеИЂ
eпЉЙзїЯиЃ°жЦєж≥Х
04
зїУжЮЬ
1
жХідљУеТМдЊЫдљУеПНеЇФжАІTCRеЕНзЦЂеЇУ
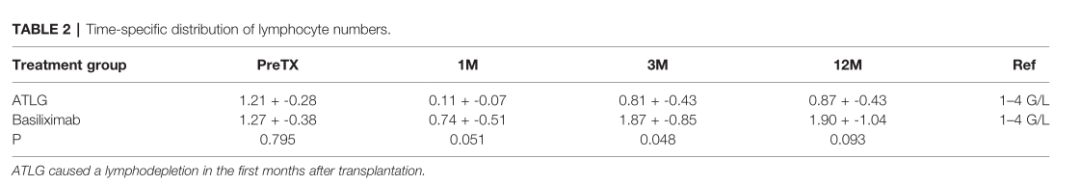
иВЊзІїж§НеРОиѓ±еѓЉж≤їзЦЧеРОпЉМATLGзїДеЬ®зђђдЄАдЄ™жЬИеЖЕеє≥еЭЗжЈЛеЈізїЖиГЮиАЧжНЯиЊЊеИ∞0.11+-0.07 G/LгАВйШЯеИЧдЄ≠зЪДжЈЛеЈізїЖиГЮеЗПе∞СзКґжАБжМБзї≠дЇЖиЗ≥е∞С14姩пЉМеЕґдЄ≠2дЊЛжВ£иАЕеЬ®310姩жЈЛеЈізїЖиГЮиЃ°жХ∞жБҐе§НеИ∞>1G/L, 3дЊЛжВ£иАЕеЬ®жХідЄ™иІВеѓЯжЬЯеЖЕжЈЛеЈізїЖиГЮиЃ°жХ∞жМБзї≠еЗПе∞СгАВеЈіеИ©жШФеНХжКЧж≤їзЦЧзїДзЪДжЈЛеЈізїЖиГЮиЃ°жХ∞еЬ®зІїж§НеРОзЪДзђђдЄАдЄ™жЬИдєЯжЬЙжЙАдЄЛйЩНпЉМдљЖеЬ®йЪПеРОзЪДжЧґйЧізВєдЄ≠жЙАжЬЙеПЧиѓХиАЕзЪДжЈЛеЈізїЖиГЮиЃ°жХ∞еЭЗдЄКеНЗиЗ≥>1G/L(и°®2)гАВзІїж§НеРО12дЄ™жЬИйАЪињЗиВЊе∞ПзРГжї§ињЗзОЗ(eGFR)дЉ∞иЃ°зЪДзІїж§НеКЯиГљеЬ®дЄ§зїДдєЛйЧіж≤°жЬЙеЈЃеЉВ(ATLGзїД:64+-18ml/min/1.73m¬≤пЉМеЈіеИ©жШФеНХжКЧж≤їзЦЧзїД:53+-12 ml/min/1.73m¬≤;P=0.23)гАВ
еЫЊ1
йАЪињЗеѓєTCRќ≤йУЊзЪДNGSжµЛеЇПпЉМзІїж§НеРОж£АжµЛеИ∞зЪДTCRеЕЛйЪЖеЮЛзЪДзїЭеѓєжХ∞йЗПдЄОдЄ§зїДзІїж§НеЙНеЬ®жЙАжЬЙжЧґйЧізВєзЫЄељУпЉМCD4зїЖиГЮдЄЇ26,328иЗ≥107,735,CD8 TзїЖиГЮдЄЇ7,184иЗ≥87,533гАВйЗЗж†ЈеРОеЙ©дљЩзЪДеЕЛйЪЖеЮЛжХ∞йЗПе¶ВеЫЊ1жЙАз§ЇгАВ
зїУжЮЬи°®жШОпЉМж≠£е¶ВйҐДжЬЯзЪДйВ£ж†ЈеЬ®дЄ§зїДдЇЇзЊ§дЄ≠пЉМMLRеРОеЃЪдєЙзЪДеЯЇеЫ†еЇУжШЊз§ЇзЪДеЕЛйЪЖеЮЛжХ∞йЗПдљОдЇОжЬ™еИЇжњАзЪДеЯЇеЫ†еЇУгАВ
еЬ®жО•еПЧATLGж≤їзЦЧзЪДйҐДиЗіжХПжВ£иАЕзїДдЄ≠пЉМйАЪињЗFACSеИЖжЮРзЪДTзїЖиГЮи°®еЮЛзЙєеЊБжШЊз§ЇпЉМжВ£иАЕзЪДеЕНзЦЂзїЖиГЮзїДжИРеЕЈжЬЙйЂШеЇ¶еЉВиі®жАІгАВжВ£иАЕеЬ®зІїж§НеЙНеИЭеІЛTзїЖиГЮжХ∞йЗПеЗПе∞СпЉМдЄ≠жЮҐиЃ∞ењЖCD4 TзїЖиГЮжХ∞йЗПеҐЮеК†гАВе§Іе§ЪжХ∞жВ£иАЕињСжЬЯиГЄиЕЇзІїж§НзЙ©жХ∞йЗПдЄЛйЩНпЉМи°®жШОеЗПе∞СеЙВйЗПзЪДATLGиґ≥дї•еЃЮзО∞иГЄиЕЇжЈЛеЈізїЖиГЮзЪДжЄЕйЩ§гАВ
еѓєCD4еТМCD8TзїЖиГЮзЪДеИЖжЮРжШЊз§ЇдЇЖдЄОжЈЛеЈіжґИиАЧиѓ±еѓЉзЦЧж≥ХзЙєеЊБдЄАиЗіпЉМдљЖCD4/CD8жѓФеАЉзЪДеАТзљЃеП™жШѓиљїеЊЃзЪД(и°•еЕЕеЫЊ3-6)гАВ
2
TCRеЕЛйЪЖжАІзЙєеЊБ
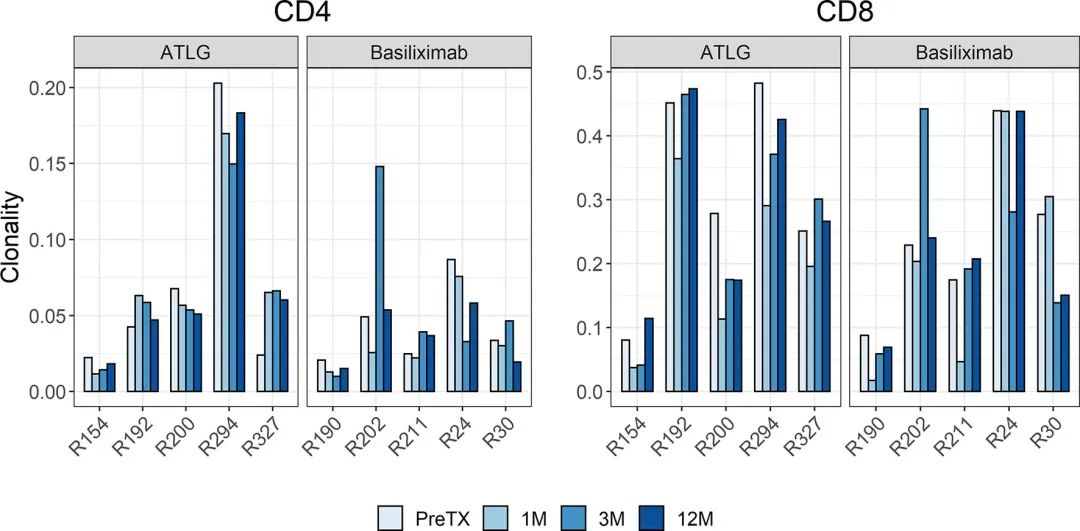
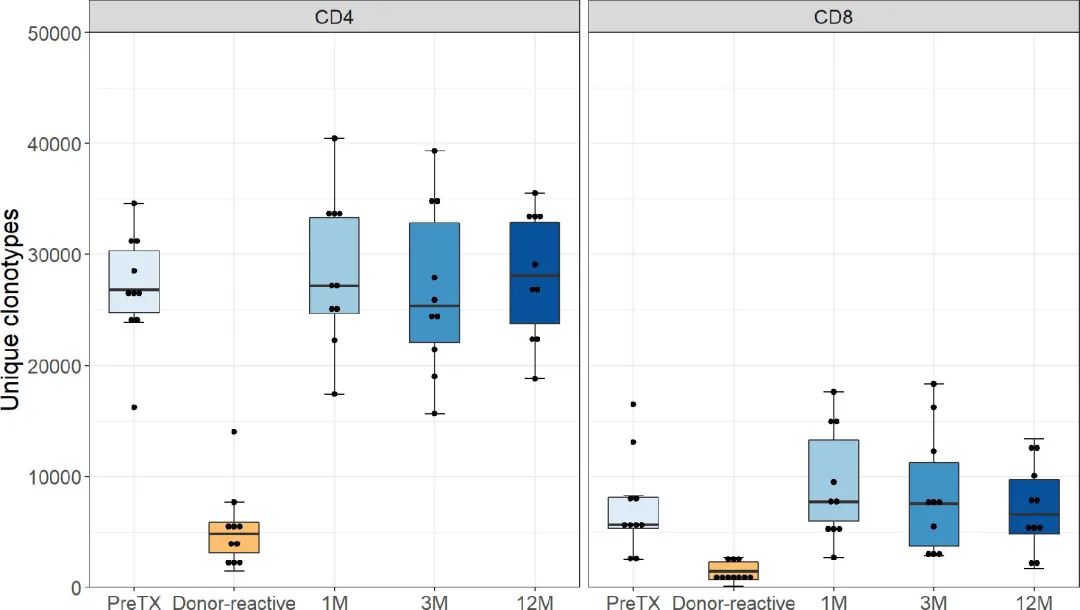
еЫЊ2
TCRзЪДе§Ъж†ЈжАІи°®зО∞еЗЇеєњж≥ЫзЪДдЄ™дљУеЈЃеЉВгАВдЄ§зїДзІїж§НеЙНеЕЛйЪЖжАІжЧ†еЈЃеЉВпЉМATLGзїДCD4еТМCD8 TзїЖиГЮзЪДеЕЛйЪЖжАІеЭЗеАЉеИЖеИЂдЄЇ0.07еТМ0.31,еЈіеИ©жШФеНХжКЧж≤їзЦЧзїДCD4еТМCD8TзїЖиГЮзЪДеЕЛйЪЖжАІеЭЗеАЉеИЖеИЂдЄЇ0.04еТМ0.24гАВзІїж§НеРОж†ЈжЬђзЪДеЕЛйЪЖжАІдњЭжМБдЇЖдЄ™дљУеЈЃеЉВжАІпЉМCD4йШ≥жАІTзїЖиГЮеТМCD8йШ≥жАІTзїЖиГЮйЪПжЧґйЧізЪДеПШеМЦеЬ®дЄ§зїДйЧіжЧ†зїЯиЃ°е≠¶еЈЃеЉВ(CD4:F(1.45, 11.6)=0.64 p= 0.496;CD8: F(3,24)=0.60 p=0.620)(еЫЊ2)гАВ
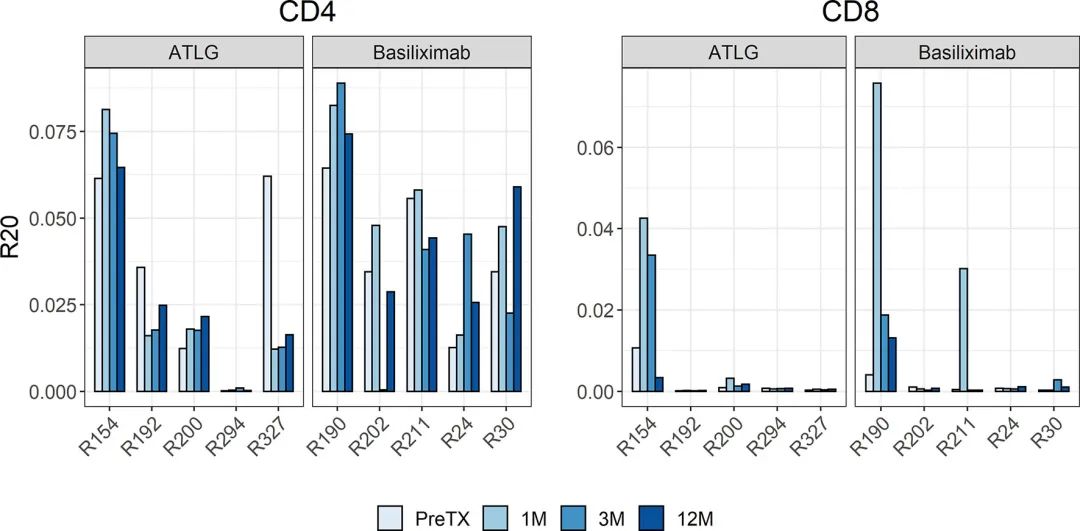
еЫЊ3
R20жµЛйЗПпЉМеЕНзЦЂдЉШеКњзЪДеЇ¶йЗПпЉМжШЊз§ЇдЄ§дЄ™йШЯеИЧж≤°жЬЙеИЖз¶їпЉМи°®жШОеЬ®еЗПе∞СеЙВйЗПATLGж≤їзЦЧеРОпЉМжАїдљУTCRеЇУдЄ≠еЕЛйЪЖдЉШеКњж≤°жЬЙеҐЮеК†(еЫЊ3)гАВиѓ±еѓЉж≤їзЦЧеРОCD4еТМCD8йШ≥жАІTзїЖиГЮзЪДR20жШѓз®≥еЃЪзЪДпЉМеЬ®зІїж§НеРОзЪДжЙАжЬЙжЧґйЧізВєж≤°жЬЙиІВеѓЯеИ∞зїЯиЃ°е≠¶еЈЃеЉВ(CD4: F(3, 24)=0.85 p= 0.479;CD8: F(1.19, 9.52)=0.79, p=0.418)гАВеЬ®ATLGж≤їзЦЧзїДзЪДдЄАдЄ™еПЧиѓХиАЕ(R294)дЄ≠жЬЙдЄАдЄ™йЂШеЇ¶дЄ∞еѓМзЪДеЕЛйЪЖпЉМеН†жХідЄ™TзїЖиГЮеЇУзЪД10%дї•дЄКпЉМеєґдЄФеЬ®зІїж§НеЙНеТМзІїж§НеРОзЪДжѓПдЄ™жЧґйЧізВєйГљжЬЙеПСзО∞пЉМињЩжШѓиѓ•жВ£иАЕдљОR20еАЉзЪДеОЯеЫ†гАВ
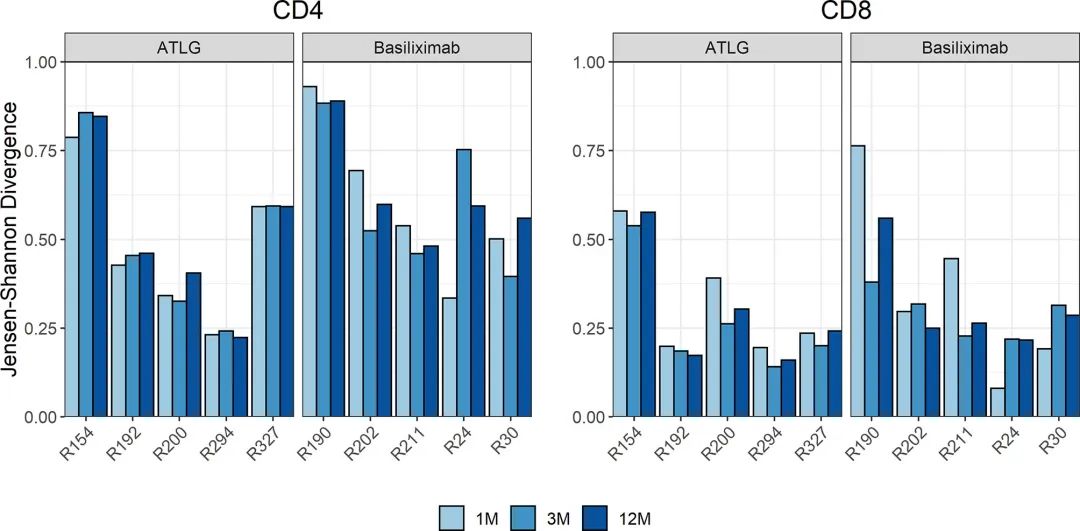
еЫЊ4
йАЪињЗеѓєйЗПATLGзїДдЄОеЈіеИ©жШФеНХжКЧж≤їзЦЧзїДжВ£иАЕеЬ®жЈЛеЈізїЖиГЮйЗНеїЇињЗз®ЛдЄ≠TCRеЇУињЫи°МйЗПеМЦжЭ•иІВеѓЯжАїдљУеС®иљђжШѓеР¶е≠ШеЬ®еЈЃеЉВпЉМињЩе∞ЖзФ±йЂШJSDи°®з§ЇгАВдЄ§зїДеЬ®жЙАжЬЙжЧґйЧізВєжµЛйЗПзЪДJSDеАЉзЫЄдЉЉзІїж§НеРО(еЫЊ4)гАВеЬ®зІїж§НеРОпЉМжО•еПЧATLGж≤їзЦЧзЪДжВ£иАЕдЄОжО•еПЧеЈіеИ©жШФеНХжКЧж≤їзЦЧзЪДжВ£иАЕзЫЄжѓФпЉМеєґж≤°жЬЙзїПеОЖжЫійЂШзЪДеЕНзЦЂз≥їзїЯе§НеОЯзОЗгАВ
еЫЊ5
еРМж†ЈпЉМTCRпЉИTзїЖиГЮеПЧдљУпЉЙеЇУдЄ≠зЪДVJзїДеРИеЬ®иѓ±еѓЉж≤їзЦЧеЙНеРОзЪДеПШеМЦеЬ®дЄ§зїДдєЛйЧідєЯзЫЄдЉЉгАВдЄОжАїдљУTCRеЇУзЫЄжѓФпЉМCD4еТМCD8зЪДVJзїДеРИзЪДиљђжНҐеЈЃеЉВдїОеЯЇзЇњеЉАеІЛиЊГдљОпЉМеє≥еЭЗJSDеИЖеИЂдЄЇ0.02еТМ0.07гАВеЫЊ5жШЊз§ЇдЇЖATLGиѓ±еѓЉзїДдЄАеРНеЕЄеЮЛжВ£иАЕзІїж§НеЙНеТМзІїж§НеРОзђђдЄАдЄ™жЬИзЪДVJиБФеРИдљњзФ®жГЕеЖµгАВзДґиАМпЉМеѓєзІїж§НеРОеЄЄиІБзЧЕжѓТжДЯжЯУзЪДеЈ®зїЖиГЮзЧЕжѓТ(CMV)жИЦEBзЧЕжѓТ(EBV)еЈ≤зЯ•зЙєеЉВжАІTCRзЪДйЙіеЃЪи°®жШОпЉМдЄ§дЄ™ж≤їзЦЧзїДдєЛйЧізЪДзЧЕжѓТзЙєеЉВжАІTзїЖиГЮжХ∞йЗПзЫЄељУпЉМеєґдЄФдїНзДґе≠ШеЬ®пЉМйЪПжЧґйЧіз®≥еЃЪ(CMV: CD4: F(3,24)=0.76 p=0.530;CD8: F(3,24)=0.27 p=0.849;EBV:CD4: F(3,24)=1.64 p= 0.206;CD8: F (1.13, 9.03) =1.32, p=0.287)гАВдЄОзІїж§НеЙНзЪДTзїЖиГЮеЇУзЫЄжѓФпЉМдЊЫдљУеПНеЇФжАІCD4TзїЖиГЮеЇУжШЊз§ЇCMVзЙєеЉВжАІTзїЖиГЮзЪДдЄ∞еЇ¶еҐЮеК†(t(9)=-2.9 p=0.017)гАВзЧЕжѓТзЙєеЉВжАІTзїЖиГЮзЪДзіѓзІѓйҐСзОЗиІБи°•еЕЕеЫЊ7гАВ
3
дЊЫдљУеПНеЇФжАІTзїЖиГЮеЕНзЦЂеЇУ
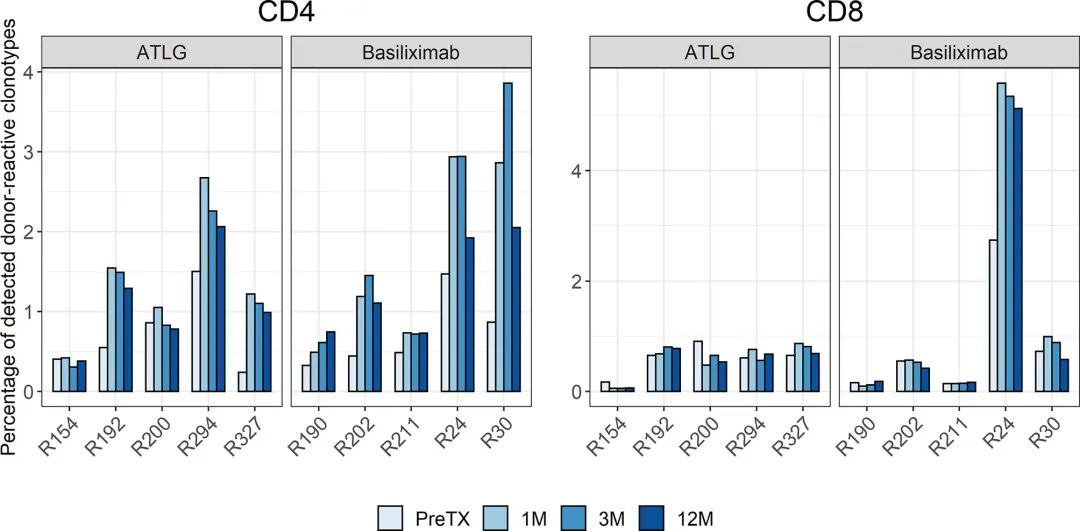
еЫЊ6
зІїж§НеЙНз°ЃеЃЪдЊЫдљУеПНеЇФжАІTCRеЕНзЦЂеЇУгАВеѓєзІїж§НеЙНеТМзІїж§НеРОе§ІйЗПTзїЖиГЮеЇУдЄ≠жЙАжЬЙеЕЛйЪЖеЮЛдЄ≠еПѓж£АжµЛеИ∞зЪДйҐД嚥жИРдЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЪДеИЖжЮРжШЊз§ЇпЉМзІїж§НеРОеПѓж£АжµЛеИ∞зЪДCD4дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЪДзЩЊеИЖжѓФжШЊиСЧеҐЮеК†пЉМиАМдЄОиѓ±еѓЉж≤їзЦЧжЧ†еЕ≥(t(9)=-3.89 p=0.004)гАВзІїж§НеРОATLGзїДCD4дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЩЊеИЖжѓФеє≥еЭЗеҐЮеК†0.67%пЉМиЊЊеИ∞1.38%¬±0.83гАВеРМж†ЈпЉМеЬ®еЈіеИ©жШФеНХжКЧж≤їзЦЧзїДдЄ≠пЉМзІїж§НеРОCD4дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛеє≥еЭЗеҐЮеК†0.92%пЉМиЊЊеИ∞1.64%¬±1.17гАВ
еЫЊ6жШЊз§ЇдЇЖжЙАжЬЙжВ£иАЕеЬ®жЙАжЬЙжЧґйЧізВєзЪДдЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЪДзЩЊеИЖжѓФпЉМеєґеЬ®и°•еЕЕи°®7дЄ≠жШЊз§ЇгАВж≠£е¶ВйҐДжЬЯзЪДйВ£ж†ЈпЉМеЬ®зІїж§НеРОиІВеѓЯжЧґйЧіеЖЕпЉМеЈіеИ©жШФеНХжКЧж≤їзЦЧзїДжЙАжЬЙеПЧиѓХиАЕзЪДCD4TзїЖиГЮдЄ≠дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЪДжХ∞еАЉеҐЮеК†гАВзДґиАМпЉМеЬ®ATLGзїДдЄ≠пЉМдЄ§дЄ™дЇЇдЊЫдљУеПНеЇФжАІзїЖиГЮзЪДеҐЮеК†дЄН姙жШОжШЊпЉМињЩеПѓиГљжШѓзФ±ињЩдЇЫеПЧиѓХиАЕйХњжЬЯжЈЛеЈізїЖиГЮеЗПе∞СеЉХиµЈзЪДгАВ
дЄОCD4дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЫЄеПНпЉМзІїж§НеРОCD8дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЩЊеИЖжѓФжЧ†зїЯиЃ°е≠¶жДПдєЙеПШеМЦ(t(9)=-1.01 p=0.341)гАВ
жАїдљУиАМи®АпЉМеЬ®зІїж§НеРОзЪДжХідЄ™иІВеѓЯжЬЯеЖЕпЉМдЄ§дЄ™ж≤їзЦЧзїДзЪДдЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЩЊеИЖжѓФзЫЄдЉЉ(CD4: F(1.26, 10.08)=1.38 p=0.279;CD8: F(1.06, 8.48)=1.15, p=0.319)гАВ
ињЩзІНдЊЫдљУеПНеЇФжАІеЇУзЪДеҐЮеК†дЄНдїЕеЬ®еЕЛйЪЖеЮЛж∞іеє≥дЄКиІВеѓЯеИ∞пЉМиАМдЄФеЬ®зІїж§НеРОеЊ™зОѓдЊЫдљУеПНеЇФжАІTзїЖиГЮзЪДйҐСзОЗж∞іеє≥дЄКдєЯиІВеѓЯеИ∞гАВеѓєдЇОCD4дЊЫдљУеПНеЇФжАІTзїЖиГЮпЉМзІїж§НеРОиІВеѓЯеИ∞жШЊиСЧеҐЮеК†(t(9) =-3.59 p=0.006)пЉМиАМCD8дЊЫдљУеПНеЇФжАІTзїЖиГЮзЪДзЩЊеИЖжѓФеЬ®зІїж§НеРОдњЭжМБзЫЄдЉЉ(t(9)=1.57 p=0.150)гАВATLGзїДеТМеЈіеИ©жШФеНХжКЧж≤їзЦЧзїДзІїж§НеРОCD4дЊЫдљУеПНеЇФжАІTзїЖиГЮеє≥еЭЗеНЗйЂШеИЖеИЂдЄЇ0.90%еТМ0.89%гАВ
05
иЃ®иЃЇ
иѓ•жЦЗзЂ†зЪДдЉШзВєеЬ®дЇОеѓєжЈЛеЈіеОїйЩ§иѓ±еѓЉж≤їзЦЧеРОжЈЛеЈізїЖиГЮеЖНзФЯињЫи°МдЇЖиѓ¶зїЖзЪДжППињ∞пЉМеМЕжЛђеѓєжѓПдљНжВ£иАЕзЪДжХідЄ™еЊ™зОѓTCRеЕНзЦЂеЇУеТМдЊЫдљУзЙєеЉВжАІTзїЖиГЮињЫи°МдЇЖTCRжµЛеЇПгАВињЩзІНжЈ±еЕ•зЪДжµЛеЇПеИЖжЮРдљњдљЬиАЕиГље§ЯиОЈеЊЧжЫіеЕ®йЭҐзЪДжХ∞жНЃпЉМдї•иѓДдЉ∞ATLGж≤їзЦЧеТМеЈіеИ©жШФеНХжКЧж≤їзЦЧеѓєеПЧдљУTCRеЕНзЦЂеЇУзЪДељ±еУНгАВињЩй°єз†Фз©ґдЄЇжЈ±еЕ•дЇЖиІ£ATLGж≤їзЦЧзЪДжХИжЮЬеТМеЃЙеЕ®жАІжПРдЊЫдЇЖжЬЙеКЫзЪДжФѓжМБгАВ
ж†єжНЃзЫЃеЙНзЪДжХ∞жНЃпЉМеЊЧеЗЇзїУиЃЇпЉМиВЊзІїж§НеПЧиАЕеЬ®еЗПе∞СеЙВйЗПATLGеРОйЗНжЦ∞е°ЂеЕЕзЪДTCRеЕНзЦЂеЇУдЄНдЉЪзЉ©е∞ПжИЦеАЊжЦЬпЉМеѓЉиЗіжХідљУе§Ъж†ЈжАІеТМTзїЖиГЮеС®иљђзОЗдЄОжО•еПЧеЈіеИ©жШФеНХжКЧж≤їзЦЧзЪДжВ£иАЕзЫЄељУгАВеРМж†ЈеЬ∞пЉМжО•еПЧдљОеЙВйЗПATLGж≤їзЦЧзЪДжВ£иАЕдЄОжО•еПЧеЈіеИ©жШФеНХжКЧж≤їзЦЧзЪДжВ£иАЕдЄАж†ЈпЉМеѓєдЊЫдљУеПНеЇФжАІTзїЖиГЮжХ∞йЗПеҐЮеК†гАВ
дљОеЙВйЗПATLGдњЭзХЩдЇЖTCRеЕНзЦЂеЇУзЪД嚥зКґпЉМжљЬеЬ®еЬ∞йЩНдљОдЇЖжДЯжЯУжИЦзЩМзЧЗзЪДжШУжДЯжАІпЉМиАМдЄНдЉЪеҐЮеК†жОТжЦ•еПНеЇФгАВ
#3

ж†ЗйҐШпЉЪProspective Tracking of Donor-Reactive T-Cell Clones in the¬†Circulation and Rejecting Human¬†Kidney Allografts
еЙНзЮїжАІињљиЄ™дЊЫдљУеПНеЇФжАІTзїЖиГЮеЬ®и°АеЊ™зОѓеТМеПСзФЯжОТжЦ•еПНеЇФзЪДдЇЇз±їиВЊзІїж§НдЄ≠зЪДеЕЛйЪЖгАВ
еПСи°®жЬЯеИКпЉЪFrontiers in Immunology
еПСи°®жЧ•жЬЯпЉЪ2021еєі10жЬИ
ељ±еУНеЫ†е≠РпЉЪ8.79
01
ж†ЈжЬђ
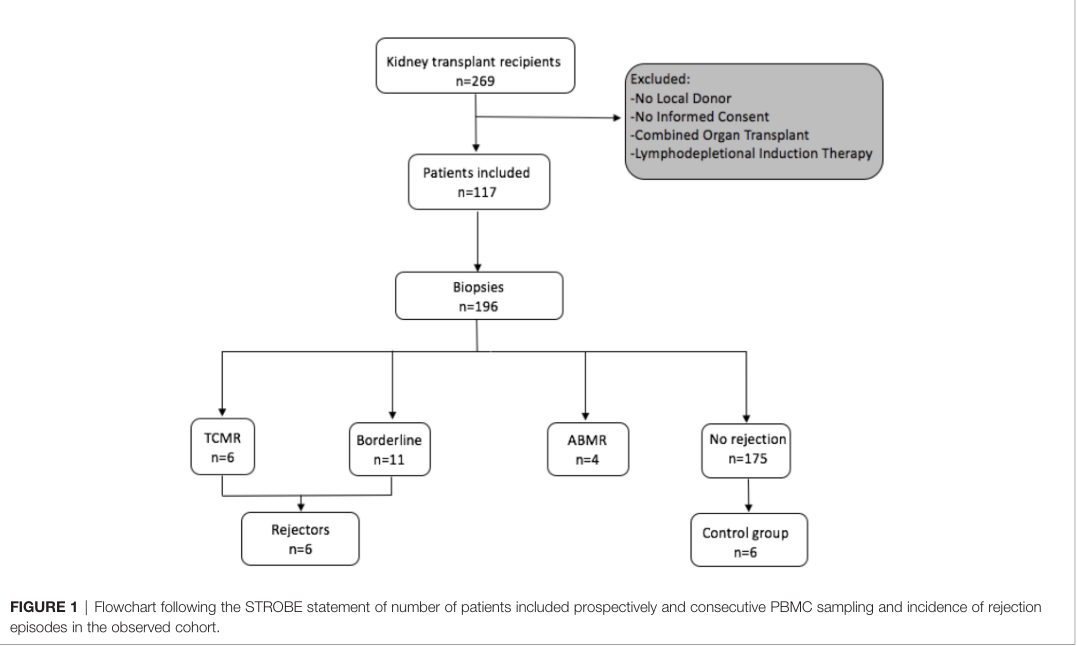
зІїж§НеЙНеЕ±зЇ≥еЕ•117дЊЛзђ¶еРИжЭ°дїґзЪДеПЧдљУпЉМеЬ®зІїж§НжЧґеИЖз¶їеПЧдљУеТМдЊЫдљУе§ЦеС®еНХдЄ™ж†ЄзїЖиГЮ(PBMCs)еєґеЖЈеЖїдњЭе≠ШиЗ≥еИЖжЮРгАВ
02
иГМжЩѓ
еРМзІНеЉВдљУиВљеТМHLAеИЖе≠РзЪДжКЧеОЯиѓЖеИЂеѓЉиЗізІїж§НеРОдЊЫдљУеПНеЇФжАІTзїЖиГЮзЪДжњАжіїпЉМеПѓиГљеѓЉиЗіTзїЖиГЮдїЛеѓЉзЪДжОТжЦ•еПНеЇФ(TCMR)гАВTзїЖиГЮеПЧдљУ(TCR)еЇУзЪДжµЛеЇПеПѓзФ®дЇОињљиЄ™иВЊзІїж§НеРОжВ£иАЕи°Ажґ≤еТМзїДзїЗдЄ≠зЪДдЊЫдљУеПНеЇФеЇУгАВ
03
еЃЮй™МжЦєж≥Хе≠¶
aпЉЙз†Фз©ґиЃЊиЃ°
bпЉЙTCRжµЛеЇП
cпЉЙзїЯиЃ°жЦєж≥Х
04
зїУжЮЬ
1
еЃЪдєЙжХідљУеТМдЊЫдљУеПНеЇФжАІTCRеЕНзЦЂеЇУ
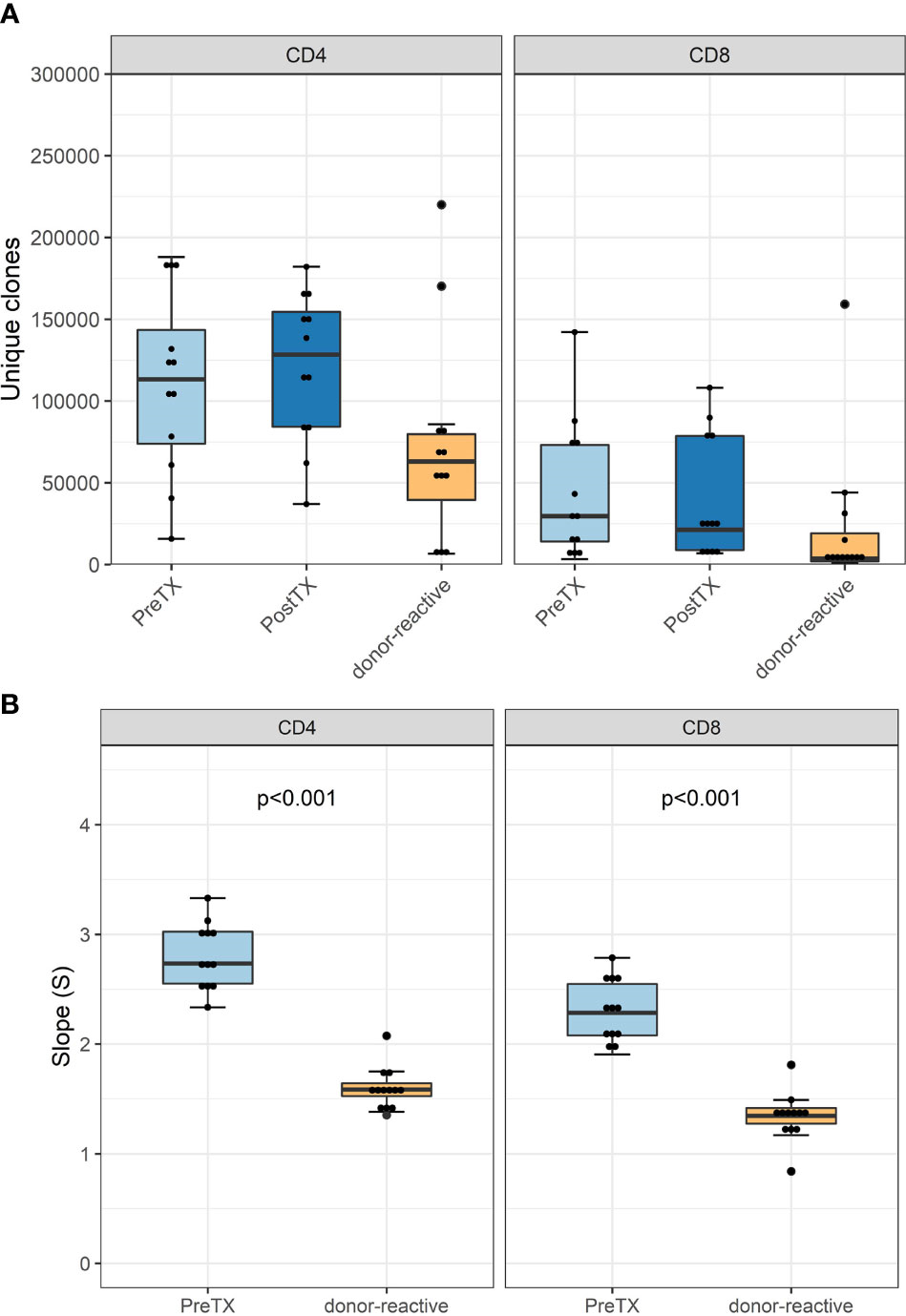
еЫЊ2
зІїж§НеЙНж£АжµЛеИ∞зЪДTCRеЕЛйЪЖеЮЛжХ∞йЗПдЄОзІїж§НеРОзЫЄељУ(еЫЊ2A)гАВж≠£е¶ВйҐДжЬЯзЪДйВ£ж†ЈпЉМдЄОеЊ™зОѓдЄ≠жЬ™еПЧеИЇжњАзЪДжХідљУTзїЖиГЮзЫЄжѓФпЉМжЭ•иЗ™MLRзЪДеЇФз≠ФзїЖиГЮжШЊз§ЇеЗЇзЪДеЕЛйЪЖеЮЛжХ∞йЗПжШЊзЭАеЗПе∞СгАВжѓПдЄ™жВ£иАЕзЪДеЕЛйЪЖеЮЛжХ∞йЗПеТМеЕЛйЪЖжХ∞зЪДиѓ¶зїЖдњ°жБѓиІБи°•еЕЕи°®2-4гАВ
е§Ъж†ЈжАІеИЖжЮРеИ©зФ®еєВеЊЛжЦЬзОЗзЪДиѓБеЃЮдЇЖдЊЫдљУ-еПНеЇФжАІTзїЖиГЮеЇУзЪДеЈ≤зЯ•зЙєеЊБ;дєЯе∞±жШѓиѓіпЉМеЃГдї£и°®дЇЖдЄАдЄ™зЛђзЙєзЪДTзїЖиГЮеЕЛйЪЖзЊ§дљУпЉМдЄОжЬ™еИЇжњАзЪДжХідљУTCRеЇУзЫЄжѓФпЉМеЃГзЪДе§Ъж†ЈжАІиЊГдљОпЉМеєґдЄФеЕЈжЬЙиЊГе∞СзЪДзЛђзЙєеЕЛйЪЖ(еЫЊ2B)гАВ
жѓПдЄ™еПЧиѓХиАЕзЪДVJдљњзФ®жГЕеЖµеЬ®зІїж§НеЙНеРОзЪДж†ЈжЬђдЄ≠еЭЗжЬЙжЙАдЄНеРМпЉМеєґдЄФжѓПдЄ™еПЧиѓХиАЕзЪДдЊЫдљУеПНеЇФжАІTCRеЕНзЦЂеЇУдЄ≠дєЯж≤°жЬЙзЙєеЃЪзЪДVжИЦJеЯЇеЫ†еН†зїЭеѓєдЉШеКњпЉИж≤°жЬЙе±Хз§ЇжХ∞жНЃпЉЙгАВ
2
зІїж§НеРОеЊ™зОѓдЄ≠дЊЫдљУеПНеЇФжАІеЕЛйЪЖзЪДжЙ©еҐЮ
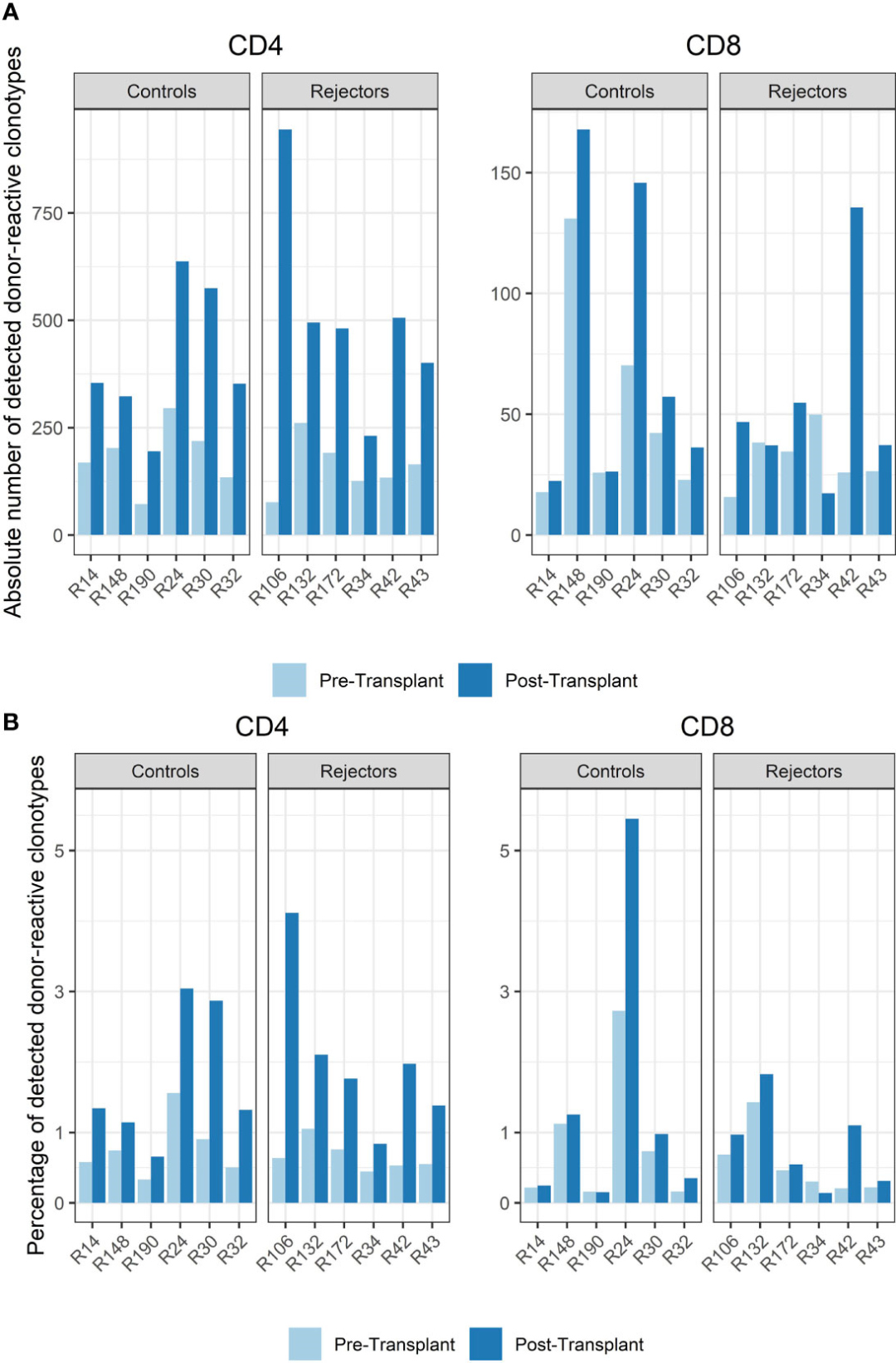
еЫЊ3
еЬ®зІїж§НеЙНжВ£иАЕи°Ажґ≤дЄ≠еПСзО∞зЪДжЙАжЬЙзЛђзЙєзЪДдЇТи°•еЖ≥еЃЪеМЇ3 (CDR3)еЇПеИЧдЄ≠пЉМCD4еТМCD8еЕЛйЪЖеЮЛзЪДдЊЫдљУеПНеЇФжАІTзїЖиГЮзЩЊеИЖжѓФеИЖеИЂдЄЇ0.34-1.56%еТМ0.16%-2.73%гАВиІВеѓЯдЊЫдљУеПНеЇФжАІTзїЖиГЮеЬ®еЊ™зОѓдЄ≠зЪДдЄ∞еЇ¶еТМйҐСзОЗпЉМеПСзО∞жЙАжЬЙCD4зїЖиГЮзЪД0.43%иЗ≥1.92%еТМжЙАжЬЙCD8зїЖиГЮзЪД0.15иЗ≥1.49%жШѓдЊЫдљУеѓЉеРСзЪД(еЫЊ3)гАВ
еѓєзЕІзїДеТМжОТжЦ•зїДзЪДжіїж£АжЧґйЧізВєеИЖеИЂдЄЇзІїж§НеРО6-141姩(дЄ≠дљН61姩)еТМ7-251姩(дЄ≠дљН94姩)пЉМдЄОзІїж§НеЙНзЫЄжѓФпЉМеЗ†дєОжЙАжЬЙеПЧиѓХиАЕе§ЦеС®и°АдЄ≠CD4еТМCD8 TзїЖиГЮзЪДдЊЫдљУеПНеЇФжАІеЕЛйЪЖзЪДзїЭеѓєжХ∞йЗПеТМзЩЊеИЖжѓФйГљеЭЗеҐЮеК†(p<0.001пЉМеЭЗеАЉеЈЃ: -1.197, CI:-1.802пЉМ -0.593пЉМеЫЊ3)гАВеЬ®жіїж£АжЧґйЧізВєдЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЪДзЩЊеИЖжѓФдЄ≠дєЯеПѓдї•зЬЛеИ∞ињЩзІНеЈЃеЉВпЉМеєґдЄФеЬ®жОТжЦ•жВ£иАЕеТМеѓєзЕІзїДдЄ≠CD4иЊЊеИ∞зїЯиЃ°е≠¶жДПдєЙ,дљЖCD8йШ≥жАІTзїЖиГЮж≤°жЬЙ(p< 0.001пЉМеЭЗеАЉеЈЃ:-1.168, CI:-1.723пЉМ-0.612)гАВињЩдЇЫеПШеМЦжШѓзФ±дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЉХиµЈзЪДпЉМйҐСзОЗиЊГдљОпЉМеЬ®зІїж§НеЙНжЬ™ж£АжµЛеИ∞пЉМж≤°жЬЙжЯРдЇЫеЕЛйЪЖеЮЛзЪДдЉШеКњжИЦеНХдЄАдЊЫдљУеПНеЇФжАІеЕЛйЪЖзЪДдЉШеКњеҐЮеК†гАВеЬ®жЙАжЬЙеПЧиѓХиАЕдЄ≠йГљеПѓдї•ж£АжµЛеИ∞ињЩзІНеҐЮеК†пЉМеМЕжЛђ4еРНжВ£иАЕеЬ®зІїж§НеРО6姩пЉМеП¶е§Ц2еРНжВ£иАЕеЬ®зІїж§НеРО251姩дєЯеПСзО∞дЇЖињЩзІНеҐЮеК†гАВжОТжЦ•иАЕеТМеѓєзЕІзїДдєЛйЧідЊЫдљУеПНеЇФжАІTзїЖиГЮзЪДеҐЮеК†ж≤°жЬЙеЈЃеЉВ[жЬ™йЕНеѓєе≠¶зФЯTж£Ай™М;p=0.64(CD4+)еТМp=0.52(CD8+)]пЉМжАїдљУиАМи®АпЉМдЊЫдљУеПНеЇФжАІеЕЛйЪЖеЬ®CD4йГ®еИЖзЪДеҐЮеК†жѓФCD8еЉВдљУеЕЛйЪЖжЫіжШОжШЊгАВ
3
еЊ™зОѓдЄ≠зЪДTCRеЕЛйЪЖе§Ъж†ЈжАІ
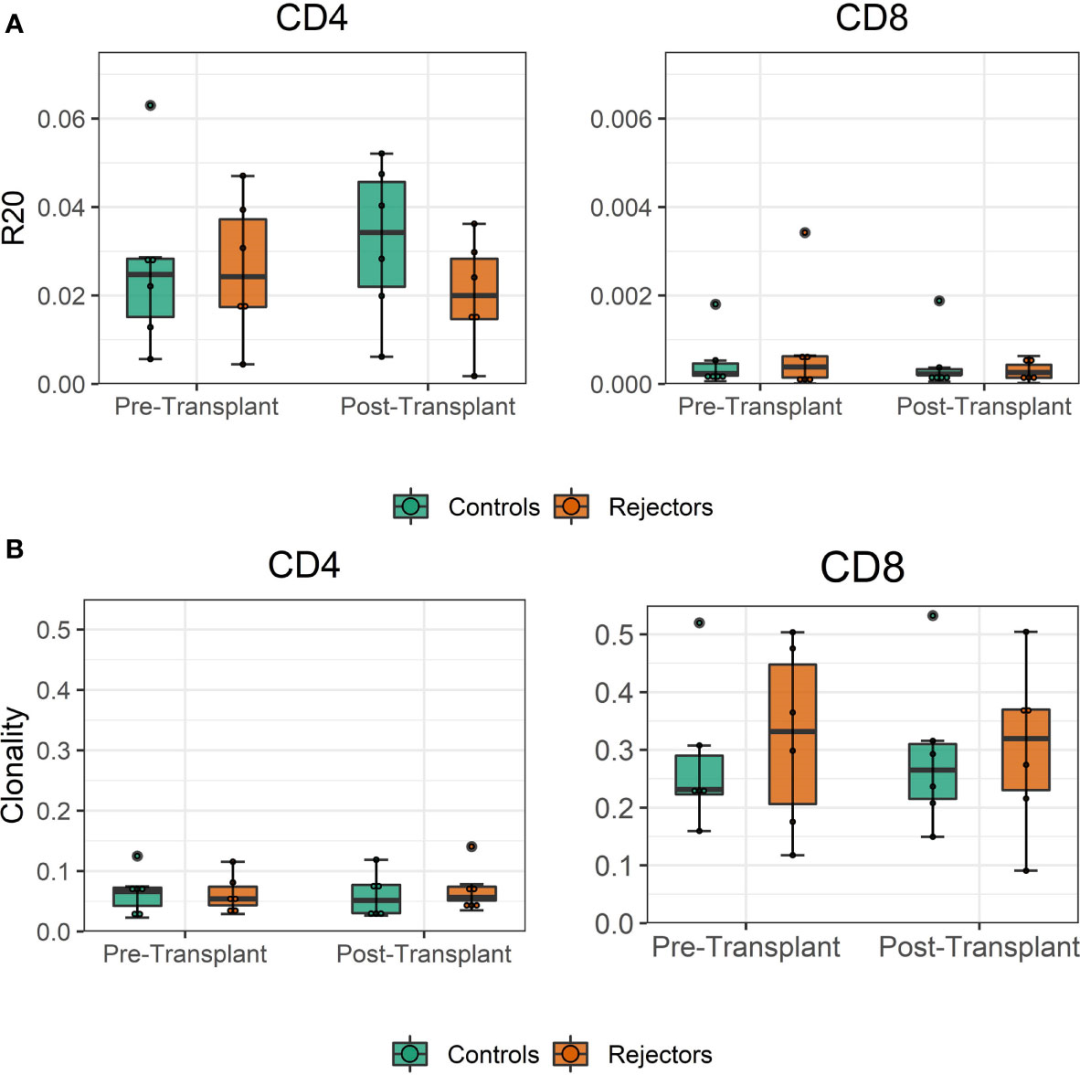
еЫЊ4
йАЪињЗеЕЛйЪЖжАІжµЛйЗПзЪДзІїж§НеЙНеЯЇеЫ†е§Ъж†ЈжАІпЉМCD4зїЖиГЮдЄЇ0.018-0.13,CD8TзїЖиГЮдЄЇ0.13 – 0.5гАВ
зІїж§НеРОж†ЈжЬђзЪДеЕЛйЪЖжАІдЄОзІїж§НеЙНзЪДеЕЛйЪЖжАІзЫЄељУпЉМе¶ВеЫЊ4жЙАз§ЇгАВж≤°жЬЙеПСзО∞R20дљЬдЄЇеЕНзЦЂдЉШеКњеЇ¶жМЗж†ЗеЬ®жОТжЦ•зїДеТМеѓєзЕІзїДдєЛйЧізЪДеЈЃеЉВ(еЫЊ4B)гАВ
йЗПеМЦдЇЖзІїж§НеЙНеРОTCRеЕНзЦЂеЇУзЪДжАїдљУеПШеМЦпЉМдї•з°ЃеЃЪзЙєеЉВжАІеЕЛйЪЖзЪДжШЊиСЧеҐЮеК†жШѓеР¶иІБдЇОTCRеЕНзЦЂеЇУжАїдљУеПШеМЦпЉМе¶ВжЮЬжЬЙзЪДиѓЭпЉМеЇФиѓ•и°®зО∞дЄЇиЊГйЂШзЪДJensen-ShannonжХ£еЇ¶пЉИJSDпЉЙгАВзДґиАМпЉМJSDеАЉиЊГдљОпЉМи°®жШОеЬ®йЗЗж†ЈжЬЯйЧіпЉМжХідљУеЕНзЦЂеЇУеПШеМЦдЄНе§ІпЉМжОТжЦ•жВ£иАЕдЄОеѓєзЕІзїДжЧ†зїЯиЃ°е≠¶еЈЃеЉВ(и°•еЕЕеЫЊ3)гАВ
дљЬиАЕж≤°жЬЙеПСзО∞жОТжЦ•еПНеЇФжВ£иАЕзЪДе§ЦеС®и°АдЊЫдљУзЙєеЉВжАІеЇУдЄОеѓєзЕІзїДжЬЙеЈЃеЉВпЉМдљЖеЬ®жЙАжЬЙзІїж§НеПЧиАЕдЄ≠пЉМињЩдЇЫдЊЫдљУеПНеЇФжАІзїЖиГЮзЪДеҐЮеК†еєґж≤°жЬЙдЉійЪПзЭАжАїдљУеЇУзЪДжШЊиСЧеПШеМЦгАВ
3
иВЊзІїж§НжОТжЦ•еПНеЇФжЧґдЊЫдљУеПНеЇФжАІTзїЖиГЮеЗЇзО∞жШОж،浪洶
еЬ®дЄ§зІНжОТжЦ•зІїж§НзЪДжіїж£АдЄ≠пЉМйАЪињЗеЬ®еЕЈжЬЙзїДзїЗе≠¶TCMRзЪДж†ЈжЬђдЄ≠еПСзО∞дЇЖ6,186еТМ23,108дЄ™TзїЖиГЮпЉМеЕґдЄ≠еМЕжЛђ3,248еТМ10,266зІНдЄНеРМзЪДTзїЖиГЮеЕЛйЪЖеЮЛпЉМиАМеЬ®еѓєзЕІжіїж£АдЄ≠жЬ™ж£АжµЛеИ∞TCRзЙєеЉВжАІRNAгАВж†єжНЃзІїж§НеЙНMLRзЪДеЃЪдєЙпЉМеЬ®ињЩдЇЫTзїЖиГЮдЄ≠пЉМдЊЫдљУеПНеЇФзїЖиГЮзЪДйҐСзОЗеИЖеИЂдЄЇ4.8%еТМ2.5%пЉМеИЖеИЂдї£и°®3.7%еТМ2.4%зЪДзЛђзЙєеЕЛйЪЖеЮЛгАВзФ±дЇОFACSеИЖйАЙеѓєињЩдЇЫж†ЗжЬђдЄНеПѓи°МпЉМеЫ†ж≠§дЄНеПѓиГљеНХзЛђеИЖжЮРCD4еТМCD8TзїЖиГЮпЉМеЫ†ж≠§еѓєе§ІйЗПж†ЈжЬђињЫи°МињЫдЄАж≠•еИЖжЮРгАВ
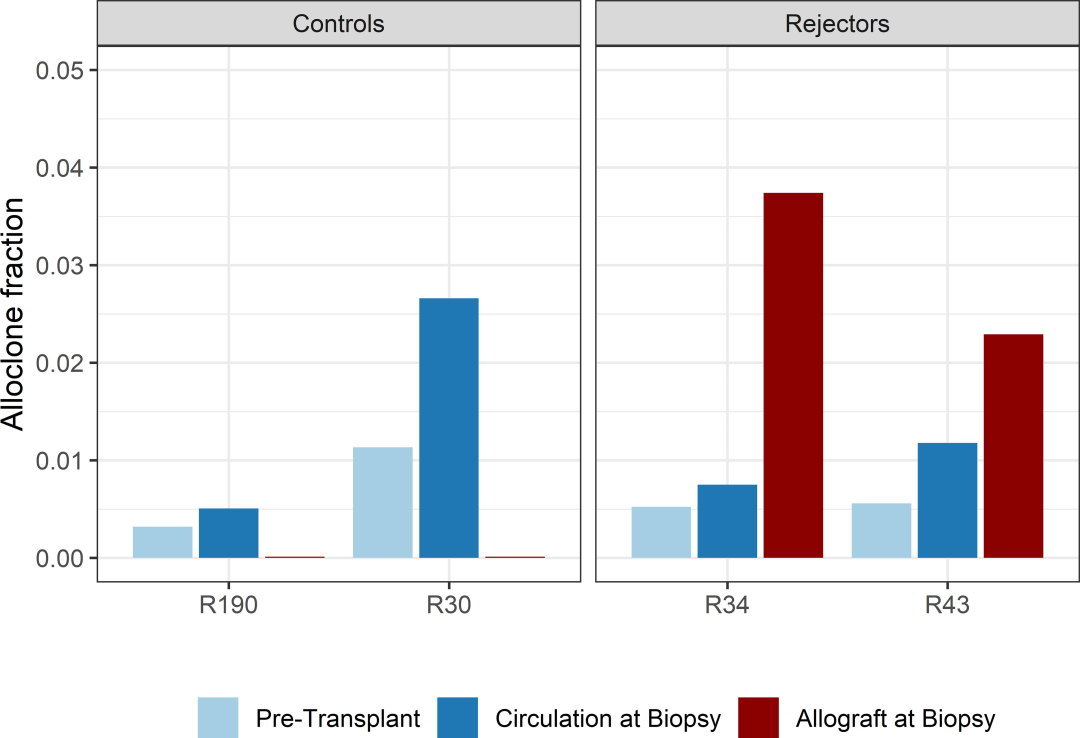
еЫЊ5
йАЪињЗдЄОеРМжЬЯеЊ™зОѓдЄ≠дЊЫдљУеПНеЇФжАІTзїЖиГЮзЪДжѓФдЊЛзЫЄжѓФпЉМеЉВдљУзІїж§НзЙ©дЄ≠дЊЫдљУеПНеЇФжАІеЕЛйЪЖзЪДжѓФдЊЛжЬЙжЙАеҐЮеК†(еЫЊ5)гАВе¶ВеЙНжЙАињ∞пЉМжВ£иАЕR34еТМR43зЪДжіїж£АдЄ≠дЊЫдљУеПНеЇФжАІеЕЛйЪЖзЪДжѓФдЊЛеИЖеИЂдЄЇ3.7%еТМ2.4%пЉМиАМеРМжЬЯе§ЦеС®и°АдЄ≠дЊЫдљУеПНеЇФжАІеЕЛйЪЖзЪДжѓФдЊЛеИЖеИЂдЄЇ0.6%еТМ1.5%гАВжЬЙиґ£зЪДжШѓпЉМеܮ浪洶зЪДTзїЖиГЮдЄ≠ж≤°жЬЙиІВеѓЯеИ∞еЕЛйЪЖдЉШеКњпЉМињЩи°®жШОеЬ®TCMRжЬЯйЧіпЉМеЗ†зІНжКЧеОЯзЙєеЉВжАІTзїЖиГЮжЬЙеєњж≥ЫзЪДеПНеЇФгАВ
R34еТМR43浪洶TCRеЕНзЦЂеЇУзЪДR20еИЖеИЂдЄЇ0.038еТМ0.023пЉМеЕЛйЪЖжАІеИЖеИЂдЄЇ0.042еТМ0.055гАВињЩдЇЫеАЉдЄОиІВеѓЯеИ∞зЪДе§ЦеС®TCRеЕНзЦЂеЇУеАЉзЫЄељУ(еЫЊ4)гАВ
дЄОжЬѓеЙНе§ЦеС®и°АTCRеЇУеТМжіїж£АжЧґе§ЦеС®и°АTCRеЇУзЪДJSDеАЉзЫЄжѓФпЉМжіїж£АжЧґзЪДдЊЫдљУеМЇеЯЯ浪洶TCRеЕНзЦЂеЇУдЄОжіїж£АжЧґе§ЦеС®и°АTCRеЇУдєЛйЧізЪДJSDеАЉжЫійЂШпЉМињЩжДПеС≥зЭАзІїж§НеРОдЇЇдљУTCRеЕНзЦЂеЇУеПСзФЯдЇЖжШЊиСЧеПШеМЦ(и°®2)гАВеЉВдљУзІїж§НзЙ©дЄ≠е≠ШеЬ®зЪДеЙН20зІНеЕЛйЪЖеЮЛеИЧи°®еПКеЕґеЬ®е§ЦеС®и°Аж†ЈжЬђдЄ≠зЪДйҐСзОЗиІБи°•еЕЕи°®5гАВ
ињШйАЪињЗжѓФиЊГдЇЖеРМзІНеЉВдљУзІїж§Нзɩ浪洶TзїЖиГЮеТМеЊ™зОѓTзїЖиГЮзЪДVJдљњзФ®жГЕеЖµгАВиЩљзДґиІВеѓЯеИ∞жВ£иАЕR34дЄ≠TRBV7-9xTRBJ2-7еТМTRBV7-2xTRBJ2-7еЬ®зїДзїЗдЄ≠зЪДдљњзФ®жЫіеЉЇпЉМиАМжВ£иАЕR43дЄ≠TRBV7-2xTRBJ2-1еТМTRBV7-9xTRBJ2-5еЬ®зїДзїЗдЄ≠зЪДдљњзФ®жґИ姱пЉМдљЖеЬ®зїДзїЗдЄ≠зЪДжАїдљУVJдљњзФ®жГЕеЖµеТМе§ЦеС®и°АдЄ≠зЪДVJдљњзФ®жГЕеЖµдњЭжМБдЄАиЗі(и°•еЕЕеЫЊ4)гАВжВ£иАЕR34еТМR43зЪДVJдљњзФ®дєЛйЧізЪДJSDеИЖеИЂдЄЇ0.065еТМ0.063пЉМеЫ†ж≠§йЭЮеЄЄзЫЄдЉЉгАВ
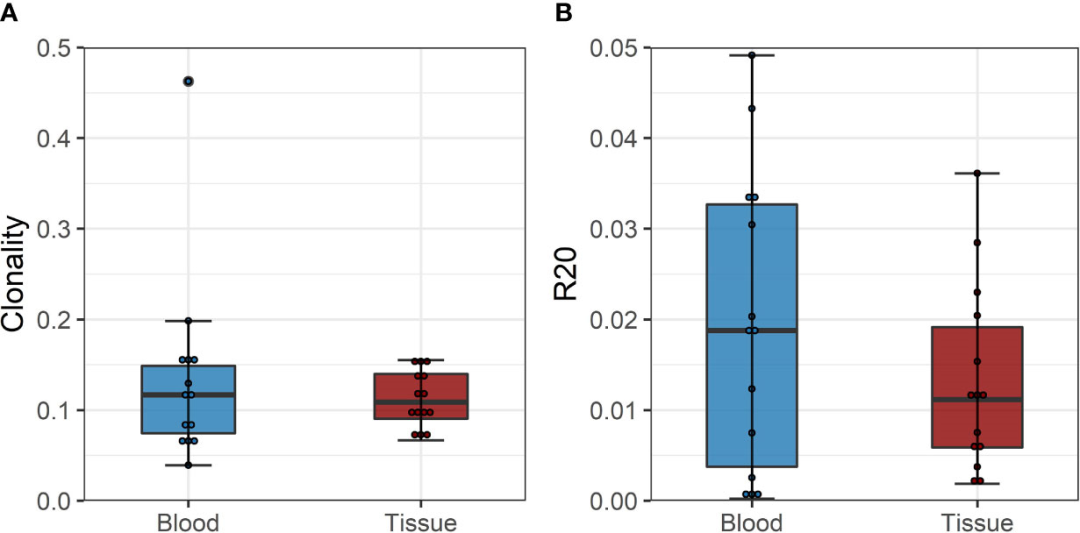
еЫЊ6
дЄЇдЇЖиѓБеЃЮињЩдЇЫеПСзО∞пЉМйАЪињЗеѓєдЄГдЄ™зїПињЗзїЖиГЮжОТжЦ•еПНеЇФзЪДиВЊзІїж§НеПЧиАЕзЪДжіїж£АеТМи°Ажґ≤ж†ЈжЬђињЫи°МдЇЖз±їдЉЉзЪДйШЯеИЧеИЖжЮРгАВ
е∞љзЃ°зЉЇдєПжШОз°ЃзЪДдЊЫдљУ-еПНеЇФеЇУеТМдЄНеРМзЪДжµЛеЇПжЦєж≥ХпЉМе§Ъж†ЈжАІеИЖжЮРжШЊз§ЇдЇЖзЫЄдЉЉзЪДзїУжЮЬгАВеЬ®зїДзїЗж†ЈжЬђеТМжіїж£АжЧґйЧізВєзЪДеЊ™зОѓдєЛйЧіпЉМйАЪињЗеЕЛйЪЖжАІеТМR20жµЛйЗПзЪДTCRеЇУзЪДе§Ъж†ЈжАІж≤°жЬЙеЈЃеЉВгАВдЄОе§ЦеС®и°АTCRеЇУзЫЄжѓФпЉМ浪洶зїЖиГЮзЪДеє≥еЭЗеЕЛйЪЖжАІдЄЇ0.112жѓФ0.135 (p=0.411пЉМеЭЗеАЉеЈЃ:-0.023, CI:-0.036пЉМ -0.082)пЉМ R20дЄЇ0.013vs.0.019 (p=0.117пЉМеЭЗеАЉеЈЃ:0.006, CI:-0.002пЉМ-0.014)(еЫЊ6)гАВе§ЦеС®и°АеТМзїДзїЗйЧіVJдљњзФ®зЪДJSDиМГеЫідЄЇ0.03 ~ 0.21(и°•еЕЕи°®6)гАВ
4
жАїдљУеТМдЊЫдљУеПНеЇФжАІTCRеЕНзЦЂеЇУзЪДзљСзїЬеИЖжЮР
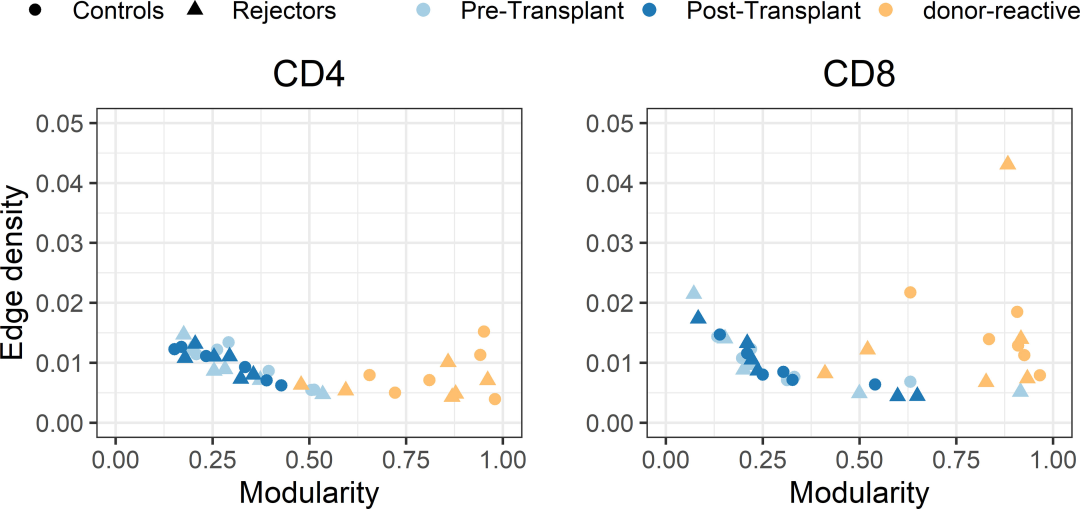
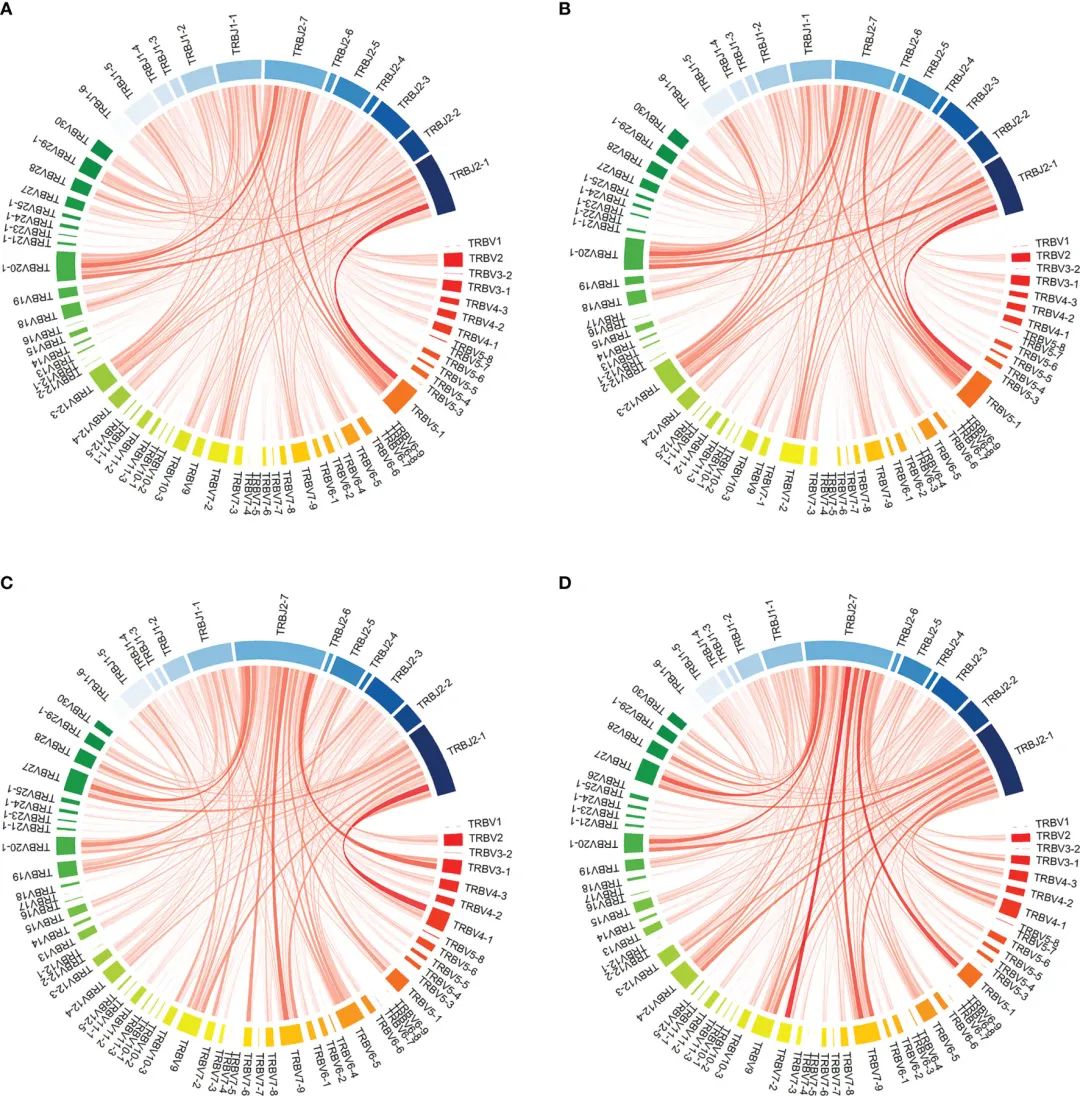
еЫЊ7
дЊЫдљУ-еПНеЇФжАІеЕНзЦЂеЇУзЪДдЄ™дљУзЙєеЉВжАІзљСзїЬжШЊз§ЇеЗЇжѓФзІїж§НеЙНзљСзїЬжЫійЂШзЪДж®°еЭЧеМЦ(йЕНеѓєе≠¶зФЯTж£Ай™М;P<0.001;CD4еТМCD8)еТМзІїж§НеРОзЪДжМЗж†З(йЕНеѓєе≠¶зФЯTж£Ай™М;P<0.001;CD4еТМCD8)пЉМи°®жШО嚥жИРзЪДз∞ЗеЖЕеЕЈжЬЙжЫізіІеѓЖзЪДињЮйАЪжАІ(еЫЊ7)гАВж≠§е§ЦпЉМеЬ®иЊєзЉШеѓЖеЇ¶жЦєйЭҐпЉМдЄ§дЄ™жЧґйЧізВєжИЦдЊЫдљУеПНеЇФеЇУдєЛйЧіж≤°жЬЙжШОжШЊеЈЃеЉВ(жЦєеЈЃеИЖжЮР;CD4зїЖиГЮ p=0.149, CD8зїЖиГЮ p=0.095)гАВињЩжШѓзљСзїЬдЄ≠жХідљУињЮйАЪжАІзЪДеЇ¶йЗПпЉМињЩи°®жШОпЉМе∞љзЃ°ж†єжНЃдЄНеРМжЧґйЧізВєеТМдЊЫдљУ-еПНеЇФеЇУзЪДиЊєзЉШеѓЖеЇ¶жЧ†ж≥ХжµЛйЗПеЃЮйЩЕињЮжО•зЪДеПѓиІВеѓЯеИ∞зЪДеҐЮеК†пЉМдљЖдЊЫдљУ-еПНеЇФжАІеЕНзЦЂзљСзїЬзЪДињЮжО•дЄїи¶БеИЖзїДеЬ®йЫЖзЊ§дЄ≠(еѓЖйЫЖињЮжО•зЪДиКВзВєзїД)пЉМйЫЖзЊ§е§ЦзЪДињЮжО•з®АзЦПгАВзЫЄжѓФдєЛдЄЛпЉМеЊ™зОѓжХідљУTCRеЇУзЪДдљОж®°еЭЧеМЦеАЉи°®жШОеЉВиі®жАІињЮжО•ж®°еЉПпЉМиАМж≤°жЬЙ嚥жИРйЂШеЇ¶ињЮжО•зЪДжЛУжЙСз∞ЗгАВзїЉдЄКжЙАињ∞пЉМињЩи°®жШОдЇЖдЊЫдљУзЙєеЉВжАІеЕНзЦЂзљСзїЬзЪДжЫіеЉЇзЪДзїЖеИЖпЉМе∞ЖеЕЛйЪЖеЮЛеИЖдЄЇеЕЈжЬЙзЫЄдЉЉCDR3еЇПеИЧзЪДзЊ§дљУгАВеЫЊ7еП≥йЭҐжЭњдЄ≠зЪДеЉВеЄЄеАЉжШѓељ±еУНеЫЊзРЖиЃЇзЙєеЊБзЪДдљОеЕЛйЪЖеЮЛиЃ°жХ∞зЪДCD8еЇУгАВ
05
иЃ®иЃЇ
ж†єжНЃжХ∞жНЃпЉМеЊЧеЗЇзЪДзїУиЃЇпЉМеЬ®зІїж§НеРОе§ЦеС®и°АдЄ≠иВЊзІїж§НеПЧиАЕзЪДдЊЫдљУеПНеЇФжАІTзїЖиГЮеЬ®зїПињЗйЭЮжЈЛеЈіжґИиАЧиѓ±еѓЉж≤їзЦЧеРОеҐЮеК†гАВдЊЫдљУеПНеЇФжАІTзїЖиГЮеЕЈжЬЙжШОжШЊе§Ъж†ЈжАІзЪДTCRпЉМжЪЧз§ЇзЭАе§ІйЗПйТИеѓєзІїж§НзЙ©дЄНеРМи°®дљНзЪДTзїЖиГЮ襀жњАжіїпЉМиАМињЩзІНзїДеРИеЬ®е§ЦеС®и°АдЄ≠еєґжЬ™еПНжШ†еЗЇжЭ•гАВињЩеЬ®зљСзїЬеИЖжЮРдЄ≠еЊЧеИ∞й™МиѓБпЉМдљЬиАЕж≤°жЬЙиІВеѓЯеИ∞жШЊиСЧзЪДзІїж§НзїДзїЗдЄ≠зЙєеЃЪжКЧеОЯеЉХеѓЉзЪДTзїЖиГЮз∞ЗпЉМжЧ†иЃЇжШѓеЬ®еЊ™зОѓињШжШѓзІїж§НзїДзїЗдЄ≠зЪДTзїЖиГЮдЄ≠гАВ
зДґиАМпЉМиІВеѓЯеИ∞CDR3еМЇеЯЯеЬ®дЊЫдљУеПНеЇФжАІеЕЛйЪЖеЮЛзЪДеРМзІНеЉВдљУиВЊзІїж§НдЄ≠еЕЈжЬЙйЗНи¶БжДПдєЙпЉМе∞љзЃ°еЃГдїђзЪДйҐСзОЗиЊГдљОпЉМдљЖеЃГдїђжШѓжЬАйЫЖдЄ≠ињЮжО•зЪДеЕЛйЪЖеЮЛдєЛдЄАгАВ
#4

ж†ЗйҐШпЉЪPerturbations of the T-cell immune repertoire in kidney transplant rejection
иВЊзІїж§НжОТжЦ•дЄ≠TзїЖиГЮеЕНзЦЂеЇУзЪДжФєеПШ
еПСи°®жЬЯеИКпЉЪFrontiers in Immunology
еПСи°®жЧ•жЬЯпЉЪ2022еєі11жЬИ
ељ±еУНеЫ†е≠РпЉЪ8.79
01
ж†ЈжЬђ
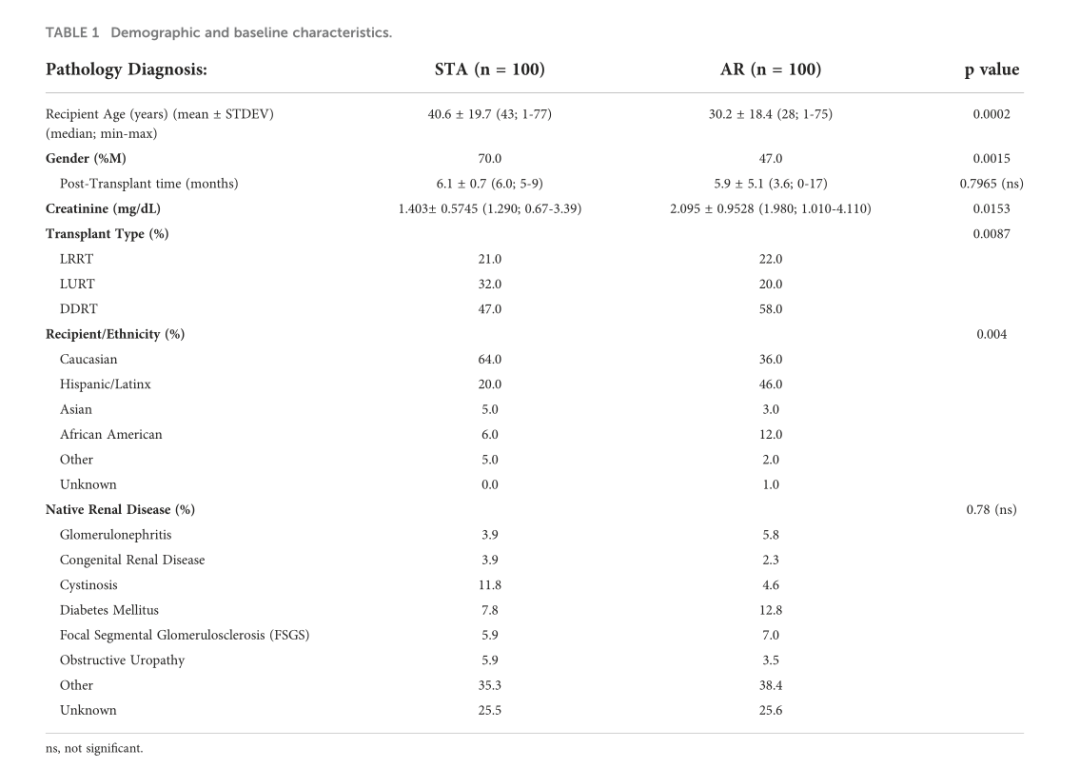
еѓєжЭ•иЗ™200еРНзЙєжЃКиВЊзІїж§НеПЧиАЕзЪД323дїље§ЦеС®и°Аж†ЈжЬђињЫи°МдЇЖжµЛеЇПпЉМеЕґдЄ≠жЬЙ(n=100)еТМж≤°жЬЙ(n=100)жіїж£АиѓБеЃЮзЪДжА•жАІжОТжЦ•еПНеЇФгАВ
02
иГМжЩѓ
еЬ®жЬђз†Фз©ґдЄ≠пЉМйАЪињЗиѓДдЉ∞дЇЖе§ІйЗПжИРдЇЇиВЊзІїж§НжВ£иАЕзЪДTCRеЕНзЦЂеЇУпЉМдї•дЊњиГље§ЯиЊ®еИЂTзїЖиГЮеЕЛйЪЖеТМзІїж§НжЧґйЧідєЛйЧізЪДдљОйҐСеПШеМЦпЉМзїДзїЗе≠¶иѓБеЃЮзЪДжА•жАІжОТжЦ•еПНеЇФпЉМдї•еПКTзїЖиГЮжИЦжКЧдљУдїЛеѓЉзЪДжОТжЦ•еПНеЇФзЪДдїїдљХзЙєеЉВжАІеПШеМЦгАВ
03
еЃЮй™МжЦєж≥Хе≠¶
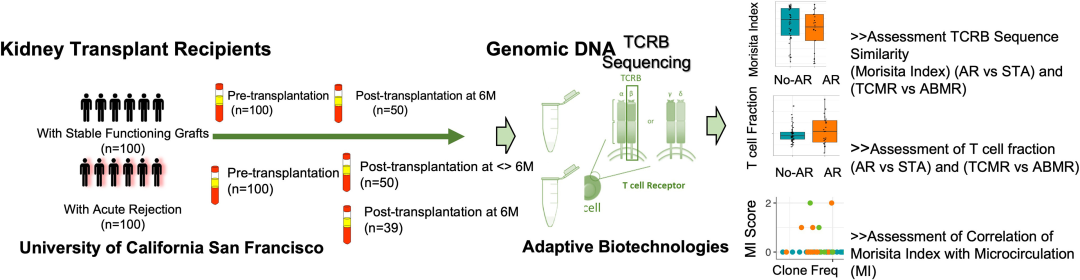
еЫЊ1
aпЉЙж†ЈеУБжФґйЫЖ
bпЉЙеЯЇеЫ†зїДDNAзЪДеИЖз¶їеТМTзїЖиГЮеПЧдљУеПѓеПШќ≤йУЊжµЛеЇП
cпЉЙTCRќ≤жµЛеЇПзїУжЮЬзЪДзїЯиЃ°еИЖжЮР
04
зїУжЮЬ
1
TзїЖиГЮеЕНзЦЂеЇУзЪДе§Ъж†ЈжАІеПКеЕґдЄОзІїж§НдЄіеЇКи°®еЮЛзЪДеЕ≥иБФ
еЫЊ2
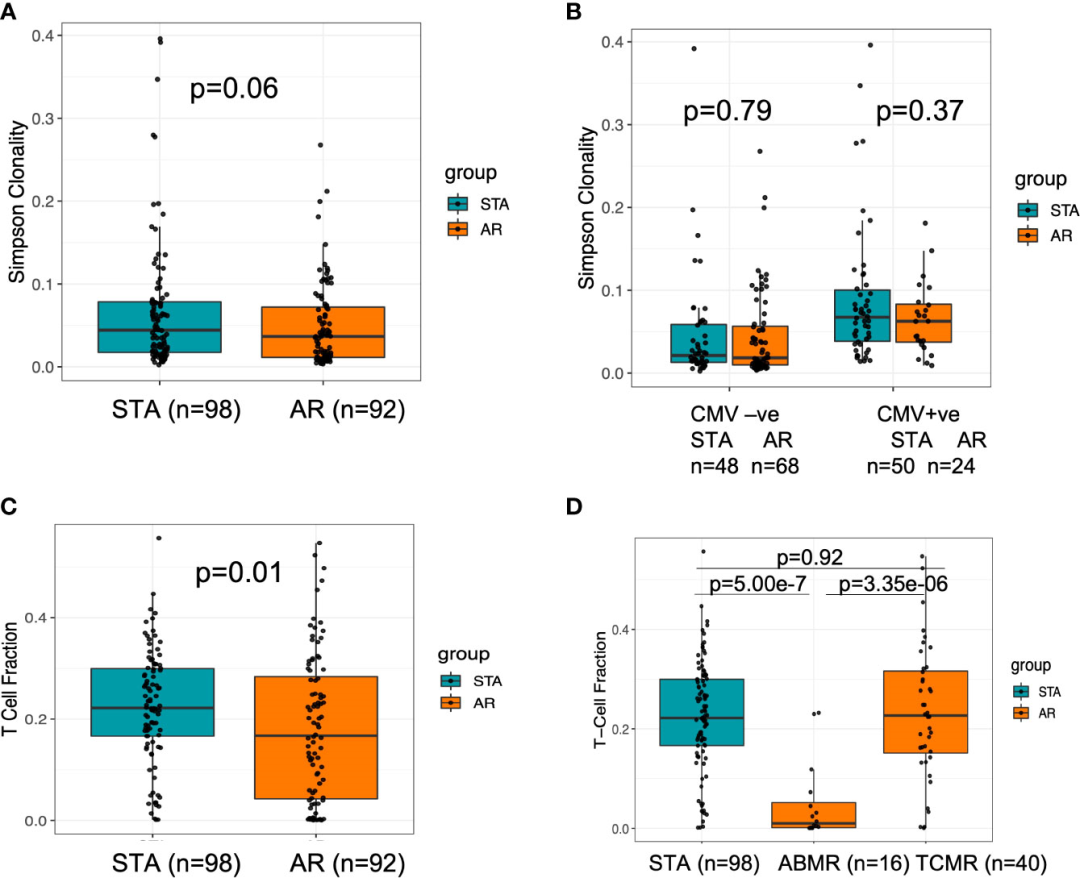
еЬ®зІїж§НеЙНйШґжЃµпЉМдїОзІїж§НеРОеЗЇзО∞жА•жАІжОТжЦ•еПНеЇФзЪДеПЧиѓХиАЕжФґйЫЖзЪДе§ЦеС®и°Аж†ЈжЬђдЄ≠иІВеѓЯеИ∞жЫіе§ІзЪДTзїЖиГЮеЇУе§Ъж†ЈжАІ(еЫЊ2A)гАВдљњзФ®еЕИеЙНеПСи°®зЪДжЦєж≥Х(21)пЉМжО®жЦ≠еПЧиѓХиАЕеЬ®еЯЇзЇњжЧґзЪДCMVзКґжАБ;зДґиАМпЉМеЃГдЄНиГљеМЇеИЖжљЬдЉПжАІжДЯжЯУеТМжіїеК®жАІжДЯжЯУгАВдЄОSTAзїДзЫЄжѓФпЉМARзїДдЄ≠CMV na√ѓveзЪДжВ£иАЕжХ∞йЗПжШОжШЊжЫіе§Ъ(51% vs.26%;з≤Њз°ЃP=0.0005)гАВ
еРМжЧґпЉМжЫійЂШзЪДTзїЖиГЮеЕЛйЪЖжАІеЬ®зІїж§НеРОжО®жЦ≠CMV PCRйШ≥жАІзЪДжВ£иАЕ(n=116)дЄ≠еПѓиІБгАВ(еЫЊ2b)гАВеПѓдї•иІВеѓЯеИ∞пЉМARзїДзЪДCMVйШ≥жАІзОЗжЬЙжЙАеҐЮеК†(жА•жАІжОТжЦ•еПНеЇФжЧґCMVйШ≥жАІзОЗдЄЇ57%пЉМиАМеРМдЄАжВ£иАЕзІїж§НеЙНзЪДCMVйШ≥жАІзОЗдЄЇ32% (p=0.03)гАВ
2
зІїж§НеЙНTCRBV01еТМTCRBJ01-02зЪДеПШеЉВеПКеЕґзІїж§НеРОзЪДдЄіеЇКзЫЄеЕ≥жАІ

и°•еЕЕеЫЊ1
йАЪињЗињЫдЄАж≠•иѓДдЉ∞дЇЖеЯЇзЇњж†ЈжЬђдЄ≠VеЮЛеТМJеЮЛTCRеЯЇеЫ†зЪДдљњзФ®ж®°еЉПпЉМдї•з°ЃеЃЪеПѓиГљдЄОARй£ОйЩ©еҐЮеК†зЫЄеЕ≥зЪДеЈЃеЉВеЯЇеЫ†дљњзФ®(и°•еЕЕеЫЊ1A, B)гАВеПѓдї•иІВеѓЯеИ∞ARеПЧиѓХиАЕдЄ≠TCRBV01еТМTCRBJ01-02зЪДдљњзФ®еҐЮеК†(p<0.05, WilcoxonзІ©еТМж£Ай™М)гАВ
3
зІїж§НеЙНзЪДеЯЇзЇњTCFrеТМзІїж§НжОТжЦ•й£ОйЩ©
еЫЊ3
йАЪињЗжіїж£АеИЖжЮРдЇЖиѓБеЃЮдЄЇBanff(14)еИЖз±їзЪДжА•жАІжОТжЦ•еПНеЇФжВ£иАЕзЪДзІїж§НеЙНTзїЖиГЮеИЖжХ∞пЉМдї•еПКTзїЖиГЮдїЛеѓЉзЪДжОТжЦ•еПНеЇФ(TCMR)жИЦжКЧдљУдїЛеѓЉзЪДжОТжЦ•еПНеЇФ(ABMR)зЧЕдЊЛпЉМеПѓдї•иІВеѓЯеИ∞дЄ§зІНз±їеЮЛзЪДжОТжЦ•еПНеЇФйШЯеИЧдєЛйЧіе≠ШеЬ®жШЊиСЧеЈЃеЉВ(Kruskal Wallis p=4.03e-06)пЉМдљњзФ®еРОDunnж£Ай™Мp=3.35e-6(еЫЊ2D)пЉМ ABMR TCFrеАЉиЊГдљОгАВ
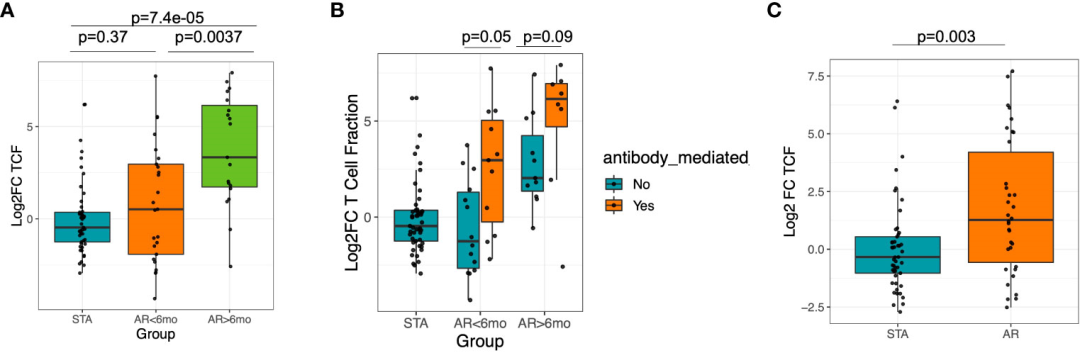
дЄЇдЇЖжѓФиЊГеПѓиГље≠ШеЬ®зЪДе§НжЭВеЫ†зі†пЉМжѓФиЊГдЇЖжАІеИЂгАБеєійЊДжИЦзІНжЧПдєЛйЧіеПШеМЦеЯЇзЇњTзїЖиГЮеИЖжХ∞гАВжАІеИЂ(M vs. F)гАБеєійЊД(<=37 vs. 38+)еЈЃеЉВжЧ†зїЯиЃ°е≠¶жДПдєЙпЉМWilcoxonзІ©еТМж£Ай™Мp>0.05гАВеПѓдї•иІВеѓЯеИ∞пЉМзІїж§НеРО6дЄ™жЬИеРОпЉМARйШЯеИЧдЄ≠TCFrжА•еЙІдЄКеНЗпЉМзЙєеИЂжШѓеѓєдЇОжЩЪжЬЯжА•жАІжОТжЦ•зЪДжВ£иАЕ(log2еАНеПШеМЦдЄ≠дљНSTA:-0.34пЉМдЄ≠дљН<6дЄ™жЬИAR:0.59пЉМдЄ≠дљН>6дЄ™жЬИAR:3.52;post-hoc Dunn ж£Ай™МпЉМи∞ГжХіеРОP=0.0037vs AR<6mo, P=7.4e-5 vs STA)(еЫЊ3A)гАВ
ељУињЫдЄАж≠•е∞ЖжОТжЦ•жВ£иАЕеИЖдЄЇABMRеТМйЭЮABMRжЧґпЉМжЧ†иЃЇеПСзФЯжОТжЦ•зЪДжЧґйЧіе¶ВдљХпЉМABMRзїДзЪДTCFrжШЊиСЧеҐЮеК†(AR ABMR vs STA, Wilcoxon P=0.04, ARйЭЮABMR vs STA Wilcoxon P=0.56)(еЫЊ3B)гАВ
жАїдљУиАМи®АпЉМ70.5%зЪДARжВ£иАЕзІїж§НеРОTCFrеҐЮеК†пЉМиАМSTAжВ£иАЕдЄЇ46.9% (Fisherз≤Њз°ЃпЉМp=0.03)(еЫЊ3C)гАВдЇЛеЃЮдЄКпЉМињЩжШѓеЫ†дЄЇиЃЄе§ЪARйШЯеИЧжВ£иАЕзЪДеЯЇзЇњTCFrйЭЮеЄЄдљОпЉМеЬ®жіїж£Аз°ЃиЃ§жОТжЦ•жЧґеє≥еЭЗжА•еЙІеҐЮеК†>10еАНгАВдЄОTCFrзЫЄеПНпЉМеѓєTCRеЇУеЕЛйЪЖжАІињЫи°Мз±їдЉЉеИЖжЮРжЧґпЉМеПѓдї•иІВеѓЯеИ∞ARеТМSTAйШЯеИЧдЄ≠зЪДеПЧиѓХиАЕдєЛйЧіж≤°жЬЙеЈЃеЉВ(и°•еЕЕеЫЊ2)пЉМињЩи°®жШОTCFrзЪДжЙ©еҐЮеПѓиГљжШѓзФ±дЇОTзїЖиГЮеЇУзЪДжХідљУеҐЮеК†пЉМиАМдЄНдїЕдїЕжШѓжЬАйЂШйҐСзОЗеЕЛйЪЖзЪДжЙ©еҐЮгАВ
4
TCRеЕНзЦЂеЇУйЂШеС®иљђеТМжА•жАІжОТжЦ•еПНеЇФ
еЫЊ4
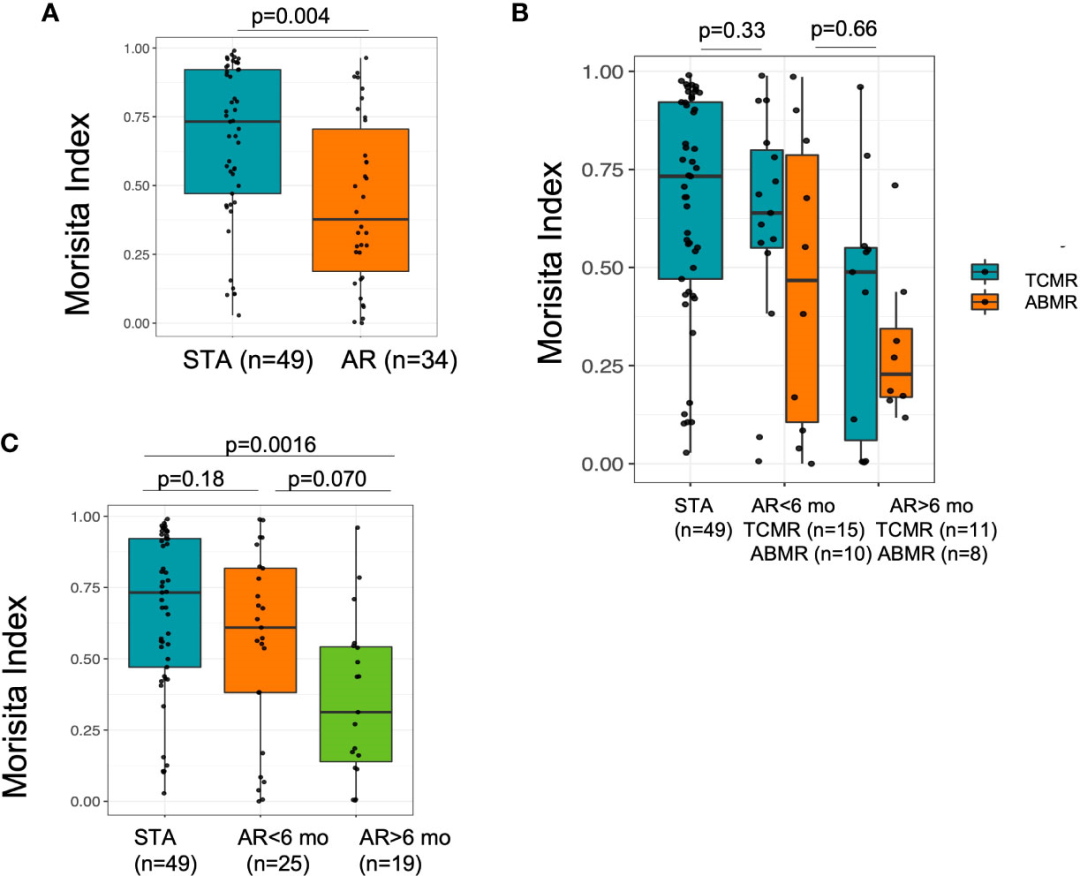
TзїЖиГЮеЇУеС®иљђдљњзФ®MorisitaжМЗжХ∞(22)ињЫи°МжµЛйЗПпЉМиѓ•жМЗжХ∞еЯЇдЇОдЄ§дЄ™ж†ЈжЬђдєЛйЧіеЕ±дЇЂзЪДеЕЛйЪЖжЭ•жѓФиЊГTзїЖиГЮзЪДжХ∞йЗПеТМйҐСзОЗгАВйАЪињЗжѓФиЊГSTAжВ£иАЕеТМARжВ£иАЕзЪДеЯЇзЇњж†ЈжЬђеТМзІїж§НеРОжФґйЫЖзЪДж†ЈжЬђзЪДйЕНеѓєеАЉжЭ•иѓДдЉ∞TCRеЇУиљђжНҐзЪДжЉФеПШпЉМSTAжВ£иАЕеТМARжВ£иАЕзЪДж†ЈжЬђеЭЗе§ІдЇО500дЄ™TзїЖиГЮгАВзФ±дЇОеЇУеС®иљђеПЧжЧґйЧізЪДељ±еУНпЉМеПѓдї•ж†єжНЃдїЦдїђзЪДARдЇЛдїґжШѓеПСзФЯеЬ®зІїж§НеРО6дЄ™жЬИеЙНињШжШѓ6дЄ™жЬИеРОињЫдЄАж≠•еИТеИЖARзїДгАВеС®иљђеҐЮеК†жЬАе§ЪзЪДжШѓARйШЯеИЧ(R=-0.33, p=0.029)(и°•еЕЕеЫЊ3)пЉМзІїж§НеРО6дЄ™жЬИеРОеЗЇзО∞жЩЪжЬЯжОТжЦ•еПНеЇФзЪДжВ£иАЕ(STAзЪДдЄ≠дљНMorisitaжМЗжХ∞:0.73пЉМзІїж§НеРОдЄНеИ∞6дЄ™жЬИзЪДARзЪДдЄ≠дљНMorisitaжМЗжХ∞:0.61пЉМзІїж§НеРО6дЄ™жЬИеРОARзЪДдЄ≠дљНMI:0.31, Kruskal-Wallis p=0.004)(еЫЊ4A)гАВ
дЄЇдЇЖињЫдЄАж≠•з†Фз©ґдЄіеЇКзЙєеЊБдЄОжВ£иАЕзЪДйЂШеС®иљђзОЗжШѓеР¶жЬЙеЕ≥пЉМзДґеРОеѓєABMRжВ£иАЕињЫи°МзїЖеИЖпЉМеПСзО∞дЄОжОТжЦ•з±їеЮЛж≤°жЬЙзїЯиЃ°е≠¶жДПдєЙ(еЫЊ4B)гАВињЩи°®жШОпЉМйЂШеС®иљђйАЪеЄЄдЄОжОТжЦ•еПНеЇФжЬЙеЕ≥пЉМиАМдЄНдїЕдїЕжШѓжКЧдљУдїЛеѓЉзЪДжОТжЦ•еПНеЇФжВ£иАЕпЉМдЄОжА•жАІжОТжЦ•еПНеЇФеПСзФЯзЪДжЧґйЧіжЧ†еЕ≥(p = 0.0016пЉМи∞ГжХіp)(еЫЊ4C)гАВ
жѓФиЊГзІїж§НеРОVеТМJеЯЇеЫ†зЪДдљњзФ®пЉМеПѓдї•иІВеѓЯеИ∞STAжВ£иАЕдЄ≠TCRBV18зЪДдљњзФ®зХ•жЬЙеҐЮеК†;зДґиАМпЉМељУдњЃж≠£е§ЪйЗНжµЛиѓХжЧґпЉМињЩеєґдЄНжШЊиСЧгАВж≤°жЬЙеЕґеЃГTCRB VеЯЇеЫ†и°®зО∞еЗЇеЈЃеЉВжШЊиСЧ(и°•еЕЕеЫЊ4A, B)гАВињЩдЇЫеПСзО∞и°®жШОпЉМеЬ®е≠§зЂЛзЪДзІїж§НеРОж†ЈжЬђдЄ≠жµЛйЗПTCRеЕНзЦЂеЇУзЪДеПШеМЦеПѓиГљдЄНиґ≥дї•йҐДжµЛжОТжЦ•еПНеЇФпЉМиАМжХіеРИзІїж§НеЙНжИЦеЯЇзЇњи°Ажґ≤ж†ЈжЬђдЄОзІїж§НеРОи°Ажґ≤ж†ЈжЬђдєЛйЧізЪДеПШеМЦе∞ЖжЫіжЬЙдїЈеАЉпЉМдї•иѓДдЉ∞еК®жАБеЇУзЪДдЄіеЇКељ±еУНгАВ
5
еЊЃеЊ™зОѓзВОзЧЗиѓДеИЖдЄОMorisitaжМЗжХ∞иѓДеИЖжШЊиСЧзЫЄеЕ≥
еЫЊ5
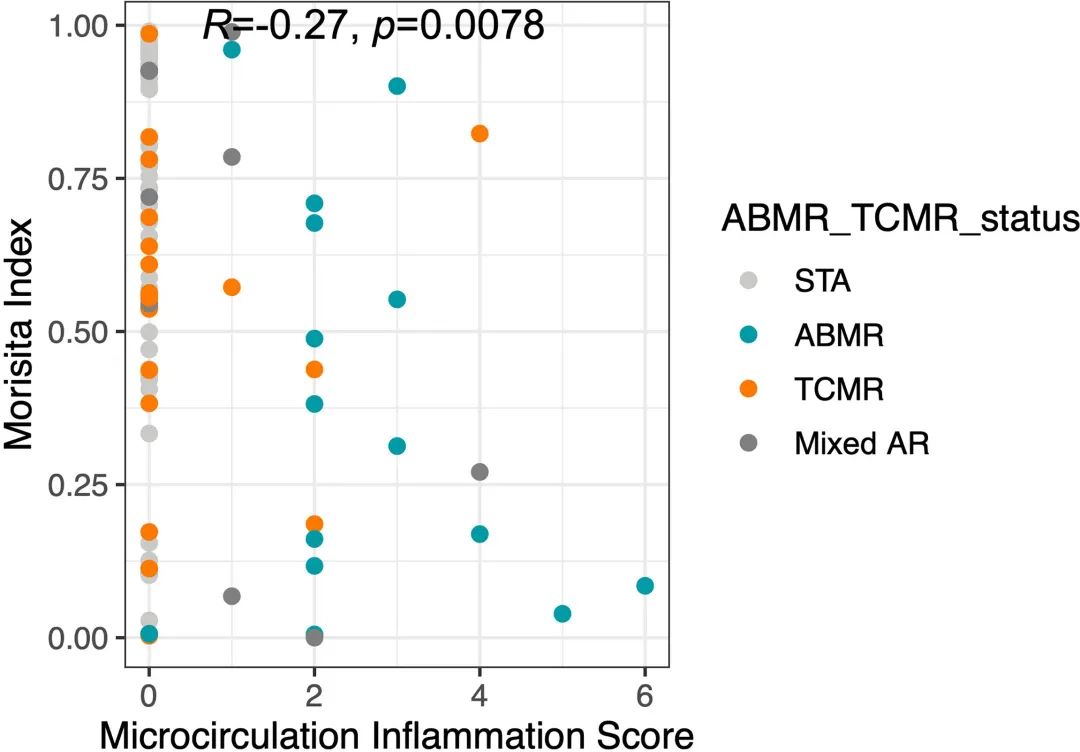
еЊЃеЊ™зОѓзВОзЧЗ(MI)жШѓдЄАдЄ™зіѓзІѓиѓДеИЖпЉМеМЕжЛђиВЊе∞ПзРГзВО(gs)еТМе∞ПзЃ°еС®еЫіжѓЫзїЖи°АзЃ°зВО(ptc)пЉМдЄОиВЊзІїж§НйҐДеРОиЊГеЈЃзЫЄеЕ≥(23)гАВеЬ®зІїж§НеРОж†ЈжЬђдЄ≠пЉМењГиВМжҐЧж≠їиѓДеИЖдЄОMorisitaжМЗжХ∞дєЛйЧіе≠ШеЬ®жШЊиСЧзЫЄеЕ≥жАІ(spearmanвАЩs Rho=-0.27, p=0.0078пЉМеЫЊ5)гАВеЬ®зІїж§НеРОж†ЈжЬђдЄ≠пЉМMorisitaжМЗжХ∞е∞ПдЇО0.3зЪДжВ£иАЕдЄ≠пЉМ43.5%зЪДжВ£иАЕењГиВМжҐЧж≠ї>0пЉМиАМењГиВМжҐЧж≠ї=0зЪДжВ£иАЕдЄЇ15.7% (Fisherз≤Њз°Ѓж£Ай™МпЉМp=0.009)гАВињЩи°®жШОйЂШеС®иљђзОЗеПѓиГљдЄОжЫідЄ•йЗНзЪДжОТжЦ•еПНеЇФжЬЙеЕ≥гАВ
05
иЃ®иЃЇ
жЬђз†Фз©ґиѓБеЃЮпЉМж£АжµЛеЕНзЦЂеЇУеПШеМЦдЄОзІїж§НеРОжОТжЦ•еПНеЇФзЫЄеЕ≥пЉМињЩи°®жШОTзїЖиГЮеПЧдљУжµЛеЇП(10)еПѓиГљдЄЇеПЧдљУжПРдЊЫзІїж§НеЙНеТМзІїж§НеРОжОТжЦ•й£ОйЩ©йҐДжµЛгАВиѓ•ж£АжµЛеЕЈжЬЙжљЬеЬ®зФ®дЇОзІїж§НеРОзЪДеЕНзЦЂжКСеИґеЖ≥з≠ЦзЪДиГљеКЫпЉМеЯЇдЇОTCRf/еЇУеС®иљђзОЗзЪДжА•еЙІеҐЮеК†пЉМеЕґдЄ≠зІїж§НеРОеЕНзЦЂеЇУйЂШеС®иљђзОЗзЪДйЙіеЃЪи°®жШОдЊЫдљУзЙєеЉВжАІгАБеПНеЇФжАІTзїЖиГЮзЪДжЙ©еҐЮгАВж≠£еЬ®ињЫи°МзЪДињЫдЄАж≠•еЈ•дљЬдЄ≠пЉМеЬ®жЦ∞зЪДжВ£иАЕзїДдЄ≠зЛђзЂЛй™МиѓБињЩдЇЫзїУжЮЬпЉМйАЪињЗTCRSeqеТМжµБеЉПзїЖиГЮжЬѓињЫдЄАж≠•з†іиѓСTзїЖиГЮжКЧеОЯиѓЖеИЂдЊЫдљУеИЇжњАзЪДеПЧдљУзїЖиГЮеҐЮжЃЦпЉМињЫдЄАж≠•дЇЖиІ£еЕЛйЪЖеЮЛеТМеС®иљђзКґжАБпЉМињЩжЬЙеК©дЇОиѓЖеИЂжШЊжАІи°®дљНпЉМеЬ®зІїж§НзЙ©еКЯиГљеЗЇзО∞дЄіеЇКжБґеМЦдєЛеЙНпЉМйҐДжµЛзІїж§НиВЊжОТжЦ•й£ОйЩ©гАВ
дїАдєИжШѓImmuHub¬ЃжКАжЬѓпЉЯ
жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљеЖЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂеЯЇеЫ†зїДе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇSeq-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛпЉМеєґжОИжЭГж≥ЫзФЯе≠РпЉИзЇ≥жЦѓиЊЊеЕЛдї£з†БпЉЪGTHпЉЙдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-TraqиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq |TзїЖиГЮеЕНзЦЂжµЛиѓДдї•еПКImmuHubеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier зЦЊзЧЕжЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБTCR-TиНѓзЙ©еЉАеПСз≠Йеє≥еП∞зЃ°зЇњгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВ

