
жИРдЇЇжА•жАІжЈЛеЈізїЖиГЮзЩљи°АзЧЕпЉИALLпЉЙзЪДйҐДеРОе≠ШеЬ®йЂШеЇ¶еЉВиі®жАІпЉМеПЧжВ£иАЕзЙєеЊБгАБзЦЊзЧЕзЙєеЊБз≠ЙеРДзІНеЫ†зі†зЪДељ±еУНгАВеПѓжµЛйЗПжЃЛзХЩзЧЕпЉИMRDпЉЙжШѓALLдЄіеЇКзїУжЮЬзЪДжЬЙеКЫйҐДжµЛжМЗж†ЗпЉМеПѓдї•иѓДдЉ∞ж≤їзЦЧеПНеЇФпЉМйҐДжµЛе§НеПСй£ОйЩ©пЉМйАРжЄРжИРдЄЇALLж≤їзЦЧеЖ≥з≠ЦдЄ≠зЪДж†ЄењГеЈ•еЕЈгАВ
MRDдЄНеРМж£АжµЛжЦєж≥ХзЪДжХПжДЯжАІгАБзЙєеЉВжАІеТМдЄіеЇКжДПдєЙжЬЙжЙАеЈЃеИЂпЉМдљХжЧґдї•еПКе¶ВдљХиѓДдЉ∞MRDпЉМе¶ВдљХеРИзРЖеЬ∞жМЗеѓЉдЄіеЇКеЖ≥з≠ЦеЕЈжЬЙе§НжЭВжАІгАВињСжЬЯгАКblood advancesгАЛжЭВењЧеПСи°®дЇЖдЄАзѓЗжЭ•иЗ™зЊОеЫљдЄУеЃґе∞ПзїДзЪДеЕ≥дЇОжИРдЇЇALL MRDж£АжµЛзЪДзїЉињ∞жЦЗзЂ†пЉМжАїзїУдЇЖMRDж£АжµЛеЇФзФ®дЄ≠зЪДеЄЄиІБдЄіеЇКйЧЃйҐШпЉМеєґзїЩеЗЇеРИзРЖеМЦеїЇиЃЃпЉМеѓєдЇОжИСдїђзЪДдЄіеЇКеЈ•дљЬдєЯеЕЈжЬЙеАЯйЙіеТМжМЗеѓЉжДПдєЙгАВеП¶е§ЦињЩзѓЗжЦЗзЂ†еѓєдЇОе¶ВдљХиІ£иѓїNGS MRDжК•еСКзїУжЮЬдєЯзїЩеЗЇдЇЖиѓ¶зїЖеїЇиЃЃгАВ
дЄЛйЭҐе∞±иЃ©жИСдїђдЄАиµЈжЭ•иѓ¶зїЖдЇЖиІ£дЄЛеРІ~

зЫЃеЙНеЄЄиІБзЪДеЗ†зІНMRDж£АжµЛжЦєж≥ХйГљеРДжЬЙеЕґдЉШзЉЇзВєпЉМжАїзїУе¶Ви°®1гАВ
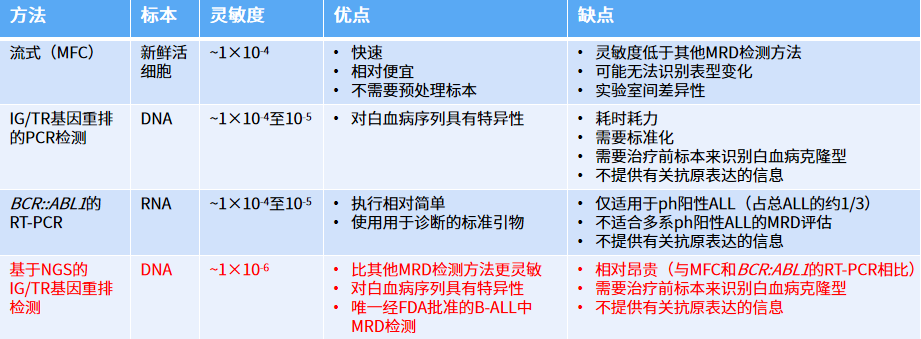
и°®1
еѓєдЇОB-ALLжВ£иАЕпЉМеЯЇдЇОNGSзЪДзЩљи°АзЧЕзЙєеЉВжАІIG/TR еЕЛйЪЖеЮЛ MRD еЃЪйЗПжШѓдЄіеЇКеЖ≥з≠ЦзЪДй¶ЦйАЙгАВеЫ†дЄЇиѓ•жЦєж≥ХжѓФеЕґдїЦж£АжµЛеЕЈжЬЙжЫійЂШзЪДзБµжХПеЇ¶еТМеѓєе§НеПСзЪДйЙіеИЂеКЫгАВ
еЬ®phйШ≥жАІALLжВ£иАЕдЄ≠пЉМNGSзЪДIG/TRж£АжµЛеТМBCR::ABL1зЪДRT-PCRжШѓMRDиѓДдЉ∞зЪДи°•еЕЕжЦєж≥ХгАВNGSжЦєж≥ХеѓєзЩљи°АзЧЕеЕЛйЪЖзЪДзЙєеЉВжАІйЂШдЇОBCR::ABL1зЪДRT-PCRпЉМеЫ†ж≠§еПѓиГљжЫійАВеРИйҐДжµЛйҐДеРОеТМе§Іе§ЪжХ∞ж≤їзЦЧеЖ≥з≠ЦгАВ
еѓєдЇОT-ALLжВ£иАЕпЉМIG/TRзЪДNGSж£АжµЛеТМеЕґдїЦMRDж£АжµЛжШѓMRDиѓДдЉ∞зЪДи°•еЕЕжЦєж≥ХгАВNGSжЦєж≥ХжѓФеЕґдїЦжЦєж≥ХеЕЈжЬЙжЫійЂШзЪДзБµжХПеЇ¶пЉМдљЖеЬ®T-ALLдЄ≠ињШж≤°жЬЙеЊЧеИ∞еЊИе•љзЪДй™МиѓБгАВ
ељУIG/TRзЪДNGSж£АжµЛеЫ†дЄЇжЯРдЇЫеОЯеЫ†дЄНеПѓзФ®жЧґпЉИжѓФе¶Вж≤°жЬЙеПѓињљиЄ™зЪДеЕЛйЪЖгАБзїПжµОжИРжЬђиАГиЩСгАБйЬАи¶БзіІжА•еЖ≥з≠ЦжЧґпЉЙпЉМжИЦйЬАи¶БиѓДдЉ∞жКЧеОЯи°®иЊЊдї•йАЙжЛ©жКЧеОЯеЃЪеРСеЕНзЦЂж≤їзЦЧжЧґпЉМMFCж£АжµЛеПѓдї•жПРдЊЫеЄЃеК©пЉМеТМеЕґдїЦMRDж£АжµЛзЫЄиЊЕзЫЄжИРгАВ
еѓєдЇОжЧ†ж≥ХињЫи°МIG/TRзЪДNGS MRDж£АжµЛзЪДphйШ≥жАІALLжВ£иАЕпЉМIG/TRзЪДPCRж£АжµЛдЉШдЇОBCR::ABL1зЪДRT-PCRжИЦMFCгАВеЬ®IG/TRзЪДNGSжИЦPCRйГљдЄНеПѓзФ®зЪДжГЕеЖµдЄЛпЉМBCR::ABL1зЪДRT-PCRдЉШдЇОMFCгАВ

MRDзЪДе§ЦеС®и°АпЉИPBпЉЙзЫСжµЛеЕЈжЬЙйБњеЕНдЊµеЕ•жАІй™®йЂУпЉИBMпЉЙйЗЗж†ЈзЪДдЉШзВєгАВжЬЙз†Фз©ґиѓБжШОдЇЖеЯЇдЇОPBеТМBMзЪДNGS MRDж£АжµЛзїУжЮЬеЕЈжЬЙеЊИеЉЇзЪДзЫЄеЕ≥жАІгАВдљЖжШѓPBдЄ≠зЪДзЦЊзЧЕиіЯжЛЕеПѓиГљжѓФBMдљО1еИ∞2дЄ™еѓєжХ∞еАНпЉМеЫ†ж≠§PBзЫСжµЛеПѓиГљжЧ†ж≥Хж£АжµЛеИ∞йЭЮеЄЄдљОж∞іеє≥зЪДMRDгАВ
еѓєдЇОBMеПЧзіѓзЪДжВ£иАЕпЉМеїЇиЃЃиЗ≥е∞СеЬ®иЃ∞ељХеИ∞MRDйШіжАІдєЛеЙНзЫСжµЛBM MRDгАВеЬ®дљњзФ®йЂШиі®йЗПBMж†ЈжЬђиЊЊеИ∞MRDйШіжАІеРОпЉМеПѓдї•иАГиЩСињЫи°МPB MRDзЫСжµЛпЉИеНХзЛђжИЦдЄОеЃЪжЬЯ BMиѓДдЉ∞дЇ§жЫњпЉЙпЉМжЬАе•љдљњзФ®йЂШзБµжХПеЇ¶зЪДNGS MRDж£АжµЛпЉМдї•еЗПе∞СдЊµеЕ•жАІBMж£АжЯ•зЪДйҐСзОЗгАВ
еѓєдЇОеНХзЇѓйЂУе§ЦзЦЊзЧЕпЉИе¶ВBзїЖиГЮжИЦTзїЖиГЮжЈЛеЈіжѓНзїЖиГЮжЈЛеЈізШ§пЉЙжВ£иАЕпЉМPB MRDзЫСжµЛеПѓиГљеЬ®дЄіеЇКдЄКжЬЙзФ®пЉМдљЖеЊИе∞СжЬЙжХ∞жНЃжФѓжМБеЕґеЬ®ињЩзІНжГЕеЖµдЄЛзЪДдљњзФ®гАВ

еЬ®жО•еПЧдЄАзЇњALLж≤їзЦЧзЪДжВ£иАЕдЄ≠пЉМиЊЊеИ∞MRDйШіжАІзЪДжЧґйЧіеЬ®й£ОйЩ©еИЖе±ВдЄ≠иµЈзЭАйЗНи¶БдљЬзФ®гАВеЕ≥дЇОMRDиѓДдЉ∞зЪДжЧґжЬЇеТМйҐСзОЗпЉМжИСдїђдєЛеЙНдєЯжАїзїУињЗеЫљеЖЕе§ЦжМЗеНЧеТМдЄУеЃґеЕ±иѓЖдЄ≠зЪДеїЇиЃЃпЉМиѓ¶иІБвАЬеП≤дЄКжЬАеЕ®жЈЛз≥їи°Ажґ≤иВњзШ§MRDж£АжµЛжЬАдљ≥жЧґжЬЇжАїзїУпЉБвАЭ
жО•еПЧдЄАзЇњALLж≤їзЦЧзЪДжВ£иАЕеЇФеЬ®иѓ±еѓЉеРОжО•еПЧMRDиѓДдЉ∞пЉМеЬ®жЬАеИЭзЪД2иЗ≥3еєіеЖЕиЗ≥е∞СжѓП3иЗ≥4дЄ™жЬИињЫи°МдЄАжђ°гАВеѓєдЇОиѓ±еѓЉеРОMRDдїНйШ≥жАІзЪДжВ£иАЕдї•еПКеЕЈжЬЙдЄНиЙѓй£ОйЩ©зЦЊзЧЕзЙєеЊБдЄФе§НеПСй£ОйЩ©зЫЄеѓєиЊГйЂШзЪДжВ£иАЕпЉМеЇФиАГиЩСжЫійҐСзєБзЪД MRDиѓДдЉ∞пЉИдЊЛе¶ВжѓП1-2дЄ™жЬИдЄАжђ°пЉМзЫіеИ∞иЃ∞ељХеИ∞MRD йШіжАІпЉЙгАВ
еѓєдЇОжО•еПЧеРМзІНеЉВдљУHSCTжИЦCAR-TзїЖиГЮж≤їзЦЧзЪДжВ£иАЕпЉМеЇФеЬ®HSCTжИЦCAR-TзїЖиГЮж≤їзЦЧеЙНињЫи°МMRDиѓДдЉ∞пЉИеѓєдЇОи°Ажґ≤е≠¶зЉУиІ£жВ£иАЕпЉЙпЉМеєґдЄФеЬ®HSCTжИЦCAR-Tж≤їзЦЧеРОзЪДиЗ≥е∞СзђђдЄАеєіеЖЕжѓП2иЗ≥3дЄ™жЬИињЫи°МдЄАжђ°гАВ
еЬ®з°ЃеЃЪдЄ™дљУжВ£иАЕзЪДMRDзЫСжµЛжМБзї≠жЧґйЧіжЧґпЉМеЇФиАГиЩСжАїдљУе§НеПСй£ОйЩ©гАБзФ®еЯЇдЇОPBзЪДйЂШзБµжХПеЇ¶MRDж£АжµЛдљЬдЄЇBMиѓДдЉ∞зЪДжљЬеЬ®жЫњдї£жЦєж°ИзЪДеПѓзФ®жАІгАБдї•еПКMRDзЫСжµЛзЪДжИРжЬђгАВ

дЄАдЇЫеЕЈжЬЙйЂШеН±зїЖиГЮеИЖе≠РзЙєеЊБзЪДжВ£иАЕжИЦжО•еПЧж†ЗеЗЖж≤їзЦЧе§НеПСй£ОйЩ©йЭЮеЄЄйЂШзЪДжВ£иАЕеПѓиГљдїОеРМзІНеЉВдљУHSCTдЄ≠иОЈзЫКгАВиЙѓе•љзЪДMRDеК®еКЫе≠¶пЉИжМБзї≠MRDйШіжАІпЉЙжШѓеР¶иГљжКµжґИдЄОйЂШеН±зїЖиГЮеИЖе≠РзЙєеЊБзЫЄеЕ≥зЪДдЄНиЙѓйҐДеРОпЉЯMRDдњ°жБѓеПѓиГљеѓєHSCTзЪДеЖ≥з≠ЦеЕЈжЬЙжМЗеѓЉжДПдєЙгАВ
еѓєдЇОж†ЗеН±ALLжВ£иАЕпЉИеМЕжЛђжЧ†IKZF1 plusеЯЇеЫ†еЮЛзЪДPh йШ≥жАІALLжВ£иАЕпЉЙеЬ®дЄАзЇњж≤їзЦЧеЉАеІЛеРОвИЉ3 дЄ™жЬИеЖЕйАЪињЗеЯЇдЇОNGSзЪДIG/TRж£АжµЛеТМ/жИЦйАЪињЗBCRпЉЪпЉЪABL1зЪД PCRпЉИеѓєдЇОPhйШ≥жАІALLпЉЙж£АжµЛиЊЊеИ∞MRDйШіжАІпЉМдЄНжО®иНРињЫи°МеЄЄиІДеРМзІНеЉВдљУHSCTгАВ
еѓєдЇОеЬ®1√Ч10-6зБµжХПеЇ¶дЄЛиЊЊеИ∞MRDйШіжАІзЪДйЂШеН±ALLжВ£иАЕпЉМж≤°жЬЙиґ≥е§ЯзЪДжХ∞жНЃжО®иНРжФѓжМБжИЦеПНеѓєеРМзІНеЉВдљУ HSCTпЉМеЇФж†єжНЃжВ£иАЕжДПжДњгАБжЫњдї£зЦЧж≥ХзЪДеПѓзФ®жАІеТМзІїж§НзЫЄеЕ≥ж≠їдЇ°й£ОйЩ©пЉМеБЪеЗЇдЄ™дљУеМЦеЖ≥еЃЪгАВеѓєдЇОжЬ™жО•еПЧеРМзІНеЉВдљУHSCTзЪДйЂШеН±жВ£иАЕпЉМеЇФињЫи°МMRDзЪДињЮзї≠зЫСжµЛгАВ
еЬ®жО•еПЧblinatumomabзЪДдЄАзЇњж≤їзЦЧеРОдїНдњЭжМБMRDйШ≥жАІзЪДжВ£иАЕйҐДеРОиЊГеЈЃпЉМеєґдЄФеПѓиГљеЬ®й¶Цжђ°зЉУиІ£жЧґеПЧзЫКдЇО HSCTгАВеЇФиАГиЩСеЬ®HSCTдєЛеЙНж†єйЩ§MRDзЪДз≠ЦзХ•пЉМеЫ†дЄЇMRDйШ≥жАІALLжВ£иАЕзЪДHSCTеРОзїУе±АиЊГеЈЃгАВ

еЬ®е§НеПС/йЪЊж≤їжАІжГЕеЖµдЄЛпЉМMRDйШіжАІзЪДеЃЮзО∞дєЯжШѓйҐДеРОеЫ†зі†дєЛдЄАгАВињЗеОїжЙАжЬЙйАЪињЗжМљжХСеМЦзЦЧиЊЊеИ∞зЉУиІ£зЪДе§НеПС/йЪЊж≤їжАІALLжВ£иАЕйÚ襀忯聁ињЫи°МеРМзІНеЉВдљУHSCTдљЬдЄЇеФѓдЄАзЪДж≤їжДИжЬЇдЉЪпЉМдљЖйЪПзЭАеЕНзЦЂзЦЧж≥ХзЪДињЫе±ХпЉМињЩзІНиЃ§зЯ•еЬ®еПСзФЯеПШеМЦгАВ
е§НеПС/йЪЊж≤їжАІALLжВ£иАЕеЇФжО•еПЧеЉВеЯЇеЫ†HSCTжИЦCAR-tзїЖиГЮж≤їзЦЧпЉИжЬАе•љжШѓеЬ®дЄіеЇКиѓХй™МзЪДиГМжЩѓдЄЛпЉЙпЉМжЧ†иЃЇMRDеѓєжМљжХСжАІж≤їзЦЧзЪДеПНеЇФе¶ВдљХгАВеЬ®ињЩдЇЫеЈ©еЫЇжЦєж≥ХдєЛеЙНж†єйЩ§MRDдЄОжЫіе•љзЪДйҐДеРОзЫЄеЕ≥пЉМдљЖдЄНжШѓеѓєжЙАжЬЙжВ£иАЕйГљеПѓи°МгАВ
е¶ВжЮЬзђ¶еРИжЭ°дїґпЉМеЇФе∞ЖCAR-Tж≤їзЦЧеРОж£АжµЛеИ∞MRDйШ≥жАІзЪДжВ£иАЕиљђиѓКињЫи°МеЉВеЯЇеЫ†HSCTжИЦз†Фз©ґжАІMRDеЃЪеРСж≤їзЦЧгАВ

зЫЃеЙНжЬЙеЗ†зІНжЬЙжХИзЪДйЭЮзІїж§НзЦЧж≥ХеПѓзФ®дЇОMRDйШ≥жАІB-ALLжВ£иАЕзЪДж≤їзЦЧпЉМжѓФе¶ВжЬЙз†Фз©ґжХ∞жНЃи°®жШОBlinatumomabеѓєжМБзї≠жАІжИЦе§НеПСжАІMRDйШ≥жАІзЪДB-ALLжВ£иАЕеЕЈжЬЙеЊИе•љзЪДзЦЧжХИпЉМinotuzumab ozogamicinеТМCD19 CAR-Tж≤їзЦЧдєЯеПѓиГљжЬЙжХИгАВ
ињЫи°МйАВељУж≤їзЦЧеРОдїНиГљжМБзї≠ж£АжµЛеИ∞MRDзЪДжВ£иАЕжИЦMRD е§НеПСзЪДжВ£иАЕеЇФжО•еПЧMRDеЃЪеРСж≤їзЦЧгАВе¶ВжЮЬжЬЙйЂШеПѓдњ°еЇ¶жК•еСКзЪДзїУжЮЬеПНжШ†зЬЯеЃЮMRDзЪДе≠ШеЬ®пЉМжЧ†иЃЇеЕґж∞іеє≥е¶ВдљХпЉМйГљеїЇиЃЃињЫи°Меє≤йҐДгАВ
еѓєдЇОе§Іе§ЪжХ∞MRDжМБзї≠е≠ШеЬ®жИЦе§НеПСдЄФжЧҐеЊАжЬ™жО•еПЧињЗ CD19йЭґеРСж≤їзЦЧзЪДB-ALLжВ£иАЕпЉМжО®иНРдљњзФ® BlinatumomabгАВ
еѓєдЇОеРИйАВзЪДжВ£иАЕпЉМдєЯеПѓдї•иАГиЩСдљњзФ®inotuzumab ozogamicinгАБCD19 CAR-TзїЖиГЮзЦЧж≥ХжИЦз†Фз©ґжАІMRDйЭґеРСзЦЧж≥ХпЉМжЬАе•љжШѓеЬ®дЄіеЇКиѓХй™МзЪДиГМжЩѓдЄЛгАВ

ж≠£з°ЃзРЖиІ£IG/TRзЪДNGS MRDж£АжµЛзїУжЮЬжЬЙеК©дЇОеЫізїХж≤їзЦЧеє≤йҐДеБЪеЗЇж≤їзЦЧеЖ≥з≠ЦгАВеЯЇдЇОNGS MRDеИЖжЮРзЪДеЄЄиІБйЧЃйҐШеТМиІ£з≠Фе¶Ви°®2жЙАз§ЇгАВ

и°®2
ељУйЗЗзФ®IG/TRзЪДNGS MRDж£АжµЛжЧґпЉМеЬ®еЉАеІЛMRDеЃЪеРСж≤їзЦЧдєЛеЙНпЉМењЕй°їеМЇеИЖдЄіеЇКзЫЄеЕ≥зЪДMRDдЄОдљОж∞іеє≥гАБйЭЮжБґжАІиГМжЩѓеЇПеИЧгАВйЗНе§НжµЛиѓХдї•иѓДдЉ∞еЕЛйЪЖеЮЛзЪДеК®жАБеПШеМЦеПѓиГљжЬЙеК©дЇОеМЇеИЖзЬЯж≠£зЪДMRDеТМдЄіеЇКдЄКжЧ†жДПдєЙзЪДиГМжЩѓеЇПеИЧгАВ
еЇФи∞®жЕОиІ£йЗКT-ALLжВ£иАЕдЄ≠襀蜚誙зЪДTRеЇПеИЧзЪДдљОж∞іеє≥MRDпЉМеЫ†дЄЇеЬ®T-ALLдЄ≠еМЇеИЖеЕЈжЬЙдЄіеЇКжДПдєЙзЪДMRDдЄОиГМжЩѓеЇПеИЧе∞§еЕґеЕЈжЬЙжМСжИШжАІгАВ
еЬ®ж®°ж£±дЄ§еПѓзЪДжГЕеЖµдЄЛпЉМеЇФеЬ®еЉАеІЛж≤їзЦЧеЙНжЭГи°°MRDеЃЪеРСж≤їзЦЧзЪДй£ОйЩ©еТМзЫКе§ДгАВеѓєдЇОдЄНз°ЃеЃЪж£АжµЛеИ∞зЪДдљОж∞іеє≥еЇПеИЧжШѓеР¶дї£и°®зЬЯеЃЮMRDиАМеїЇиЃЃиІВеѓЯзЪДзЧЕдЊЛпЉМеЇФињЫи°МйЭЮеЄЄеѓЖеИЗзЪДињЮзї≠зЫСжµЛдї•иІВеѓЯеЇПеИЧзЪДеК®жАБеПШеМЦпЉМеєґеЬ® MRDж∞іеє≥жШОжШЊдЄКеНЗиґЛеКњзЪДжГЕеЖµдЄЛеЉАеІЛMRDеЃЪеРСж≤їзЦЧгАВ
ељУж†єжНЃMRDзїУжЮЬеБЪеЗЇж≤їзЦЧеЖ≥з≠ЦжЧґпЉМйЬАзЙҐиЃ∞MRDзЪДйҐДеРОељ±еУНеПЦеЖ≥дЇОзОѓеҐГпЉМеПЧжЙАзФ®ж£АжµЛжЦєж≥ХеПКеЕґзБµжХПеЇ¶/зЙєеЉВжАІгАБиѓДдЉ∞жЧґжЬЇеТМзЦЊзЧЕзЫЄеЕ≥зЙєеЊБпЉИе¶ВзїЖиГЮеИЖе≠Рй£ОйЩ©пЉЙз≠ЙеПШйЗПзЪДељ±еУНгАВеЯЇдЇОNGSзЪДMRDж£АжµЛеПѓдї•иЊЊеИ∞1 √Ч 10-6зЪДзБµжХПеЇ¶пЉМињЩжЬЙеК©дЇОжЫіеЗЖз°ЃеЬ∞иѓДдЉ∞ж≤їзЦЧеПНеЇФгАБй£ОйЩ©еИЖе±ВеТМйҐДжµЛе§НеПСй£ОйЩ©гАВйЪПзЭАеЬ®дЄіеЇКзОѓеҐГдЄ≠дљњзФ®жЫіжЦ∞зЪДгАБйЂШзБµжХПеЇ¶зЪДMRDеИЖжЮРзФЯжИРжЫіе§ЪжХ∞жНЃпЉМMRDж£АжµЛзЪДдљЬзФ®еПѓиГљдЉЪињЫдЄАж≠•жЙ©е§ІпЉМжЬЙжЬЫжПРйЂШ ALL жВ£иАЕзЪДж≤їжДИзОЗгАВ
еПВиАГжЦЗзМЃ
Short NJ, et al. Clinical use of measurable residual disease in adult ALL: recommendations from a panel of US experts. Blood Adv. 2025 Mar 25;9(6):1442-1451. doi: 10.1182/bloodadvances.2024015441.

иЙЊж≤РиТљдЄУж≥®дЇОеЕНзЦЂзїДдЇМдї£жµЛеЇПйҐЖеЯЯе§ЪеєіпЉМжШѓеЕ®еЫљй¶ЦеЃґжО®еЗЇи°Ажґ≤иВњзШ§NGS MRDж£АжµЛдЇІеУБSeq-MRD¬ЃзЪДеЕђеПЄгАВSeq-MRD¬ЃйАВзФ®дЇОB/Tз≥їзЩљи°АзЧЕгАБB/Tз≥їжЈЛеЈізШ§гАБе§ЪеПСжАІй™®йЂУзШ§пЉМиГље§ЯеЄЃеК©дЄіеЇКеМїзФЯйҐДжµЛйХњжЬЯзЦЧжХИгАБиѓДдЉ∞ж≤їзЦЧжХИжЮЬгАБзЫСжµЛзЉУиІ£зКґжАБдї•еПКж£АжµЛжЧ©жЬЯе§НеПСгАВзїПињЗе§ЪеєізЪДзІѓзіѓеТМеПСе±ХпЉМSeq-MRD¬ЃеЬ®дЄіеЇКж£АжµЛеТМзІСе≠¶з†Фз©ґдЄКеЭЗеПЦеЊЧдЄНе∞СжИРжЮЬпЉМеєґиОЈеЊЧеЫљйЩЕеЄВеЬЇиЃ§еПѓгАВ
иОЈеЊЧжђІзЫЯCEиµДиі®иЃ§иѓБ
Seq-MRD¬ЃиОЈеЊЧжђІзЫЯCEиµДиі®пЉИж≥®еЖМеПЈпЉЪDE/CA20/01-IVD-Luxuslebenswelt-190/22пЉЙпЉМиОЈжЙєзЪДжШѓдЇЇжЈЛеЈіBзїЖиГЮеЊЃе∞ПжЃЛзХЩзЧЕеЯЇеЫ†ж£АжµЛиѓХеЙВзЫТпЉИеПѓйАЖжЬЂзЂѓзїИж≠ҐжµЛеЇПж≥ХпЉЙгАВ¬†

иОЈеЊЧдЄЙй°єеПСжШОдЄУеИ©
иЙЊж≤РиТљжО®еЗЇзЪДSeq-MRD¬Ѓи°Ажґ≤зЩМзЧЗMRDж£АжµЛжШѓжЬАжЧ©жЙєеЃЮзО∞еХЖдЄЪеМЦзЪДдЇІеУБпЉМиЗ™2016еєіз†ФеПСдЄУеИ©жКАжЬѓиЗ≥дїКпЉМиЙЊж≤РиТљSeq-MRD¬ЃеЈ≤зїПиОЈеЊЧ3й°єеЫљеЃґеПСжШОдЄУеИ©пЉЪ
[1]вАЬдЄАзІНеЇФзФ®дЇОйЂШйАЪйЗПжµЛеЇПж£АжµЛTзїЖиГЮзЩљи°АзЧЕеЊЃе∞ПжЃЛзХЩзЧЕзЪДеЉХзЙ©зїДеРИеПКиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2016 11204857.0пЉМжОИжЭГеЕђеСКеПЈ:CN 106957906 BпЉЙ
[2]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДиѓХеЙВзЫТвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1550133.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109652518 BпЉЙ
[3]вАЬдЄАзІНж£АжµЛеЊЃе∞ПжЃЛзХЩзЧЕMRDзЪДжЦєж≥ХвАЭпЉИдЄУ еИ© еПЈ: 2018 1 1549203.0пЉМжОИжЭГеЕђеСКеПЈ: CN 109680062 BпЉЙ

иОЈеЊЧзЫЄеЕ≥иљѓдїґиСЧдљЬ
[1]вАЬеЕНзЦЂзїДеЇУMRDж£АжµЛиЗ™еК®еМЦжК•еСКз≥їзїЯ[зЃАзІ∞ImmuReport] V1.0вАЭпЉИзЩїиЃ∞еПЈпЉЪ2019SR0916207пЉЙ
[2]вАЬSeq-MRDж£АжµЛиЗ™еК®еМЦеИЖжЮРз≥їзїЯпЉИDiscTermiteпЉЙ[зЃАзІ∞пЉЪDiscTermite]0.4.6вАЬпЉИзЩїиЃ∞еПЈпЉЪ2019SR1131517пЉЙ
[3]вАЬеЯЇдЇОеЕНзЦЂзїДеЇУдЇМдї£жµЛеЇПзЪДеЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛжХ∞жНЃе§ДзРЖз≥їзїЯвАЭпЉИзЩїиЃ∞еПЈпЉЪ2020SR0507594пЉЙ

иОЈеЊЧиН£и™ЙиѓБдє¶
1гАБиЙЊж≤РиТљиБФеРИжµЩе§ІйЩДдЄАйїДж≤≥жХЩжОИеЃМжИРзЪДгАКжЦ∞еЮЛCAR-TзїЖиГЮз†ФеПСеПКеЕґж≤їзЦЧжБґжАІи°Ажґ≤зЧЕдЄіеЇКиљђеМЦеИЫжЦ∞дљУз≥їеїЇзЂЛгАЛиОЈ2023еєіеЇ¶жµЩж±ЯзЬБзІСе≠¶жКАжЬѓињЫж≠•е•ЦдЄАз≠Йе•ЦгАВSeq-MRD¬ЃеЬ®иѓ•жКАжЬѓзЪДеИЫжЦ∞дЄОеЇФзФ®дЄ≠иµЈеИ∞дЇЖеЕ≥йФЃжАІдљЬзФ®гАВ

2гАБиЙЊж≤РиТљзФ≥жК•зЪДвАЬеЕНзЦЂзїДTCR/IgйЂШйАЪйЗПжµЛеЇПжКАжЬѓ/и°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛ/Seq-MRD¬ЃвАЭеЫ†еЕґеИЫжЦ∞жАІгАБеЙНж≤њжАІгАБеЄВеЬЇеЃЮзФ®жАІиН£иОЈвАЬ2022еєіеЇ¶CCTBдЄ≠еЫљиВњзШ§ж†ЗењЧзЙ©дЇІдЄЪеИЫжЦ∞е§ІдЉЪеИЫжЦ∞жКАжЬѓ/дЇІеУБиѓДйАЙвАЭй°єзЫЃдЇМз≠Йе•ЦгАВ

2023еєіиОЈжЙєдЇЖгАРеЕ®и°А/й™®йЂУеЯЇеЫ†зїДDNAжПРеПЦиѓХеЙВзЫТгАСпЉИз¶їењГеРЄйЩДжЯ±ж≥ХпЉЙе§Зж°ИзЉЦеПЈпЉЪжµЩжЭ≠жҐ∞е§З20230798 пЉМиѓХеЙВзЫТеИЖеИЂйАВзФ®дЇОдЇЇе§ЦеС®и°АгАБй™®йЂУж†ЈжЬђзЪДж†ЄйЕЄзЪДжПРеПЦгАВ
еПСи°®зЫЄеЕ≥жЦЗзМЃ
Seq-MRD¬ЃеПСи°®зЫЄеЕ≥жЦЗзМЃ
1гАБHuang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H.¬†Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. Bone Marrow Transplant.¬†2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

2гАБChen H, Gu M, Liang J, Song H, Zhang J, Xu W, Zhao F, Shen D, Shen H, Liao C, Tang Y, Xu X.¬†Minimal residual disease detection by next-generation sequencing of different immunoglobulin gene rearrangements in pediatric B-ALL.¬†Nat Commun. 2023 Nov 17;14(1):7468. doi: 10.1038/s41467-023-43171-9. пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

3гАБMin’er Gu,Yahong Xia, Jingying Zhang, Yongmin Tang, Weiqun Xu, Hua Song ¬†Xiaojun Xu.¬†The effectiveness of blinatumomab in clearing measurable residual disease in pediatric B-cell acute lymphoblastic leukemia patients detected by next-generation sequencing.¬† Cancer Med. 2023 Dec;12(24):21978-21984. doi:10.1002/cam4.6771. пЉИзВєеЗїйУЊжО•еПѓжЯ•зЬЛжЦЗзЂ†еЖЕеЃєпЉЙ

4гАБYan N, Wang ZL, Wang XJ, etпЉМal.¬†Measurable residual disease testing by next generation sequencing is more accurate compared with multiparameter flow cytometry in adults with B-cell acute lymphoblastic leukemia.¬†Cancer Lett. 2024 Jul 4;598:217104. doi: 10.1016/j.canlet.2024.217104.

иОЈеЊЧеЫљйЩЕеЄВеЬЇиЃ§еПѓ
2023еєіDelveInsightеЕђеПЄеПСеЄГзЪДMRDеЫљйЩЕеЄВеЬЇз†Фз©ґжК•еСКдЄ≠пЉМиЙЊж≤РиТљ/Seq-MRD¬ЃжШѓдЄ≠еЫљеФѓдЄАдЄАеЃґеЕђеПЄ/дЇІеУБињЫеЕ•еЫљйЩЕи∞Гз†ФеЄВеЬЇжК•еСКгАВDelveInsightжШѓдЄАеЃґйҐЖеЕИзЪДеМїзЦЧдњЭеБ•еЄВеЬЇз†Фз©ґеТМеХЖдЄЪеҮ胥еЕђеПЄпЉМдї•еЕґзО∞жИРзЪДиБФеРИеЄВеЬЇз†Фз©ґжК•еСКдї•еПКдЄЇеМїзЦЧдњЭеБ•и°МдЄЪзЪДеЕђеПЄжПРдЊЫзЪДеЃЪеИґиІ£еЖ≥жЦєж°ИиАМйЧїеРНгАВ

жЭ≠еЈЮиЙЊж≤РиТљзФЯзЙ©зІСжКАжЬЙйЩРеЕђеПЄжИРзЂЛдЇО2016еєіпЉМжШѓеЫљйЩЕеЙНж≤њзЪДдЄУж≥®дЇОеЕНзЦЂй©±еК®еМїе≠¶жКАжЬѓзЪДеЫљеЃґйЂШжЦ∞жКАжЬѓдЉБдЄЪгАВеИЫеІЛдЇЇеЫҐйШЯжЭ•иЗ™зЊОеЫљиКЭеК†еУ•е§Іе≠¶пЉМеЬ®2010еєіеЉАеІЛдљњзФ®еЕНзЦЂзїДеЯЇеЫ†йЂШйАЪйЗПжµЛеЇПжКАжЬѓеЉАе±ХеРДзІНзЦЊзЧЕзЫЄеЕ≥з†Фз©ґпЉМдЇО2016еєійАЪињЗиЗ™дЄїз†ФеПСпЉМеЕ®еЫљй¶ЦеЃґжО®еЗЇNGS-MRDи°Ажґ≤иВњзШ§еЊЃе∞ПжЃЛзХЩзЧЕпЉИMRDпЉЙж£АжµЛSeq-MRD¬ЃпЉМеєґжОИжЭГж≥ЫзФЯе≠РдљњзФ®гАВеРМжЧґпЉМеЕђеПЄжЛ•жЬЙImmun-Traq¬ЃиВњзШ§ж≤їзЦЧдЉійЪПиѓКжЦ≠гАБImmun-Cheq¬Ѓ¬†|еЕНзЦЂеКЫжµЛиѓДдї•еПКImmuHub¬ЃеЕНзЦЂзїДжµЛеЇПзІСз†ФжЬНеК°дЇІеУБпЉМеєґеЄГе±АжЬЙеЯЇдЇОAIжЬЇеЩ®е≠¶дє†зЃЧж≥ХзЪДT-classifier¬ЃиВњзШ§жЧ©з≠ЫгАБеНХзїЖиГЮжµЛеЇПгАБTCR-TеТМжКЧдљУеПСзО∞з≠Йеє≥еП∞зЃ°зЇњгАВзЫЃеЙНдЄЇж≠ҐеПСи°®дЇЖжХ∞еНБзѓЗиЃЇжЦЗпЉМеЕґдЄ≠еМЕжЛђпЉЪThe New England Journal of Medicine(IF:158.5), Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24),¬†Nature Communications¬†(IF:17)з≠Йе§ЪзѓЗйЂШеИЖжЭВењЧгАВеЕђеПЄжЮДеїЇеЗ†еНБй°єеПСжШОдЄУеИ©еТМиљѓдїґиСЧдљЬжЭГдЄЇж†ЄењГзЪДиЗ™дЄїзЯ•иѓЖдЇІжЭГдљУз≥їпЉМдЄЇеМїйЩҐдЄіеЇКгАБзФЯеСљзІСе≠¶з†Фз©ґгАБжЦ∞иНѓеЉАеПСз≠ЙжПРдЊЫиІ£еЖ≥жЦєж°ИеТМдЇІеУБгАВиЙЊж≤РиТљдЄУж≥®дЇОйАЪињЗиІ£з†БйАВеЇФжАІеЕНзЦЂз≥їзїЯжЭ•жФєеПШзЦЊзЧЕзЪДиѓКжЦ≠еТМж≤їзЦЧпЉМеєґиЗіеКЫдЇОжО®ињЫеЕНзЦЂй©±еК®еМїе≠¶йҐЖеЯЯеПСе±ХгАВ


