近日,艾沐蒽宣布自主研发的人T细胞组库动态检测试剂盒(可逆末端终止测序法)Immun-Traq®癌症治疗伴随诊断获得欧盟CE资质(注册号:AT/CA01/I0019269)。
Immun-Traq® | 肿瘤治疗伴随诊断,基于免疫组二代高通量测序(NGS)技术,通过特异性对病患血液里的T细胞受体(TCR)基因进行多样性和克隆性检测分析,同时结合病患所使用的治疗方法综合评估,来帮助医疗工作者和癌症病人预测和评估治疗的效果,让病患能在对抗癌症的斗争中更有效地选择治疗手段,并且避免浪费癌症病人治疗的时间和金钱。
Immun-Traq®的主要特点:
01
灵敏度高通过治疗前后T细胞的多态性和克隆性变化来评估患者的免疫情况
02
使用无创的样本收集方式——血液样本采集(也可针对肿瘤组织活检样本)
03
采用先进且成熟的技术——二代基因测序
04
通过世界领先的生物信息学分析算法诠释临床信息
检测意义
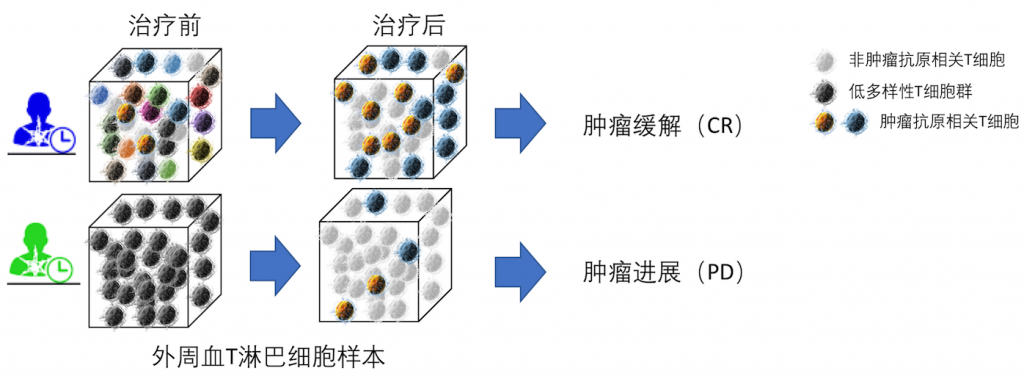
在治疗前,根据T细胞多样性和单克隆T细胞,可以更准确预测出患者是否能从即将采用的治疗方法中获益,让病患在对抗癌症的过程中更有效地选择治疗方案
在治疗后,根据患者体内T细胞多样性和克隆性变化,帮助医生和患者判断正在使用的肿瘤治疗的疗效,避免浪费病人的时间、金钱和生命,以防错过最佳治疗时机。
适用人群
各类癌症患者,如肺癌、乳腺癌、胃癌、结直肠癌、肝癌、食管癌、宫颈癌等癌症患者
送样要求
(1)使用EDTA抗凝管,采集新鲜外周血10mL,4℃保存运输,48h内送达。
(2)组织样本量5mg以上,干冰、液氮或RNAlater液条件下保存和运输。
关于Immun-Traq®合作
2022年5月26日,艾沐蒽就与迈迪科达成战略合作:基于迈迪科DC疫苗在癌症中的治疗,艾沐蒽将利用其Immun-Traq®测序免疫分析平台来监测患者治疗过程中的TCR变化。其目标便是利用TCR测序和免疫大数据分析,有效地对免疫治疗效果进行评价。
关于Immun-Traq®过往发表研究成果
1. Sheng J, Wang H, Liu X, Deng Y, Yu Y, Xu P, Shou J, Pan H, Li H, Zhou X, Han W, Sun T, Pan H, Fang Y. Deep Sequencing of T-Cell Receptors for Monitoring Peripheral CD8+ T Cells in Chinese Advanced Non-Small-Cell Lung Cancer Patients Treated With the Anti-PD-L1 Antibody. Front Mol Biosci ( 2021).
2. Jiang, H., Zheng, Y., Qian, J. et al. Efficacy and safety of sintilimab in combination with chemotherapy in previously untreated advanced or metastatic nonsquamous or squamous NSCLC: two cohorts of an open-label, phase 1b study. Cancer Immunol Immunother (2020).
3. Wang,X. et al. Quantitative characterization of T-cell repertoire alteration in Chinese patients with B-cell acute lymphocyte leukemia after CAR-T therapy. Bone Marrow Transplantation (2019).
关于CE
CE标志(CE Marking)是按照法规要求,部分产品在部分欧洲国家上市时,必须带有的产品安全标志。带有CE标志的产品意味着产品符合欧盟相关产品法规基本/通用要求,适于预期用途,可以在要求CE标志的国家自由流通。